 Параканкрозная (перифокальная) пневмония представляет собой очаг воспаления, развивающийся вокруг злокачественного образования (карциномы). Заболевание возникает в результате осложнения карциномы легких, соответственно без онкологического процесса данный недуг не развивается. Болезнь тяжело поддается лечению вследствие сниженного иммунитета и онкологии, усугубляющей течение параканкроза.
Параканкрозная (перифокальная) пневмония представляет собой очаг воспаления, развивающийся вокруг злокачественного образования (карциномы). Заболевание возникает в результате осложнения карциномы легких, соответственно без онкологического процесса данный недуг не развивается. Болезнь тяжело поддается лечению вследствие сниженного иммунитета и онкологии, усугубляющей течение параканкроза.
Причины заболевания
Развитию болезни способствуют следующие факторы:
- Первый – ослабление местного иммунитета вокруг злокачественного образования;
- Второй – ухудшение проходимости в дыхательных путях, в результате распада опухоли или прорастания ее в легочную ткань.
Возбудителями заболевания наиболее часто являются пневмококки и клебсиеллы, а также микоплазмы, вирусы, легионеллы и хламидии.
Предрасполагающие факторы
Основанием развития патологии является злокачественный процесс, протекающий в легких, однако не у каждого больного возникает данное заболевание.
Возникновению заболевания предрасполагают неблагоприятные факторы:
- пагубные привычки (курение, алкоголь);
- хронические заболевания органов дыхания;
- неполноценное питание;
- ослабленный иммунитет, обусловленный хроническими переутомлениями, стрессами, простудными болезнями;
- работа в неблагоприятных условиях – загрязненный воздух, сквозняки или морозы.
Данные факторы изменяют микроциркуляцию легких, способствуя развитию болезни.
Симптомы
Типичные признаки параканкрозного воспаления:
- подъем температуры (до 39 градусов);
- боли в груди, усиливающиеся во время вдоха;
- кашель;
- одышка;
- мокрота с примесью крови;
- нарастающая интоксикация, проявляющаяся тошнотой, слабостью, отсутствием аппетита.
Появляется одышка, вследствие чего развивается дыхательная недостаточность. Кашель носит тяжелый, мучительный характер, не приносящий облегчения. Из-за суженых дыхательных путей с трудом отделяется мокрота.
Характерными признаками пневмонии являются боли в груди, обостряющиеся при вдохе, в связи с чем больной вынужден переходить на поверхностное дыхание для уменьшения болезненности.
Диагностика
При предположении карциномы у больного с признаками воспаления легких необходимо выполнение дополнительных исследований для более точной диагностики.
Диагностические мероприятия включают:
- рентгенография грудной клетки;
- компьютерная томография;
- бронхография;
- бронхоскопия вместе с биопсией;
- торакотомия;
- пункция плевры.
Отличительной особенностью данной пневмонии является отсутствие положительной динамики и изменение рентгенологической картины на фоне антибиотикотерапии.
Лечение
Лечением такого заболевания в совокупности занимаются два специалиста: пульмонолог с онкологом. Схема лечения данного воспаления легких существенно отличается от остальных видов пневмоний.
Антибактериальная терапия
Антибактериальная терапия, при всей ее малой эффективности именно для этого типа пневмонии, назначается в целях купирования воспаления и дальнейшего его распространения. Для лечения используются препараты группы фторхинолов, макролидов и пенициллинов, а после полученных результатов бак-посева назначается антибактериальный препарат, наиболее эффективный к данному виду бактерий.
Дезинтоксикация
В целях снижения интоксикации больному проводится инфузионная терапия в совокупности с мочегонными средствами (диуретиками). В дополнении к лечению могут быть назначены гемосорбция или плазмоферез.
Улучшение дренажа бронхов
Для повышения дренажной функции дыхательных органов и очищения их от вязкой мокроты используются бронхолитические (бронхорасширяющие) и муколитические средств для разжижения тягучей мокроты, для наилучшего ее отхождения.
Противораковая терапия
Для сокращения роста опухоли применяется лучевая или химиотерапия. Поскольку противораковое лечение на фоне сопутствующей пневмонии опасно усилением воспаления вследствие большего подавления иммунитета, сначала необходимо снять острую симптоматику параканкрозного процесса, после чего проводить лечение онкологии.
Хирургическое лечение
При отсутствии положительной динамики консервативного лечения проводится хирургическое вмешательство. Операция показана при условии ее осуществления: отсутствии метастаз и разложения опухоли. В данной ситуации удаляется легочная ткань вместе с опухолью.
Последствия
Перифокальная пневмония при отсутствии адекватного лечения, опасна своими осложнениями с летальным исходом:
- Сепсис. При большом количестве токсинов в крови развивается обширное воспаление всего организма больного.
- Плеврит. Из-за наличия жидкости в плевре развивается воспаление плевральной оболочки.
- Дыхательная недостаточность. В результате нарушения работы дыхательной системы и невозможности усваивать кислород развивается дыхательная недостаточность.
- Ателектаз. Спадание участка легкого, в результате которого снижается наполнение альвеол кислородом.
Прогноз
Параканкрозная пневмония является нехорошим признаком при онкологии легкого. Относительно благоприятным прогноз может быть в случае незначительных размерах опухоли и отсутствии метастазирования. Своевременное обращение к специалисту и адекватная терапия увеличивают шансы больного на выздоровление.
Источник: ingalin.ru
Особенности параканкрозной пневмонии
Параканкрозной (перифокальной) называют пневмонию, которая развивается в тканях легких вокруг злокачественного новообразования – рака (карциномы) легкого.
Рак легких является наиболее распространенным онкологическим заболеванием в мире.
По данным ВОЗ, карцинома легкого занимает лидирующую позицию в структуре заболеваемости населения злокачественными новообразованиями. По данным разных авторов, от 15 до 50% случаев рака легкого осложняется воспалением легочной паренхимы с обязательным вовлечением в патологический процесс альвеол.
Причины возникновения параканкрозной пневмонии
Соотношение мужчин и женщин в структуре заболеваемости раком легких составляет 6:1. Соответственно, частота заболеваемости параканкрозной пневмонией среди мужчин в разы превышает таковую среди женщин.
Параканкрозная пневмония является осложнением карциномы легких. В свою очередь, рак значительно усугубляет течение воспалительного процесса в легких.
Возбудителями параканкрозной пневмонии чаще всего являются пневмококки, реже – клебсиеллы, вирусы, микоплазмы, хламидии, легионеллы. Раковая опухоль угнетает местный иммунитет, поэтому вокруг новообразования создаются условия, благоприятные для развития патогенных и условно-патогенных микроорганизмов.
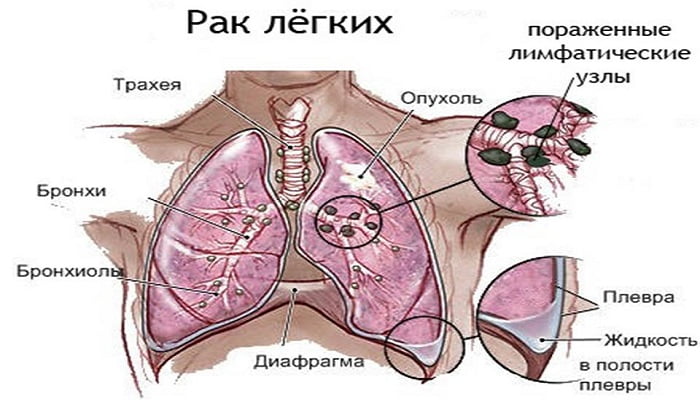
Микроорганизмы в процессе своей жизнедеятельности вырабатывают токсины, которые ухудшают микроциркуляцию в тканях легких, нарушают проводимость нервных импульсов по нервам, регулирующим дренажную функцию бронхов, вызывают некроз легочной ткани. В результате в просвете альвеол скапливается воспалительное содержимое, в котором обнаруживаются слущенный легочный эпителий, микроорганизмы, лейкоциты.
Еще одним из механизмов развития перифокального воспаления легких является механическое закупоривание (обтурация) просвета бронхов распадающейся раковой опухолью или вследствие ее прорастания в их просвет. В результате этого выведение мокроты из легких становится невозможным – в альвеолах скапливается экссудат.
К факторам риска, которые способствуют развитию параканкрозной пневмонии, относятся:
- курение пациента;
 злоупотребление алкоголем;
злоупотребление алкоголем;- работа во вредных условиях труда (на сквозняке, во влажных и прохладных помещениях, с вредными производственными газами);
- аспирация жидкостями (желудочным соком, рвотными массами, кровью);
- заболевания системы крови;
- наличие хронических заболеваний органов дыхания;
- сердечно-сосудистые патологии, протекающие с застоем в малом круге кровообращения.
Эти факторы приводят к закупориванию или уменьшению просвета бронхов, нарушению микроциркуляции в тканях легких, снижению бронхопульмонального и общего иммунитета пациента.
Клиника и диагностика перифокального воспаления легких
Если на момент возникновения пневмонии известно о наличии у больного рака легкого, то диагностика параканкрозной пневмонии не составляет труда. Если же онкологический диагноз пациенту не поставлен, то такую пневмонию очень трудно отличить от других видов воспаления легких.
Основными клиническими проявлениями перифокального воспаления легких являются:
 внезапное повышение температуры;
внезапное повышение температуры;- боль в грудной клетке, усиливающаяся при дыхании;
- одышка;
- кашель;
- выделение гнойной мокроты с прожилками крови;
- интоксикационный синдром (слабость, озноб, тошнота, головные боли, отсутствие аппетита).
При перкуссии над очагом поражения определяется тупой звук, а при аускультации – хрипы, крепитация.
Лабораторные анализы крови выявляют признаки острого воспаления (повышение количества лейкоцитов, сдвиг лейкоформулы влево, повышение СОЭ).
Рентгенологическая картина обнаруживает участок затемнения, что без особой онкологической настороженности врача-рентгенолога может трактоваться как очаг воспаления.
Заподозрить, что у пациента имеет место пневмония на фоне карциномы легких, можно лишь детально узнав его анамнез (историю болезни). На рак легких у больного, особенно у мужчины, старше 40 лет, могут указывать симптомы, появившиеся до начала пневмонии (за несколько месяцев или лет):
 упорный кашель;
упорный кашель;- изменение голоса;
- необъяснимые повышения температуры тела;
- боли в грудной клетке, особенно той же локализации, что и при пневмонии;
- похудание вплоть до истощения;
- кровь в мокроте.
Для параканкрозной пневмонии характерно одновременное появление болей в грудной клетке и повышение температуры. Настораживающим симптомом для перифокального воспаления легких является кровь в мокроте («ржавая» мокрота), которая появилась сразу же при первых признаках пневмонии.
Иногда удается обнаружить раковые клетки при проведении микроскопии мазка мокроты. Раковые клетки в мокроте определяют у 50-80% пациентов с центральной карциномой. При периферическом расположении новообразования вероятность их обнаружения в мокроте уменьшается до 30-50%.
При малейшем подозрении на наличие карциномы легких у пациента с признаками легочного воспаления, требуется проведение дополнительных, более точных диагностических методов. Основными методами диагностики, которые используются для дифференциального диагноза непараканкрозных пневмоний с параканкрозной, являются:
 Рентгенография органов грудной клетки в нескольких проекциях.
Рентгенография органов грудной клетки в нескольких проекциях.- Бронхография.
- Бронхоскопия с биопсией.
- Компьютерная томография.
- Диагностическая торакотомия.
- Пункция плевральной полости.
Одной из главных отличительных особенностей параканкрозного воспаления является отсутствие уменьшения рентгенологических признаков и клинического эффекта на фоне проводимой антибактериальной терапии.
Лечение параканкрозной пневмонии
Лечением параканкрозной пневмонии должны заниматься совместно терапевты (пульмонологи) и онкологи. Тактика лечения перифокального воспаления легких очень отличается от лечения других видов пневмоний. Она включает мероприятия, направленные на лечение собственно злокачественного новообразования, а также на лечение воспаления легких.
Консервативная терапия пневмонии включает:
 антибиотикотерапию;
антибиотикотерапию;- патогенетическое лечение;
- детоксикационное лечение;
- симптоматическую терапию;
- иммуностимулирующее лечение;
- немедикаментозные методы (физиотерапию, ЛФК).
Антибиотикотерапия, несмотря на ее малоэффективность при этом виде пневмонии, назначается с целью ограничения воспалительного процесса. В начале заболевания назначаются антибиотики широкого спектра действия, после получения результатов бактериологического исследования мокроты – антибиотики, к которым чувствительны возбудители пневмонии.
В основе патогенетической терапии лежит назначение препаратов, улучшающих дренажную функцию бронхов и способствующих отхождению мокроты. При необходимости проводят лечебную бронхоскопию.
Детоксикационное лечение направлено на уменьшение признаков интоксикации, которая развивается как вследствие острой пневмонии, так и вследствие отравления организма продуктами жизнедеятельности раковых клеток. Детоксикационная терапия проводится путем массивных инфузий на фоне контролируемого диуреза, то есть совместно с мочегонными препаратами. При необходимости проводятся гемосорбция, плазмаферез и другие аппаратные процедуры.
 При неэффективности консервативной терапии прибегают к хирургическому лечению. В зависимости от размера опухоли, стадии онкологического процесса, его распространенности и наличия метастазов операции могут быть паллиативными (в случаях распада опухоли с отдаленным метастазированием) или радикальными (удаление легкого с опухолью вместе с регионарными лимфоузлами).
При неэффективности консервативной терапии прибегают к хирургическому лечению. В зависимости от размера опухоли, стадии онкологического процесса, его распространенности и наличия метастазов операции могут быть паллиативными (в случаях распада опухоли с отдаленным метастазированием) или радикальными (удаление легкого с опухолью вместе с регионарными лимфоузлами).
Прогнозы при параканкрозной пневмонии неблагоприятны. Появление перифокального воспаления легких является плохим прогностическим признаком рака легкого, поскольку свидетельствует о нарушении жизненно важной функции организма – дыхания.
Прогноз для больного может быть относительно благоприятным лишь при небольших размерах опухоли, отсутствии ее метастазирования и своевременно проведенном лечении онкологической патологии, которая и служит основной причиной возникновения параканкрозной пневмонии.
Источник: opnevmonii.ru
Рак легкого (работа 2)
Московский Государственный Медико-стоматологический Университет
Реферат на тему: РАК ЛЕГКОГО
Студент 6 курса, 9 группы вечернего-лечебного факультета
Рак несколько чаще развивается в правом легком (51,4%) и реже—в левом (48,6%). Чаще поражаются верхние доли (60%).
Макроскопически по типу роста опухоли выделяют экзофитные (эндобронхиальные), когда опухоль растет в просвет бронха, и эндофитные (экзобронхиальные), когда опухоль растет в сторону легочной паренхимы. Имеются также промежуточные формы роста.
Микроскопическое строение рака легкого. Рак развивается из метаплазированного эпителия бронхов и бронхиальных желез. Патологически различают:
— плоско клеточный ороговевающий и неороговевающий рак—наиболее часто встречающиеся формы (60%);
— недифференцированный рак—крупно-, мелко-, овсянокле-точный рак, развивающийся (в 30%) чаще у молодых, рано и широко метастазирующий;
— аденокарциному (в 10% случаев), состоящую из дифференцированных, медленно растущих клеток, и недифференцированную аденокарциному, с быстрым ростом, рано и широко метастазирующую.
Анатомические особенности строения легких, богато представленные лимфатические сосуды создают благоприятные анатомические условия для разнообразного, обильного и раннего метастазирования злокачественной опухоли. Метастазирование рака легкого происходит лимфогенным и гематогенным путем. Различают три лимфатических барьера на пути оттока лимфы из легкого: пульмональные лимфатические узлы, расположенные в толще легкого по ходу бронхов и сосудов; бронхопульмональные и трахеобронхиальные (правые и левые трахеобронхиальные и бифуркационные) лимфатические узлы. Может прослеживаться определенная региональность в лимфооттоке от долей легкого, однако при блокировке вышележащих лимфатических узлов опухолевым процессом ток лимфы часто идет ретроградно. Поэтому при операциях часто приходится удалять все три лимфатических барьера как регионарные зоны метастазирования.
Отдаленные метастазы наблюдаются в шейных, надключичных и парааортальных лимфатических узлах. В более поздних случаях—в печени, костях, головном мозге и др. органах.
Знание характера роста опухоли, гистологического строения и возможных путей метастазирования необходимо врачу, чтобы понять особенности клинической картины рака легкого, уметь поста вить диагноз.
Классификация рака легкого. Отечественная классификация
I стадия. Небольшая ограниченная опухоль крупного бронха эндо- или перибронхиальной формы роста, а также опухоль мелких и мельчайших бронхов без прорастания плевры и без призна-ков метастазирования.
II стадия. Такая же опухоль или больших размеров, но без прорастания плевральных листков, при наличии одиночных метаста-зов в ближайших лимфатических регионарных узлах.
III стадия. Опухоль, вышедшая за пределы легкого, врастает в один из соседних органов, перикард, средостение, грудную стенку, диафрагму при наличии множественных метастазов в регионар-ных лимфатических узлах.
IV стадия. Опухоль легких с обширным распространением на соседние органы, с обширными метастазами, отдаленными мета-стазами.
Классификация рака легкого по системе TNM
ТО — первичная опухоль не определяется.
ТХ— наличие опухоли доказано присутствием раковых клеток в мокроте, секрете. При рентгенологическом или эндоскопическом исследовании опухоль не определяется.
Tl— опухоль размером 3 см и менее по большому диаметру не прорастающая долевой бронх (при бронхоскопии).
Т2—опухоль более 3 см по наибольшему диаметру или опухоль любого размера с ателектазом или обструктивным пневмонитом, распространяющимся на корневую зону. При бронхоскопии распространение видимой опухоли должно быть как минимум на 2 см дистальнее карины. Сопутствующий ателектаз или обструк-тивный пневмонит вовлекает менее целого легкого без плевраль-ного выпота.
ТЗ—опухоль любого размера, распространяющаяся на сосед- л ние структуры (средостение, грудная клетка, диафрагма) или опухоль при бронхоскопии менее чем на 2 см дистальнее карины, или опухоль сочетается с ателектазом или обструктивным пневмони-том целого легкого или плевральным выпотом.
N—регионарные лимфатические узлы.
N0—нет метастазов в регионарных лимфатических узлах. N1—метастазы в лимфатические узлы корня легкого стороны поражения, включая прямое распространение первичной опухоли.
N2—метастазы в лимфатические узлы средостения.
МО—нет отдаленных метастазов.
Ml— отдаленные метастазы, включая лимфатические узлы предлестничные, шейные, подключичные, противоположного корня легкого и метастазы в другие органы.
Клиника рака легкого
Клиническая картина рака легкого весьма разнообразна и зависит от локализации, стадии заболевания, анатомического типа роста опухоли, гистологического строения и предшествующих раку заболеваний легкого.
Клинико-анатомическая классификация рака легкого по А. И. Савицкому:
Центральный рак (эндобронхиальный, перибронхиальный, разветвленный) наиболее часто встречающаяся форма, развивается из эпителия главного, долевых, сегментарных и субсегментарных бронхов.
Периферический рак (шаровидный, пневмониеподобный, рак верхушки легкого (Пенкоста), развивается из альвеолярного эпителия или эпителия мелких бронхов.
Атипические формы (в зависимости от особенностей метастазирования—медиастинальная, карциноматоз легкого, костная, мозговая, печеночная и др.).
Одним из основных и наиболее ранним симптомом центрального рака легкого является кашель, вначале сухой, в последующем — надсадный, особенно по ночам, сопровождающийся выделением мокроты с примесью крови в виде прожилок, что является признаком распада опухоли. Далее появляются боли в грудной клетке, чаще всего обусловленные прорастанием опухолью плевры или в связи с ателектазом и неспецифическим плевритом.
По мере роста опухоли происходит сужение просвета бронха и нарушение вентиляции соответствующей доли или сегмента легкого. Вначале развивается гиповентиляция, затем ателектаз и соответствующий пневмонит. Последний характеризуется внезапным подъемом температуры тела, усилением кашля. В клинической картине могут превалировать такие общие симптомы, как недомогание, немотивированная слабость, быстрая утомляемость, снижение трудоспособности, похудание, субфебрильная температура. Иногда отмечается гипертрофическая легочная остеоартропатия— синдром Мари-Бамбергера, заключающийся в гипертрофии, обызвествлении и окостенении надкостницы мелких трубчатых костей, предплечья, голени. Клинически он проявляется в утолщении кончиков пальцев кистей, принимающих форму «барабанных палочек», боли в конечностях особенно в суставах. Однако этот синдром не носит специфического характера и может встречаться в случаях различных обменных нарушений (нередко при хронических болезнях легких и сердца).
В противоположность центральному раку, клиническая картина переферического рака относительна бедна. Развиваясь в периферической зоне легкого, вдали от крупных бронхов, не вызывая заметной реакции легочной ткани, опухоль долгое время (в отдельных случаях по нескольку лет) не имеет каких-либо клинических симптомов и обнаруживается случайно при рентгенологическом исследовании. Первым клиническим симптомом является боль в груди на стороне поражения, появляющаяся при прорастании опухолью плевры, одышка и степень ее выраженности зависят от величины и положения опухоли. При прорастании опухоли в бронхи появляется кашель и кровохарканье. Периферический рак чаще сопровождается диссеминацией опухоли по плевре и образованием плеврального экссудата. Пневмониеподобная форма периферического рака легкого протекает с симптомами, во многом напоминающими пневмонию.
Рак верхушки легкого (опухоль Пенкоста) благодаря преимущественному распространению опухолевого инфильтрата через купол плевры на задние отрезки 1—11 ребер, иногда дужки нижних шейных позвонков и на ствол симпатического нерва приводит к своеобразной клинической симптоматике, в которой превалируют боли в области плечевого сустава, плеча и синдром Горнера.
Клиническая картина атипических форм рака легкого обусловлена метастазами, а первичный очаг в легком доступными диагностическими методами выявить не удается. Медиастинальная форма рака легкого выделяется в связи с особенностями, обусловленными преимущественным ростом метастатических опухолевых узлов в средостении. Она характеризуется выраженным компрессионным синдромом, степень которого зависит от локализации и размера соответствующих групп лимфатических узлов. При поражении лимфатических узлов, расположенных вокруг верхней полой вены, безымянной и непарной вен превалируют симптомы сдавления (одутловатость лица, шеи, одышка, цианоз, расширение подкожной венозной сети на грудной стенке).
Преимущественно левостороннее расположение опухолевых узлов в средостении обусловливает компрессионный парез возвратной ветви блуждающего нерва с клиникой охриплости голоса вплоть до развития афонии. При поражении задней группы медиастинальных лимфатических узлов возможны симптомы сдавления симпатического нерва (болевой синдром) и сдавление пищевода (дисфагия).
Атипический первичный карциноз легких характеризуется множественными очаговыми метастазами в легких, на фоне которых первичный очаг обычно не выявляется. Клинически это проявляется одышкой вследствие поражения большой дыхательной поверхности легких.
Симптомы рака легкого, связанные с прорастанием опухолью анатомических образований, а также регионарным и отдаленным метастазированием, отличаются большим разнообразием.
Диагностика рака легкого трудна на всех стадиях развития опухоли. В раннем периоде симптомов нет, в поздних стадиях имеются большие затруднения в дифференциальной диагностике. Выявление ранних стадий шаровидной формы периферического рака легкого возможно при профилактической флюорографии. В других случаях возможность ранней диагностики связана с определенной формой диспансерного наблюдения. Эта работа требует участия высококвалифицированных специалистов, а детальное уточняющее обследование больных может быть осуществлено в выскоспециализированных бронхо-торакальных диагностических отделениях. Прежде всего организуются пульмонологические консультативные (онкологические) комиссии из компетентных специалистов (статистики, онкоэпидемиологи, цитологи, пульмонологи, хирурги, рентгенологи и др.) по формированию групп онкориска. Последние организуются с использованием опросно-анкетного метода. Факторами риска при раке легких следует считать: возраст старше 45 лет у мужчин и 50 лет у женщин, профессиональные вредности (газо-нефтехимическая промышленность, шахтеры, асфальтировщики, работники производства цемента, асбеста, хрома и т. д.), курение табака, хронические воспалительные заболевания легких и др. Лицам из группы повышенного риска необходимо не менее 2 раз в год производить общий анализ мокроты с микроскопическим исследованием для определения клеточного состава с признаками атипии (цитологический скрининг). Как показывает практический опыт ведущих лечебных учреждений нашей страны, у 3—15% взятых на учет в группу риска диагностируется IV степень атипии клеток. Для этих лиц требуется дополнительное уточняющее обследование в специализированных диагностических бронхо-торакальных отделениях.
В более поздних стадиях первичная диагностика осуществляется на основе сбора анамнеза, физикального, лабораторного, рентгенологического и эндоскопического исследований. Особое внимание следует обращать на больных, страдающих длительным кашлем, кровохарканием и периодическим повышением температуры. При физикальном исследовании необходимо отмечать наличие ограничения подвижности грудной клетки, зоны укорочения легочного звука и ослабления дыхания. Во всех случаях для подтверждения диагноза важно многократное исследование мокроты на атипические и опухолевые клетки. Основной метод распознавания рака легкого—рентгенологический. При периферическом раке на рентгенограммах выявляют округлую плотную тень опухоли с довольно четкими бугристыми контурами. При наличии сопутствующих воспалительных процессов в легких диагностика затруднена. Для центрального рака характерны симптомы гиповентиляции или ателектаза всего легкого, доли или сегмента. Однако чаще всего—это манифестация далеко зашедшего процесса, не подлежащего радикальному оперативному вмешательству
Диагностика более ранних форм заболевания оказывается затрудненной. В этих случаях клинико-ренгенологической симптоматики рака легкого со специфическими и неспецифическими воспалительными процессами требуется особая онкологическая настороженность врача общего профиля. Полагаясь на данные рентгеноскопии и рентгенографии в одной проекции, находясь под впечатлением рентгенологического диагноза, клиницист не всегда правильно проводит клинико-рентгенологические параллели, не настаивает на более полном пульмонологическом обследовании больного, включающем тщательное томографическое исследование легкого, бронхиального дерева и средостения. Томограммы позволяют получить более четкие очертания первичного очага при периферическом раке легкого, особенно, при выраженной параканкрозной воспалительной реакции, «закрывающей» первичную опухоль. При центральном раке легкого томография выявляет нечеткость, деформацию и узурацию стенок бронха, сужение просвета бронхов, наличие увеличенных лимфатических узлов в области корней и средостения. Чрезвычайно информативным методом исследования является компьютерная томография.
Обследование заканчивается эндоскопическим исследованием с биопсией опухоли или при периферическом раке катетеризацией мелких бронхов, со взятием материала для цитологического исследования. При необходимости в специальном диагностическом бронхо-торакальном отделении проводится чрезбронхиальная пункция первичного очага и увеличенных лимфатических узлов или трансторакальная пункция субплеврально расположенной опухоли. У ряда больных окончательный диагноз может быть установлен только при диагностической торакотомии.
Для уточняющей диагностики и выявления степени распространенности процесса используются рентгенологические исследования в условиях наложенного пневмоторакса, пневмомедиастинотомография, бронхография. Дополнительные данные можно получить, применяя ангиографию, в том числе азигографию. Применяется также парастернальная медиастинотомия, биопсия увеличенных периферических узлов, медиастиноскопия с биопсией, фибробронхоскопия с чрезтрахеальной и чрезбронхиальной пункцией лимфатических узлов, цитологическое исследование плевральной жидкости, лапароскопия и лапаротомия.
Внедрение специальных методов определения степени распространения опухолевого процесса способствует повышению операбельности и резектабельности, снижению числа пробных торакотомии, увеличению числа радикальных операций, улучшению планирования рациональной консервативной терапии и улучшению результатов лечения.
ПРИНЦИПЫ ЛЕЧЕНИЯ РАКА ЛЕГКОГО
В настоящее время при лечении рака легкого применяют хирургический, лучевой и химиотерпевтический методы лечения или сочетания их в различной комбинации. Выбор метода лечения зависит отлокализации, клинико-анатомических форм опухоли, стадии ее гистологической структуры и степени дифференцировки клеток, функциональных возможностей больного, особенно функции дыхания и сердечно-сосудистой системы. Хирургическое лечение оказывается эффективным в I, II и в некоторых случаях III стадии при плоскоклеточном раке легкого и аденокарциноме. При недифференцированном раке легкого предпочтение должно быть отдано лучевому и лекарственному лечению. Среди операций различают типовые (лобэктомия, билобэктомия, пневмонэктомия) и комбинированные операции, которые сопровождаются резекцией соседнего анатомического образования (части диафрагмы, грудной стенки, перикарда).
Если локализация центрального рака легкого позволяет отсечь долевой бронх, отступив не менее 2 см от края опухоли, при отсутствии метастазов в прикорневых и трахеобронхиальных лимфатических узлах, то показана лобэктомия. Большие возможности для этого имеются при периферическом раке. Во всех остальных случаях показана пневмонэктомия с удалением бифуркационных, трахеобронхиальных лимфатических узлов с жировой клетчаткой на стороне поражения.
При малодифференцированных формах рака показана пневмонэктомия из-за частого и более широкого метастазирования в регионарные лимфатические узлы.
Более подробно по вопросам хирургического лечения рака легкого см.: Б. Е. Петерсон, «Хирургическое лечение злокачественных опухолей». Медицина, 1976, 222—237).
В последние годы более перспективным является комбинированный метод, включающий предоперационную лучевую терапию и радикальную операцию. Предоперационная лучевая терапия направлена на снижение биологической активности опухоли, уменьшение ее размеров, уничтожение субклинических метастазов в регионарных лимфатических узлах. В результате достигается снижение частоты рецидивов и метастазирования. Облучение обычно проводится с использованием современных гамма-аппаратов и ускорителей легких частиц с энергией 15—25 МэВ средними фракциями по 5 Гр ежедневно в течение 5 дней до суммарной очаговой дозы 25 Гр, а оперативное вмешательство производится спустя 2—4 дня после окончания лучевой терапии. В тех случаях, когда имеются сомнения в радикальности операции, прибегают к послеоперационной лучевой терапии, которую начинают обычно через 3—4 недели после операции с подведением суммарной очаговой дозы до 30—40 Гр при ежедневной дозе 2 Гр.
Лучевая терапия как самостоятельный метод может быть проведена по радикальной или паллиативной программе. Основным показанием к проведению лучевой терапии по радикальной программе является отностительно небольшая опухоль, при удовлетворительном состоянии больных (1—2 стадия заболевания), отказавшихся от операции, либо не подлежащих оперативному вмешательству, вследствие общих противопоказаний. Обычно облучение осуществляется через фигурные поля с захватом в зону облучения первичной опухоли, а также прикорневых, паратрахеальных и бифуркационных лимфатических узлов. Области ателектатически измененного легкого не включаются в зону облучения. При недифференцированных формах рака в зону облучения включаются надключичные области, все средостение, область противоположного корня. Недельная доза составляет 10 Гр. Суммарная очаговая доза составляет 60—70 Гр.
Паллиативная лучевая терапия проводится больным в III и IV стадиях, когда уже имеется метастатическое поражение всех групп регионарных лимфатических узлов или распространение опухоли на ребра и плевру, вовлечение в процесс магистральных сосудов, при наличиии одиночных метастазов в надключичной области. Суммарная очаговая доза составляет 45—50 Гр.
Широкое применение получила методика лучевой терапии расщепленным курсом. После подведения суммарной очаговой дозы 30 Гр делается перерыв на 3 недели, после чего к очагу подводится еще 40 Гр. Этот метод отличается лучшей переносимостью паллиативного лечения без снижения эффективности лучевого лечения. Противопоказаниями к лучевой терапии служит глубокая старость, кахексия, сопутствующие активные формы туберкулеза легких, распад опухоли, кровотечения, наличие отдаленных метастазов и др.
О более подробном изложении вопросов лучевой терапии и комбинированного лечения рака легких читайте в книге А. В. Козлова «Лучевая терапия злокачественных опухолей», М., «Медицина», 1976 г., стр. 112—118.
За последнее время в клинике и амбулаторно при раке легкого все более широкое применение находят противоопухолевые химиотерапевтические препараты.
Возможности химиотерапии рака легкого определяются в первую очередь гистологическим типом опухоли. В связи с этим особо выделяется у много курящих мужчин 40—45 лет мелкоклеточный анапластический рак легкого, отличающийся крайней злокачественностью течения, склонностью к ранней генерализации процесса и в то же время высокой чувствительностью к химиотерапевтическим (и лучевым) воздействиям. Остальные гистологические типы—плоскоклеточный (эпидермоидный), крупноклеточный и аденокарцинома отличаются малой чувствительностью к химиотерапевтическим воздействиям.
При лечении мелкоклеточного рака легкого применяются следующие схемы полихимиотерапии (комбинированной химиотерапии) : циклофосфан, адриамицин, метотрексат; циклофосфан, адриамицин, винкристин; адриамицин, циклофосфан, этапозид и др. За последнее время получены данные, свидетельствующие о том, лечебный эффект, снижает число местных рецидивов.
Полихимиотерапия немелкоклеточного рака малоэффективна.
Несколько большая чувствительность наблюдается при малодифференцированных формах рака.
Применение цитостатических средств приносит определенную пользу при экссудативных плевритах, осложняющих течение рака легкого. Повторные внутриплевральные введения тиофосфамида в разовых дозах 30—40 мг после максимальной эвакуации содержимого плевральной полости в 60—70% случаев приводят к облитерации плевральной полости и прекращению накопления экссудата у больных с различными гистологическими формами рака легкого. Сходный эффект дает внутриплевральное введение циклофосфана или блеомицина.
Для более детального ознакомления с темой химиотерапии рака легкого см.
— Блохин Н. Н., Переводчикова Н. И., «Химиотерапия опухолевых заболеваний», М., «Медицина», 1984 г., 163—180.
— Переводчикова Н. И. «Противоопухолевая химиотерапия» М., «Медицина», 1986 г., 44—48.
РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ И ФАКТОРЫ ПРОГНОЗА
С помощью хирургического метода лечения удается добиться 5-летней выживаемости лишь у 25—40% оперированных больных. Малоудовлетворительные результаты хирургического лечения чаще всего связаны с нерадикальностью операции. На длительность жизни больного оказывает влияние степень распространенности процесса, морфологическое строение опухоли легкого и степень дифференцировки.
Так, при I стадии более 5 лет живут 48,5%, при II стадии— 41,3% и при III стадии—18,4%. При наличии плоскоклеточного рака легкого более 5 лет живут 34% больных, железистого— 33,3%. При недифференцированном раке выживаемость составила всего 7,7%.
Лучевая терапия позволяет улучшить состояние больных, продлить их жизнь. Средняя продолжительность жизни больных после лучевого лечения составляет 16,7—18,9 месяца, достигая 2—3 лет, а иногда 5 лет (10%).
Комбинированная химиотерапия при мелкоклеточном раке легкого позволяет получить выраженный непосредственный эффект у 75% больных, причем у 25—45% достигается полное изчезновение всех клинических признаков заболевания. Средняя продолжительность жизни составляет 8—13 месяцев. Только больные, у которых удается получить полную клиническую ремиссию, имеют реальные шансы на удлинение жизни до 2 и более лет.
Улучшение результатов лечения этого тяжелого заболевания связывается с улучшением современной диагностики, путем активного выявления рака легкого среди населения группы «риска»,
Источник: topref.ru
Онкология легких (монография, главы 1-5)
ОГЛАВЛЕНИЕ
Аннотация
В монографии дается представление о широком спектре онкологических заболеваний легкого и наиболее надежных методиках подтверждения диагноза. Книга создана при поддержке специалистов Московской онкологической больницы № 62 и Российского Научного Центра Рентгенорадиологии. Опыт автора составил 5772 наблюдения первичных заболеваний легких, в том числе 3233 (56%) онкологических и опухолевидных поражений. Значителен опыт учреждений в дифференциальной диагностике необычных процессов в легочной ткани и редких новообразований (карциноиды, опухоли бронхиальных желез, неэпителиальные опухоли, мезотелиомы и др.) — 876 наблюдений.
В 1-й главе рассматриваются основные критерии гистологических классификаций и общие принципы морфологической диагностики. Проведен критический анализ проблем цитологической классификации, клинического и прогностического значения гетерогенности злокачественных новообразований легкого. Наглядна сравнительная таблица гистогенетической и ВОЗовской классификаций.
Во 2-й главе достаточно подробно разбирается опухоли из бронхиального эпителия, их гистогенетические источники, клеточный состав эпителиальной выстилки бронхов, Представлены современные данные о доброкачественных эпителиальных образованиях, гиперплазии, метаплазии, атипии, carcinoma in situ. Рассмотрены клеточные критерии различных фаз развития рака легкого, их гистологические характеристики, клинико-морфологические параллели. Особое внимание уделено ультраструктурной и иммуногистохимической дифференциальной диагностике мелкоклеточного рака, выделены особенности бронхиолоальвеолярного, лимфоэпителиоидного рака.
В 3-й главе описаны основные опухоли, возникающие из бронхиальных желез. Достаточно большое внимание уделено цистаденоме, ацинозноклеточной опухоли, онкоцитарной аденоме и опухоли Уортина. Перечислены основные принципы дифференциальной диагностики этой редкой патологии.
В отдельную небольшую 4-ю главу выделена информация о карциноидах. Подчеркивается их гетерогенность и необходимость выделения атипичных форм. На эти необычные опухоли обращается наиболее пристальное внимание. Дано и более подробное их описание, как на светооптическом, так и на ультраструктурном уровне. Конкретизированы и особенности биохимической патологии.
5-я глава посвящена мезотелиомам плевры. Большое практическое значение имеет классификация диффузного поражения по стадиям. Подчеркивается значение тканевых онкомаркеров в иммуногистохимической дифференциальной диагностике первичных поражений плевры.
Не эпителиальные опухоли рассмотрены в 6-й главе. Приведены структурные особенности относительно редких поражений соединительной и жировой ткани, хряща, миогенных элементов, сосудистых новообразований. Описана саркома Капоши и саркомы легочных сосудов, опухоли нейроэпидермального происхождения. Отдельный раздел посвящен необычным опухолям (зернистоклеточная миобластома, меланома, карциносаркома, бластома, опухоль Уортина, опухоль Аскина).
В 7-й главе описаны лимфопролиферативные поражения легкого (лимфомы, псевдолимфомы, плазмоцитома, гистиоцитоз Х, лимфоидный гранулематоз и др.). Метод лечения этих новообразований основывается на надежной ранней диагностике злокачественных лимфом, точной иммуногистохимической классификации гистологических вариантов и использовании современных цитостатиков и модификаторов биологической чувствительности опухоли.
В 8-й главе описаны необычные дизэмбриогенетические образования и опухолевидные процессы, включая эндометриоз, остеохондропластическую трахеобронхопатия, первичную хорионкарцинома, склерозирующую гемангиому, плазмоклеточные гранулемы. В заключении авторы предостерегают от ошибок в диагностике в связи с недостаточной информированностью с разнообразной онкологической патологией легкого. Стандартные классификации должны служить только основой для творческого подхода к использованию дополнительных методов типирования тканей.
Список литературы содержит 63 отечественных источника и 310 иноязычных. Книга предназначена для патологоанатомов, пульмонологов, онкологов, фтизиатров и хирургов.
Предисловие
Гистологическая классификация ВОЗ онкологических заболеваний легких принята во всем мире, однако в атрибуции крайне гетерогенных новообразований далеко еще не изжит значительный субъективизм. Многие относительно редкие подтипы рака легкого (мезотелиомы, неэпителиальных поражений, лимфом, гамартом) пока еще остаются мало известными морфологам, хирургам и онкологам. Сведения об этой патологии разбросаны по многочисленным периодическим изданиям. Обобщающей монографии по нетипичной онкоморфологии в нашей стране нет. Успехи электронной микроскопии, иммуноморфологии, появление целого раздела науки о тканевых маркерах требуют дополнительного рассмотрения и широких обобщений.
За рубежом широко известна капитальная монография в двух томах: H.Spencer «Patology of the Lung». Она выдержала уже 4 издания (последнее в 1985 г.). Онкологии посвящен целиком второй том. Российским специалистам эта книга малодоступна, особенно в современных условиях. Да и морфологические технологии за последние годы существенно продвинулись вперед.
Монография «Oнкоморфология легких» посвящена исключительно актуальной проблеме дифференциальной диагностики злокачественных новообразований легкого и многогранной группе псевдоопухолевых очаговых и диффузных поражений дыхательных путей на всех уровнях ниже бифуркации трахеи. Обобщены разрозненные данные литературы и представлен собственный опыт редких и казуистических наблюдений онкологической и пограничной патологии. Рассмотрены различные аспекты таких поражений с кратким анализом заболеваемости, особенностей симптоматики, факторов прогноза и оптимальных методов лечения. Энциклопедичность содержания и построение по типу справочника сделают монографию хорошим помощником врача любой специальности, особенно патоморфолога, онколога и хирурга.
Глава 1. Основные критерии гистологической классифкации новообразований легкого
Форма роста рака легкого, склонность к метастазированию, скорость распространения на соседние ткани и другие биологические особенности опухоли в значительной мере коррелируют с ее гистологической структурой. От прочих онкологических поражений рак легкого отличается чрезвычайным разнообразием гистологических вариантов. Даже в опухолях с относительно однотипной микроскопической картиной в первичном очаге и метастазах встречаются участки, представленные иным типом клеток , иной гистоархитектоникой. Обычно удается определить преобладающий тип клеток и структур опухоли, достоверно свидетельствующих о гистогенезе. Значительные успехи в этом направлении связаны с широким внедрением электронной микроскопии и иммуноморфологических методов исследования в биопсийную практику. Тем не менее в ряде случаев не удается точно определить гистогенетическую принадлежность опухоли, что связано с субъективным фактором в выборе критериев диагностики и квалификацией патологоанатомов.
В современных онкологических учреждениях, а тем более в научно-исследовательских институтах, морфологам для достижения этой цели приходится проявлять не только принципиальность и тщательность при последовательном изучении биопсийных и операционных препаратов, но и подробно описывать происходящие в опухоли процессы, фоновые изменения, связанные с возникновением и ростом злокачественных клеток, а также оценивать гистогенетическую сущность заболевания в соответствии с постоянно меняющимися взглядами и установками. Важную роль в этом плане играет также биологическая индивидуальность опухоли и организма (анамнез, клиническая картина, особенности примененных методов получения биопсийного и операционного материала).
Исторически в основу многочисленных гистологических классификаций положены общеонкологические принципы: направление дифференцировки клеток (эпидермоидная, железистоподобная) и особенности гистоархитектоники опухоли. Отсутствие характерного рисунка строения и высокая частота митозов указывают на склонность опухоли к быстрому и агрессивному росту, высокую вероятность раннего метастазирования.
Различают три основных типа рака легкого: плоскоклеточный, железистый и недифференцированный, в частности, анапластический рак. В 1962 году L.Watson и J.W.Berg выделили особо злокачественную форму недифференцированного рака — мелкоклеточный, включающий три подтипа: овсяноклеточный рак, рак из клеток промежуточного типа, комбинированный овсяноклеточный рак. Мелкоклеточный рак отличается бурным ростом, ранним и обширным метастазированием. Средняя продолжительность жизни больных мелкоклеточным раком легкого не превышает 4 месяцев. В связи с этим в 80-х годах в работах, посвященных раку легкого, было принято делить его на два принципиально различных гистологических типа: мелкоклеточный и немелкоклеточный. Этот принцип положен в основу классификации, используется при планировании последовательности применяемых методов диагностики и лечения, а также оценке их отдаленных результатов.
Первые попытки создания морфологической классификации рака легкого предприняты еще в Х1Х веке. А.Альфонский (1852) макроскопически различал медуллярную и коллоидную формы. Основы гистологической классификации заложил в 1867 г. N.Waldeyer, а в России — ГВ.Шор (1903). С самого начала за рубежом наибольшую известность приобрели наиболее полные и удобные систематизации микроскопической картины, предложенные А.Маrсhesani в 1924 году, а затем Л.Крейбергом (1967). Они послужили фундаментом современных классификаций ВОЗ (1981) с усовершенствованиями, внесенными морфологическим комитетом Группы по изучению рака легкого Национального онкологического института США (C.F.Мountain, 1987).
Предложенные морфологические критерии позволяют максимально преодолеть субъективный фактор при определении типа и подтипа опухоли, свести к минимуму количество ошибок в оценке биопсийного материала. Гистологическая номенклатура включает также определение степени дифференцировки, то есть зрелости клеток и упорядоченности основных структур опухоли. Степень дифференцировки в пределах одного подтипа определяют для систематизации данных о лекарственной чувствительности, для планирования последующего наблюдения и прогнозирования рецидивов.
По современным представлениям, к злокачественным новообразованиям бронхо-легочной системы стали относить также опухоли из нейроэндокринных клеток и элементов бронхиальных желез. До 1980-х годов их выделяли в особую группу и называли аденомами. Встречались эти опухоли редко, а их диагностика и лечение существенной проблемы не составляли.
Считалось, что эти «доброкачественные» образования развиваются чрезвычайно медленно, но возможны локальный инфильтрирующий рост и даже метастазирование. Впоследствии, установка на доброкачественность вошла в противоречие с клиническим опытом. Термин «аденома» не способствовал настороженности клиницистов и вызывал затруднения при выборе объема радикального лечения. За последние годы в изучении гистогенеза этих новообразований достигнуты значительные успехи благодаря широкому использованию электронной микроскопии и иммуноморфологических методов.
В итоге, в современной гистологической классификации бывшие «аденомы» справедливо относят к злокачественным эпителиальным опухолям, но выделяют в особую группу поражений с относительно низкой степенью злокачественности и более благоприятным прогнозом по сравнению с классическими формами рака. Карциноидные опухоли в соответствии с особенностями гистогенеза и клинического течения в современных классификациях составляют отдельную группу, а цилиндрому и мукоэпидермоидную опухоль, в связи с их большей злокачественностью по сравнению с другими новообразованиями бронхиальных желез, стали называть аденокистозным и мукоэпидермоидным раком.
Однако термин «аденома» не исчез из лексикона пульмонологов. Им стали обозначать истинно доброкачественные эпителиальные опухоли бронхов с характерной гистологической структурой — мономорфную и полиморфную (смешанная опухоль) аденомы. Эти изменения в номенклатуре имеют принципиальный характер, и не следует путать часто встречающиеся в литературе 60 70-х годов понятия «аденома карциноидного типа», «цилиндрома» с действительно доброкачественными аденомами, включенными в последнее издание гистологической классификации опухолей легких ВОЗ.
1.1. ОБЩИЕ ПРИНЦИПЫ ГИСТОЛОГИЧЕСКОЙ ДИАГНОСТИКИ И ОНКОПУЛЬМОНОЛОГИЧЕСКАЯ НОМЕНКЛАТУРА
Первая попытка классификации рака легкого относится к 1924 г., когда А.Маrchesani разделил злокачественные эпителиальные опухоли легкого на 4 основные группы: плоскоклеточный рак, аденокарцинома, мелкоклеточный недифференцированный рак, крупноклеточный недифференцированный рак. В дальнейшем это было использовано в гистологической классификации ВОЗ (первое издание, 1967), где приведена расширенная трактовка 4 основных типов рака легкого с выделением большого количества вариантов, различать которые в практической работе оказалось весьма затруднительно.
Особые трудности возникли с применением этой классификации при оценке материалов, получаемых при различных диагностических процедурах (бронхобиопсии, игловой биопсии и т.д.). Исходя из этих фактов, в последней гистологической классификации опухолей легких (ВОЗ, второе издание, 1981) предпринята попытка адаптировать ее в большей степени для нужд практической диагностики.
Гистологическая классификация опухолей лекгих (ВОЗ,1981):
Эпителиальные опухоли
- Доброкачественные
- Папиллома
- плоскоклеточная папиллома
- «переходноклеточная» папиллома
- Аденома
- Плеоморфная аденома («смешанная» опухоль)
- Мономорфная аденома
- Другие типы
- Папиллома
- Дисплазия
- Pak in situ
- ЗЛОКАЧЕСТВЕННЫЕ
- Плоскоклеточный (эпидермоидный) рак
- веретеноклеточный (плоскоклеточный) рак
- Мелкоклеточный рак
- овсяноклеточный рак
- рак из клеток промежуточного типа
- комбинированный овсяноклеточный рак
- Аденокарцинома
- ацинарная аденокарцинома
- папиллярная аденокарцинома
- бронхиолоальвеолярный рак
- солидный рак с образованием слизи
- Крупноклеточный рак
- гигантоклеточный рак
- светлоклеточный рак
- Железисто-плоскоклеточный рак
- Карциноидная опухоль
- Рак бронхиальных желез
- аденокистозный рак
- мукоэпидермоидный рак
- другие типы
- Другие опухоли
- Плоскоклеточный (эпидермоидный) рак
В данной классификации представлено меньшее количество вариантов недифференцированного рака легкого, а варианты дифференцированных типов выделены с учетом сходства их клинического течения и прогноза. Следует отметить, что если определение принадлежности опухоли к одной из 4 основных групп при выраженности главных присущих каждой из них признаков не представляет трудности, то при оценке вариантов строения и степени дифференцировки возможны существенные разногласия.
R. Yesner и соавт. (1982), изучая эффективность распознавания подгрупп главных типов рака легкого, выяснили, что мнение трех гистологов, исследовавших один и тот же материал, сошлись лишь в 38% случаев. Однако, выделение основных типов и их вариантов в известной степени соответствует клиническому течению, а также чувствительности к специфической терапии. Поэтому диагностика в соответствии с классификацией имеет важное значение для клинической практики. Например, при одних и тех же условиях (наличие метастазов в лимфатических узлах) плоскоклеточный ороговевающий рак имеет отчетливо лучший прогноз после радикального лечения, чем аденокарцинома или крупноклеточный рак.
С другой стороны, следует признать, что на практике при оценке типа, варианта строения и дифференцировки опухоли в случае, когда морфолог располагает только гистологическим методом исследования, нередко приходится сталкиваться со значительными трудностями. Так, общепринято при определении степени дифференцировки плоскоклеточного рака пользоваться следующими критериями: выраженность процессов ороговения в опухоли, наличие межклеточных мостиков, а также наличие стратификации. Характеристика степеней дифференцировки плоскоклеточного рака легкого и в последней гистологической классификации опухолей легких (ВОЗ,1981) изложена нечетко.
В связи с этим, D. Lamb (1984) рекомендует следующие количественные критерии для определения степени дифференцировки плоскоклеточного рака легкого, основанные на выраженности процессов ороговения. Высокодифференцированный рак — выраженная кератинизация (свыше 50% участков опухоли),умеренно дифференцированный рак — менее выраженное ороговение (не более 1/3 участков опухоли), низкодифференцированный рак — только единичные роговые жемчужины или единичные клетки с ороговением, или различимые клеточные мостики. Однако, это не согласуется с общепринятыми принципами классификации опухолей других органов, согласно которым тип новообразования должен кодироваться по наиболее дифференцированному участку с указанием определения, характеризующего степень дифференцировки наименее зрелых участков.
Выделение веретеноклеточного (плоскоклеточного) рака в последнем издании гистологической классификации опухолей легких (ВОЗ, 1981) имеет большое практическое значение, так как этот вариант имитирует злокачественные неэпителиальные опухоли. Задача облегчается в тех случаях, когда веретеноклеточный компонент соседствует с полигональноклеточным, типичным для плоскоклеточного рака. Сходное строение имеет и карциносаркома, поэтому уточнение диагноза в каждом случае с помощью дополнительных методов исследования (гистохимия, электронная микроскопия) может иметь существенное значение.
Группа мелкоклеточного рака представлена в гистологической классификации опухолей легких (ВОЗ, 1981) тремя вариантами: овсяноклеточным раком, раком из клеток промежуточного типа и комбинированным овсяноклеточным раком. Выделение этих вариантов мелкоклеточного рака важно для клинической практики при определении прогноза. Известно, что выживаемость, даже без лечения, выше при классической форме мелкоклеточного рака — овсяноклеточном раке.
Особые трудности при распознавании вариантов мелкоклеточного рака возникают, как правило, при исследовании биоптатов, полученных при бронхоскопии. Так, по данным W. МсNее и соавт. (1983), два гистолога не смогли диагностировать по бронхобиоптатам мелкоклеточный рак в одной трети случаев. В то время, как по операционному материалу точная диагностика имела место в 90% случаев. Наилучшие результаты получены при диагностике овсяноклеточного рака (точность 94%).
В то же время, диагностика морфологических вариантов разными гистологами существенно различается. Совпадение результатов отмечалось в 38% в соответствии с классификацией ВОЗ,1967 и в 54% в соответствии с классификацией ВОЗ,1981. Исходя из этих фактов, можно прийти в выводу, что опытные гистологи используют свои индивидуальные критерии для выделения подтипов мелкоклеточного рака, что в дальнейшем экстраполируется на оценку клинического статуса и прогноза. По мнению D. Lamb (1984), это связано с тем, что основные принципы распознавания подтипов опухоли, положенные в основу классификации ВОЗ (1981), являются не вполне определенными. Общепризнанно, что остается еще мало изученной группа новообразований, которые нельзя достоверно отнести к мелкоклеточному раку (из клеток промежуточного типа) или крупноклеточному недифференцированному раку.
R.T.Vollmer (1982), измерив клетки и диаметр ядер мелкоклеточных и крупноклеточных недифференцированных форм рака, выявил, что резких отличий между размерами клеток и ядер в этих группах не существует. Нарастание этих размеров происходит постепенно и между крайними вариантами данных двух групп имеется целый ряд опухолей, которые невозможно достоверно отнести к мелкоклеточному или крупноклеточному раку. Таким образом, определение размеров клеток не имеет решающего значения для определения варианта недифференцированного рака. На практике чаще приходится ориентироваться на общее строение опухоли (наличие розеток и т.д.).
Разделение аденокарцином на 4 типа имеет условный характер, так как варианты строения (ацинарный, папиллярный, бронхиолоальвеолярный и солидный) являются, по сути дела, типами роста опухоли, нередко обнаруживаемыми в различных ее участках. Тем не менее, при решении вопросов о степени дифференцировки приходится учитывать особенности типов роста этих опухолей. Так, для аденокарцином с признаками ацинарного строения снижение степени дифференцировки сопряжено с уменьшением количества ацинарных структур и выраженной тенденцией к формированию солидных полей.
D. Lamb (1984) предлагает к высокодифференцированным опухолям относить те аденокарциномы, в которых четко выявляется преобладание ацинарных или криброзных структур. Умеренно дифференцированная аденокарцинома содержит такие структуры менее, чем в 50% полей зрения с большим увеличением. Низкодифференцированные опухоли имеют незначительное количество железистых структур (менее 10% полей зрения с большим увеличением). Определение степени дифференцировки аденокарцином с папиллярным и бронхиолоальвеолярным типами роста не имеет в настоящее время достаточно объективных критериев.
Крупноклеточный рак представляет собой группу малодифференцированных подтипов рака, которые с учетом современных диагностических возможностей, по-видимому, следует исключить из классификации как самостоятельную нозологическую форму. Еще K.Lindberg (1935) и А.А.Абрикосов (1947) отмечали признаки железистой или плоскоклеточной дифференцировки в крупноклеточном раке. Между различными опухолями этой группы имеются и различия в клиническом течении.
Крупноклеточный рак с признаками плоскоклеточной дифференцировки (стратификацией) имеет лучший прогноз после хирургического лечения, чем другие подтипы крупноклеточного рака. Особые трудности представляет диагностика крупноклеточного рака по материалу эндоскопической биопсии. M. T. Chuang и соавт. (1984), сравнивая результаты дооперационной и послеоперационной диагностики, установили, что только в 3 случаях из 24 гистологический диагноз крупноклеточного рака подтвердился после операции.
Железисто-плоскоклеточный (аденосквамозный) рак представляет небольшую группу новообразований. Если при гистологическом исследовании всех случаев плоскоклеточного рака легкого применять дополнительную окраску на слизь, то около 5% новообразований имеют признаки слизистой секреторной активности. Такие случаи следует отличать от мукоэпидермоидного рака, который встречается крайне редко и имеет специфические особенности строения.
В классификациях ВОЗ 1967 и 1981 гг. нейроэндокринные поражения легкого объединены под термином «карциноидные опухоли». При этом в классификации ВОЗ 1981 г. зафиксировано существование морфологически злокачественного карциноида (атипичный карциноид). Если диагноз классического карциноида не представляет трудности, то критерии диагностики атипичного карциноида весьма расплывчаты.
При ретроспективном пересмотре гистологических препаратов D.Maloney и соавт. (1983) 11 из 850 опухолей легких отнесли к атипичным карциноидам. Ранее эти новообразования были расценены как недифференцированный крупноклеточный или мелкоклеточный рак. Эти опухоли могут напоминать карциноиды, так как клетки их имеют округлые ядра и ацидофильную мелкозернистую цитоплазму, но размеры клеток более крупные, при этом отмечается также более выраженный полиморфизм и наличие митозов. В строении атипичных карциноидов также могут отмечаться характерные черты: розетки, периваскулярные структуры и т.д.
В случаях, когда отсутствуют типичные гистологические черты карциноида, опухоли могут иметь сходство с мелкоклеточным раком из клеток промежуточного типа. В то же время, клиническое течение атипичного карциноида существенно отличается от течения мелкоклеточного рака. Так, по данным D. Maloney и соавт. (1983), 5 из 11 больных с атипичным карциноидом прожили более 5 лет после хирургического лечения, а остальные, признанные неоперабельными, прожили 5 лет после лучевой терапии по радикальной программе.
Опухоли бронхиальных желез в классификации ВОЗ 1981 г. разделены на две группы, одну из которых относят к доброкачественным новообразованиям, а другая обозначается как рак бронхиальных желез. При этом новая терминология более точно отражает клиническое течение этих типов опухоли. Термин «цилиндрома» изменен на термин «аденокистозный рак», а «мукоэпидермоидная опухоль» на «мукоэпидермоидный рак».
Следует подчеркнуть, что эта группа новообразований является наиболее сложной для дифференциальной диагностики по материалам бронхобиопсии в связи с неоднородностью строения в различных участках одной опухоли. На наш взгляд, это обстоятельство и является причиной нередких расхождений между результатами анализа дооперационных биоптатов и послеоперационного морфологического исследования в определении нозологической формы новообразования. Исходя из этого, следует полагать, что именно репрезентативность, а также количество диагностического материала, полученного из различных участков новообразования для гистологического и цитологического исследований, является решающим фактором, влияющим на результаты дооперационной диагностики.
Особая актуальность этой проблемы становится очевидной при определении характера объемного процесса, рентгенологически оцениваемого как рак, когда материал биопсии бывает представлен картиной воспалительных или деструктивных изменений. Действительно, если для заключения «рак» бывает достаточно единичной группы клеток, полученных при бронхоскопии, игловой биопсии или в мокроте, то для исключения рака требуется исследование всего новообразования с применением различных дополнительных методов, так как в опухоли участки рака нередко сочетаются с участками воспаления и десмопластических реакций.
В этой ситуации велика роль забора материала для исследования. При этом решающее значение для гистолога имеют два обстоятельства: количество и качество биоптата, а также возможность получения материала для исследования из различных участков новообразования. В связи с этим, особенно результативной является возможность использования различных методик: трансбронхиальная биопсия, браш-биопсия, катетеризация бронхов и игловая биопсия. Это позволяет избежать ошибок, связанных с изучением только периферической зоны патологического процесса и резко увеличивает вероятность положительного ответа.
По данным G. Buirsky и соавт. (1981), при диагностике оптически видимых поражений проксимальных отделов бронхов использование биопсии и браш-биопсии давало соответственно 67 и 65%, а комбинация этих двух методов — 80% положительных результатов. Сочетание этих же двух методов с пункцией тонкой иглой через бронхофиброскоп увеличивало количество положительных результатов до 92%.
В процессе исследования биоптатов и хирургических препаратов особенно необходимо тесное сотрудничество патологоанатома с рентгенологом и хирургом. При микроскопической оценке операционного материала необходимо точное описание границ поражения и всех анатомических структур, на которые распространяется опухоль.
При игловой биопсии полученный участок ткани обычно не превышает 3 мм в диаметре. Обработку материала проводят с учетом необходимости подготовки дополнительных препаратов для гистологического исследования и специальных окрасок, а в некоторых случаях для бактериологического исследования. Кроме того, экономно распределяя материал, всегда стараются оставить резервный участок ткани, если это возможно.
Макроскопическое изучение препарата проводится с использованием лупы. Участки для гистологического исследования тщательно выбирают и фиксируют в протоколе. Особое внимание уделяют цвету, демаркационным линиям, маркировке, размерам очага поражения, отношению к бронхиальному дереву и сосудам. Иногда для выбора зоны исследования полезно изучить препарат по пробным замороженным срезам.
Режущий инструмент должен быть в идеальном состоянии, чтобы избежать артефактов на препаратах. После частичных резекций легкого в идеале препарат расправляют путем введения в просвет бронха формалина через катетер под давлением 25-30 мм водного столба. В нерасправившиеся участки вводят катетер меньшего диаметра. Препарат оставляют в формалине на 24 часа. Улучшенный вариант фиксации раздутого участка пораженного легкого и наиболее рациональные правила обработки морфологических препаратов предложили A.Gibbs (1990), K.Satoh и соавт.(1993).
При описании опухоли необходимо указать, из какого бронха она исходит, в каком сегменте располагается, расстояние между краем очага поражения и линией резекции бронха и легочной ткани, наименьшее расстояние до плевры, фоновые изменения (эмфизема, фиброз, ателектазы и др.). Обращают внимание на размеры, консистенцию, цвет и вид на разрезе лимфатических узлов.
Иммуногистохимическое исследование существенно расширяет возможности гистологической диагностики. Появляется возможность визуализации различных вне- и внутриклеточных маркеров, которые не определяются при обычном исследовании. Метод несложен и может применяться пpи обследовании всех больных без отбора. Внутриклеточные и мембранные антигены указывают на направление дифференцировки клеток опухоли. Часто удается определить интенсивность пролиферации. Такими маркерами являются промежуточные филаменты, биогенные амины, пептидные гормоны, ферменты, эпителиальные антигены, функциональные белки. Во время иммуногистохимического исследования учитывают чувствительность и специфичность тестов на тканевые маркеры. В настоящее время широко используют хромогранин А, нейронспецифическую енолазу, креатининкиназу ВВ, ароматическую кислую декарбоксилазу 145-kDa, мембранный антиген, апопротеины сурфактанта, моноклональные антитела для выявления элементов из клеток Клара, лактоферритин (выявление аденокарциномы бронхиальных желез и мукоэпидермоидного рака), актин, тубулин и др. Для оценки степени злокачественности и ростовых характеристик используют иммуногистохимические окраски на онкофетальные антигены, моноклональные антитела Ki-67, а также ростовые факторы (онкогены, рецепторы трансферина). В некоторых случаях помогает использование проточной цитометрии для оценки плоидности ДНК. Этот показатель может более точно указывать на прогноз, чем стадия и гистологический тип опухоли.
1.2. ОСОБЕННОСТИ ЦИТОЛОГИЧЕСКОЙ ДИАГНОСТИКИ И ПРОБЛЕМЫ КЛАССИФИКАЦИИ
В ряде случаев по объективным и субъективным причинам использование инвазивных методик для определения характера патологического процесса не представляется возможным. В этой ситуации диагностический приоритет целиком принадлежит эксфолиативной цитологии. К таким случаям относятся: рентгенологически и эндоскопически скрытый рак легкого; тяжелое состояние больного, не позволяющее использовать инвазивные методики; отсутствие соответствующего оборудования и навыков у персонала. Использование рутинных методов анализа мокроты у больных с различными стадиями и локализациями рака легкого позволяет получить положительные результаты у 70-80% больных. При этом отмечается отчетливая корреляция между числом положительных результатов и числом исследованных порций мокроты. Так, по данным L.G.Koss и соавт. (1964), среди больных с положительными результатами исследования мокроты, увеличение количества анализов с одного до пяти позволяло увеличить количество положительных результатов с 60,7% при однократном исследовании до 89% при исследовании трех порций и до 96% после пяти исследований.
В последние годы широко используются методы исследования концентрированной мокроты, среди которых наибольшее распространение получил способ концентрации злокачественных или атипичных клеток в мокроте, предварительно фиксированной в 50% этиловом спирте на 2% полиэтиленгликоле М1500-1600 (G. Saccomano и соавт., 1963). Использование методов концентрации клеток в мокроте позволяет достичь значительно большего числа положительных результатов у больных с небольшими новообразованиями. Сопоставив результаты диагностики с размерами опухоли, ее локализацией и гистологической формой, E. Risse и соавт. (1987) показали, что при размерах опухоли менее 24 мм рак можно диагностировать у 50%, более 24 мм у 84% всех больных при исследовании 5 порций мокроты. Центральный рак диагностирован в 100%, а периферический в 85% наблюдений. Плоскоклеточный рак диагностируется успешнее, чем неплоскоклеточный: соответственно 100 и 74% положительных результатов.
Отчасти значительные различия в чувствительности диагностических методов объясняются тем, что в большинстве случаев плоскоклеточный рак развивается в крупных бронхах. С применением метода концентрации клеток в мокроте достигнуты заметные успехи в диагностике раннего рака легкого, когда рентгенологическое и даже бронхоскопическое обследование малоэффективно. Изучена также динамика предшествующих раку метапластических изменений бронхиального эпителия, что позволяет формировать группы повышенного риска. В то же время Truong и соавт. (1985) не отмечают высокой информативности таких исследований мокроты и указывают, что средняя чувствительность различных методов цитологической диагностики следующая: мокрота — 60%, бронхиальные смывы — 66%, браш-биопсии — 77%. Следует признать, что чувствительность цитологической диагностики при бронхоскопическом исследовании можно существенно повысить путем соответствующей организации диагностического процесса. При прицельной катетеризации бронхов с рентгенотелевизионным контролем и экспресс-цитологическим контролем удается достичь 88,8% положительных результатов у больных с периферическим раком легкого (Ф.А.Астраханцев и Т.И.Нечаева, 1972). При этом оказалась возможной оценка не только локального статуса, но и состояния окружающих опухоль тканей, так называемой сопутствующей клеточной реакции. Важно отметить, что у больных периферическим раком легкого чувствительность цитологической диагностики повышается при постбронхоскопических исследованиях нескольких порций мокроты.
Высокой эффективностью (до 96,5% положительных результатов) характеризуется также метод чрескожной биопсии, выполняемый под рентгенотелевизионным и экспресс-цитологическим контролем (Ф.А.Астраханцев и соавт., 1986).
Развитие методов инвазивной диагностики поставило перед цитологами более сложные задачи, однако и до настоящего времени дифференциальная цитологическая диагностика опухолевых поражений легких представляет серьезную проблему. По-видимому, полное использование гистологической классификации при определении типа и подтипа опухоли с помощью гистологических критериев невозможно. Длительное время большинство цитологов ориентировалось на простую трактовку опухолевых типов и критериев их диагностики в соответствии с классификацией, предложенной L.Koss (1961):
Цитологическая классификация новообразований легкого:
- Плоскоклеточный рак
- Высокодифференцированный эпидермоидный или плоскоклеточный рак
- Низкодифференцированный эпидермоидный рак — крупноклеточный вариант
- Низкодифференцированный эпидермоидный рак — мелкоклеточный вариант или овсяноклеточный
- Аденокарцинома
- Терминальная бронхиолярная аденокарцинома (включая так называемый легочный аденоматоз и альвеолярноклеточный рак)
- Первичная аденокарцинома «центрального» происхождения (включая рак, возникающий из слизистых желез)
- Мукоэпидермоидный рак «Аденома» бронха
- Опухоли, сходные с новообразованиями слюнных желез
- Карциноидный тип
В дальнейшем был предпринят ряд попыток максимально приблизить цитологические классификации к гистологическим классификациям новообразований ВОЗ. В цитологическом варианте (1977 г.) предложены следующие рубрикации:
- Доброкачественные опухоли
- Плоскоклеточная метаплазия
- Атипичная плоскоклеточная метаплазия (дисплазия и рак in situ)
- Атипичная плоскоклеточная анаплазия
- слабая
- умеренная
- выраженная
- Рак in situ
- Атипичная плоскоклеточная анаплазия
- Злокачественные опухоли
- Плоскоклеточный рак
- Мелкоклеточный рак
- Аденокарцинома
- бронхогенная
- бронхиолоальвеолярная
- Крупноклеточный рак
- Вторичные опухоли
- Неклассифицируемые опухоли
- Смешанные опухоли
На наш взгляд, эта классификация в значительной степени адаптирована к оценке эксфолиативного материала (мокрота, смывы). В ней отсутствует ряд новообразований, хорошо идентифицируемых при цитологическом исследовании мазков-отпечатков с бронхобиоптатов и игловой биопсии (опухоли бронхиальных желез, варианты мелкоклеточного рака, карциноиды и т.д.). Более обширная цитологическая классификация предложена группой цитологов СЭВ, 1983 г.:
- Реактивные и предопухолевые изменения эпителия при некоторых заболевания легких
- Гиперплазия клеток бронхиального и альвеолярного эпителия
- Плоскоклеточная метаплазия клеток бронхиального эпителия
- Опухоли легкого
- Рак
- Плоскоклеточный с ороговением (высокодифференцированный)
- без ороговения (умеренно дифференцированный)
- с низкой степенью дифференцировки
- Аденокарцинома высокодифференцированная (ацинозная, сосочковая),
- умеренно дифференцированная (железисто-солидная) с низкой степенью дифференцировки
- Недифференцированный мелкоклеточный, крупноклеточный тип
- Карциноид
- Опухоли из бронхиальных желез цилиндрома мукоэпидермоидная опухоль
- Гамартома
- Неэпителиальные опухоли: доброкачественные , злокачественные
- Рак
Однако и эта классификация не лишена недостатков. В ней встречаются терминологические неточности (например, термин «цилиндрома» вместо общепринятого «аденокистозный рак»). Представляется сомнительным объединение в одной рубрике реактивных и предопухолевых изменений эпителия без выделения такой чрезвычайно важной рубрики, как атипическая плоскоклеточная метаплазия (дисплазия)единственного состояния, которое можно на основании цитологических критериев рассматривать как предопухолевую трансформацию эпителия при формировании групп повышенного риска.
Рассматривая вопрос о практическом применении цитологических классификаций, следует подчеркнуть, что использование их в расширенном объеме, по-видимому, более целесообразно в тех случаях, когда имеется возможность изучения мазков-отпечатков с различных участков опухолей и сопоставления этих данных с результатами гистологического исследования в целях взаимного дополнения и коррекции. Когда речь идет о дооперационной диагностике, то представляется более целесообразным, ввиду многочисленных объективных и субъективных ограничений, определять нозологическую форму опухоли в пределах 4 основных групп.
При этих условиях можно отметить высокую степень общих совпадений дооперационных цитологических и послеоперационных гистологических заключений -74,6-80% с широкими колебаниями в пределах отдельных нозологических форм. Так, если при высокодифференцированном плоскоклеточном и мелкоклеточном раке отмечается до 90% совпадений, то при низкодифференцированном плоскоклеточном раке и аденокарциноме, а также крупноклеточном раке — в пределах 50% (Т.И.Нечаева и соавт., 1966).
На этом основании H.Suprun и соавт. (1980) выделяют две группы больных: с высокой результативностью цитологического типирования (плоскоклеточный ороговевающий рак — 81%, мелкоклеточный рак — 97%) и с низкой результативностью цитологического типирования (умеренно дифференцированный плоскоклеточный рак — 67%, недифференцированный крупноклеточный рак — 59%, аденокарцинома с преобладанием низкодифференцированного компонента — преимущественно солидная — 53%, бронхиолоальвеолярная аденокарцинома — 44%).
По мнению H.Suprun и соавт. (1980), к наиболее частым причинам неправильного определения гистологического типа рака легкого при цитологическом исследовании относятся следующие:
- Вид и степень дифференцировки могут существенно варьировать в пределах одной опухоли.
Некротические изменения в железистом раке могут индуцировать неспецифическую окраску цитоплазмы, напоминающую кератинизацию.
При умеренно и низкодифференцированном плоскоклеточном раке клетки в пластах наслаиваются друг на друга (имитация двуядерных клеток), имеют ядра разного размера, нередко с крупными ядрышками, что приводит к ложному заключению об аденокарциноме. - Цитологическая, также как и гистологическая дифференциальная диагностика низкодифференцированных форм плоскоклеточного рака, низкодифференцированной аденокарциномы и анапластических подтипов нередко затруднительна.
- Очень малый объем материала, полученного при фиброскопии, не позволяет точно оценить низкодифференцированную опухоль или делает диагноз невозможным. Отдельные веретено-полигональноклеточные недифференцированные типы рака могут быть ошибочно расценены как низкодифференцированный плоскоклеточный подтип.
С учетом возможностей и ограничений цитологического и гистологического методов исследования для достижения большего числа положительных результатов при оценке материала бронхоскопии необходимо стремление к взаимопониманию и сотрудничеству цитолога и гистолога. Попытки чрезмерно детализировать нозологическую диагностику на основании цитологических критериев может способствовать гипердиагностике. В связи с этим, для определения дальнейшей лечебной тактики необходимо в первую очередь решить вопрос о принадлежности опухоли к мелко- или немелкоклеточному раку.
Если установлен диагноз немелкоклеточного рака, то при отсутствии светооптических признаков дифференцировки по какому-либо из известных типов, опухоль может быть классифицирована как крупноклеточный недифференцированный рак. Однако, с учетом важности этого диагноза в плане решения вопросов тактики лечения и прогноза, желательно уточнение его, при возможности, с помощью дополнительных методов исследования (электронная микроскопия, иммуногистохимические методы).
С учетом вышеизложенного необходимо подчеркнуть чрезвычайно важное обстоятельство: диагноз недифференцированного рака, установленный в дооперационном периоде на основании светооптических методов исследования, не должен являться основанием для отказа в радикальном лечении при отсутствии других противопоказаний.
1.3. КЛИНИЧЕСКОЕ И ПРОГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ ГЕТЕРОГЕННОСТИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ЛЕГКОГО
Существенные разногласия при оценке одних и тех же новообразований различными гистологами в значительной степени обусловлены тем обстоятельством, что многие опухоли в различных участках могут иметь разную степень дифференцировки, а в некоторых случаях представлены комбинациями различных гистологических типов.
Исходя из этих фактов, в последние годы сформулировано понятие о гетерогенности опухоли. В основе гетерогенности лежат биологические факторы (генетическая нестабильность и селекция клеточных элементов новообразования в процессе роста опухоли), а также различные эпигенетические факторы, влияющие в процессе дифференцировки на клеточный фенотип. В зависимости от метода исследования опухоли можно обнаружить различные проявления ее гетерогенности: морфологические и функциональные.
Вопросы морфологической гетерогенности рака легкого и ее значение для точности диагностики в последнее время привлекают особое внимание. Гетерогенность опухоли может выявляться обычными методами исследования, как правило, при изучении всего объема первичного очага. V. Roggli и соавт. (1985) провели анализ 100 наблюдений рака легкого с применением детального гистологического изучения в соответствии с классификацией ВОЗ 1981 г. Пятью гистологами методом рандомизации изучались препараты, полученные с 10 блоков из различных участков опухоли, окрашенные гематоксилином и эозином и по Крейбергу. При компьютерной обработке данных выяснилось, что мнения 3 из 5 участников просмотра в оценке основного гистологического типа совпали в 94% случаев.
При диагностике мелкоклеточного рака мнения 4 из 5 совпали в 98% случаев, но только в 72% случаев совпали мнения в отношении подтипа мелкоклеточного рака. 34% всех новообразований оценены как гомогенные, в 21% наблюдений выявлены малые признаки гетерогенности (различия в пределах одного гистологического типа)сочетание различных вариантов строения или дифференцировки, а в 45% случаев отмечена гетерогенность гистологических типов (например, комбинация плоскоклеточного рака и аденокарциномы). При сравнении этих данных с результатами исследований Reid и Carr (1961), авторы пришли к выводу, что для правильной оценки гистологического типа необходимо исследование не менее четырех участков опухоли.
Эти данные подтверждены электронно-микроскопическими исследованиями. E.M. McDowell и соавт. (1978) предполагают, что большинство типов рака легкого развивается из базальных или слизистых, а также нейросекреторных клеток и клеток Клара, обладающих различными потенциями дифференцировки, проявляющимися в одной и той же опухоли в различных соотношениях под влиянием селективных и эпигенетических факторов. Авторы предприняли попытку разработать гистогенетическую классификацию рака легкого на основе ультраструктурного анализа 100 новообразований.
Нами произведено сопоставление ультраструктурных данных, положенных в основу гистогенетической классификации, предложенной E.M.McDowell и соавт. (1978), с результатами оценок тех же новообразований в соответствии с гистологической классификацией ВОЗ (1981). Анализируя полученные данные, а также результаты ряда других исследователей, мы пришли к выводу, что использование только гистологических методов диагностики в значительной степени снижает возможность точного распознавания опухоли, отчасти вследствие субъективизма, связанного с нечеткой очерченностью нозологических форм, но в большей степени из-за ограниченных возможностей стандартных методик. Это становится особенно очевидным при сравнении результатов гистологического и электронно-микроскопического исследований опухоли.
Небольшие железистоподобные структуры при высокодифференцированном плоскоклеточном раке, выявляющиеся на светооптическом уровне и служащие основанием, согласно рекомендации ВОЗ (1981), для определения железисто-плоскоклеточного рака, оказываются при ультраструктурном анализе ультраструктуры в ряде случаев остатками предсуществующих структур легочной ткани и представляют собой альвеолярные структуры из пневмоцитов II типа. В то же время в значительной части опухолей, расценивающихся светооптически как плоскоклеточный рак умеренной дифференцировки, при ультраструктурном исследовании различных участков новообразований выявляются признаки железистой дифференцировки.
Аналогичная ситуация возникает при исследовании недифференцированных подтипов рака, оцениваемых на основе рекомендаций ВОЗ (1967,1981). Многие из этих новообразований при ультраструктурном анализе являются низкодифференцированным плоскоклеточным или железистым раком. Таким образом, при детальном исследовании рака легкого с применением комплекса различных методов морфологического исследования, как правило, выявляется гетерогенность новообразования, которая ограничивает возможность точной диагностики опухоли стандартными методами исследования (табл. 1).:
Таблица 1.
СРАВНЕНИЕ ГИСТОГЕНЕТИЧЕСКОЙ КЛАССИФИКАЦИИ (McDowell и соавт.,1978) С ГИСТОЛОГИЧЕСКОЙ КЛАССИФИКАЦИЕЙ ОПУХОЛЕЙ ЛЕГКИХ (ВОЗ,1981)
Глава 2. Опухоли из бронхиального эпителия
Согласно современным представлениям все элементы выстилки дыхательныпутей имеют энтодермальное происхождение и развиваются из эпителиального выроста передней стенки головной кишки.
Дифференцировка всех видов клеток эпителиальной выстилки дыхательных путей и клеток слизисто-серозных желез происходит между 6-й и 17-й неделями эмбрионального развития(N-197-N)периода, обозначаемого как псевдожелезистый, когда формирующееся легкое имеет вид, гистологически сходный с железами эндокринного типа. Гистогенез эпителиальных клеток дыхательных путей представлен в схеме.
Гистогенетические источники эпителиальных клеток «R» дыхательных путей (по J.Sturgеss, 1985).
2.1. ОНКОГИСТОГЕНЕЗ
Клеточный состав эпителиальной выстилки легкого человека в разных отделах трахеобронхиального дерева неоднороден. В трахее и бронхах он представлен основными типами клеток: базальные, нейроэпителиальные, слизистые, реснитчатые и реснитчато-слизистые. Эти отделы дыхательных путей содержат также подслизистые железы, имеющие слизистые, серозные клетки, клетки протоков и онкоциты.
Эпителиальная выстилка бронхиол имеет меньшую толщину и представлена реснитчатыми цилиндрическими клетками и не продуцирующими слизь цилиндрическими клетками (клетками Клара). Альвеолы выстланы пневмоцитами I и II типа. Отдельные авторы дополнительно описывают пневмоциты III типа.
2.1.1. Клеточный состав эпителиальной выстилки
Базальные клетки в норме не достигают просвета, формируют непрерывный слой, расположенный на базальной мембране. Обычно можно различить два и более слоев этих клеток. Эти клетки овоидной формы, ядра их крупные, занимают большую часть клетки и имеют инвагинации. Цитоплазма содержит большое количество рибосом и тонофиламентов, слабо развитый аппарат Гольджи, отдельные митохондрии, короткие профили ШЭР, единичные лизосомы и гранулы гликогена.
Нейроэпителиальные клетки (синонимы: нейросекреторные, клетки Кульчицкого, К-клетки) содержат аргирофильные гранулы нейросекреторного типа. Они рассеяны в крупных бронхах, встречаясь чаще с уменьшением калибра бронха, но в бронхиолах относительно редки. Нейросекреторные клетки могут также образовывать небольшие группы из 3-5 клеток (так называемые нейросекреторные тельца). Клетки имеют пирамидальную или треугольную форму. Ядра их округлые или овальные. Основная масса цитоплазмы сконцентрирована в базальных отделах, апикальный отдел цитоплазмы узкий, в отдельных случаях выступает в просвет дыхательных путей. Цитоплазма содержит развитый аппарат Гольджи, много свободных рибосом, хорошо развитый эндоплазматический ретикулум, преимущественно гладкий, множественные пучки промежуточных филаментов и характерные округлые гранулы нейросекреторного типа диаметром от 80 до 170 нм.
Недифференцированные цилиндрические (промежуточные) клетки выявляются в эпителиальной выстилке в небольшом количестве и располагаются над базальными клетками. Они являются предшественниками слизистых и реснитчатых клеток. Апикальные отделы клеток достигают просвета дыхательных путей. Клетки имеют крупное овальное ядро и обильную электронноплотную цитоплазму, содержащую митохондрии,короткие профили ШЭР, отдельные мелкие лизосомы, отмечается большое количество полирибосом. Тонофиламентов в них обычно меньше, чем в базальных клетках. На поверхности клеток, обращенных к просвету, имеются микроворсинки. Изредка встречаются отдельные клетки, сходные с недифференцированными, но имеющие в апикальных отделах признаки цилиогенеза либо слизеобразования, либо сочетания их.
Эпителиальные секреторные клетки. Преобладающими представителями этой группы являются бокаловидные клетки, встречающиеся преимущественно в трахее и бронхах. Единичные клетки этого типа обнаруживаются также в бронхиолах. Форма клеток обусловлена значительным расширением апикальных отделов за счет накопления многочисленных крупных слизистых гранул. Узкий вытянутый базальный отдел клетки контактирует с базальной мембраной на небольшом участке. Ядро овоидной формы с неправильными очертаниями и маленьким ядрышком смещено к основанию клетки, где также выявляется небольшое количество митохондрий и тонофиламентов. Над ядром обнаруживается хорошо развитый аппарат Гольджи, а в парануклеарных пространствах — полярно ориентированные хорошо развитые профили ШЭР. Слизистые гранулы окружены тонкой, непостоянной мембраной и содержат гомогенный материал низкой электронной плотности. Апикальная поверхность клеток имеет микроворсинки различной длины, количество их также варьирует. На поздних стадиях секреции бокаловидные клетки имеют набухшую поверхность, по-видимому, за счет накопления слизи. К разновидностям слизепродуцирующих клеток относят также так называемые клетки с мелкими слизистыми гранулами, которые повсеместно встречаются в выстилке дыхательных путей. Эти клетки отличаются от бокаловидных наличием лишь небольшого количества мелких секреторных гранул, рассеянных в апикальной части цитоплазмы. На поверхности клеток обнаруживаются пальцевидные выступы цитоплазмы, обращенные в просвет дыхательных путей.
Описана также еще одна разновидность слизепродуцирующих клеток, так называемые щеточные клетки. Некоторые авторы полагают, что бокаловидные клетки после опорожнения приобретают вид, не характерный ни для слизистых, ни для реснитчатых клеток. На их свободной поверхности появляется большое количество мономорфных правильно ориентированных ворсинок, придающих поверхности клеток сходство со щеточной каемкой.
Клетки Клара (бронхиальные, нереснитчатые, не продуцирующие слизь, цилиндрические эпителиальные клетки). В эпителиальной выстилке бронхиол среди реснитчатых клеток встречаются отдельные более высокие клетки, не имеющие ресничек, секретирующие по апокриновому типу. Клетки имеют цилиндрическую форму, центрально расположенное ядро с глубокими инвагинациями в цитоплазме, большое количество митохондрий, развитый аппарат Гольджи, развитый гладкий и шероховатый эндоплазматический ретикулум. Апикальная часть содержит хорошо развитый, частично дезинтегрированный гладкий эндоплазматический ретикулум, расширенные цистерны которого, а также отдельно лежащие окруженные мембраной секреторные гранулы, содержат аморфный мелкогранулярный материал слабой электронной плотности. Митохондрии в апикальных отделах немногочислены, отличаются сферической формой, местами лишены крист, заполнены матриксом слабой электронной плотности. Клетки Клара отличаются высоким уровнем метаболизма, секретируют биологически активные вещества липопротеиновой природы. Полагают также, что эти клетки участвуют в синтезе вещества типа сурфактанта.
Реснитчатые клетки имеют цилиндрическую форму, расположены более узким основанием на базальной мембране, а апикальный их отдел достигает просвета дыхательных путей. Их количество обычно превышает количество слизепродуцирующих клеток. Отличительной особенностью этих клеток является наличие на апикальной поверхности большого количества ресничек с базальными тельцами в основании, микроворсинок и тонких выростов цитоплазмы. Цитоплазма этих клеток электроннопрозрачная из-за отсутствия секреторных гранул, содержит небольшое количество рибосом, короткие профили ШЭР, хорошо развитый аппарат Гольджи, отдельные тонофиламенты, а также глыбки гликогена. Ядра клеток содержат гипертрофированное ядрышко.
Реснитчато-слизистые клетки. Эта редкая разновидность клеток имеет сформированные реснички и содержит гранулы слизи.
Пневмоциты. Респираторные отделы легких выстланы непрерывным слоем эпителиальных клеток, обозначаемых пневмоцитами, которые различаются размерами и формой. Преобладают более мелкие, уплощенные пневмоциты I типа. Центральная часть клетки более утолщена и занята ядром округлой или овальной формы. Уплощенная часть клетки простирается по базальной мембране в виде тонких цитоплазматических отростков на значительные расстояния. Цитоплазматические органеллы развиты скудно. Между этими клетками располагаются менее многочисленные крупные пневмоциты II типа. Эти клетки имеют округлую форму, относительно небольшое овальное ядро. Цитоплазма клеток обильная с хорошо развитым аппаратом Гольджи и эндоплазматическим ретикулумом. Отличительной особенностью пневмоцитов II типа является наличие в их цитоплазме осимофильных пластинчатых телец, представляющих собой крупные окруженные мембраной округлые тельца, содержимое которых имеет слоистое строение. Встречаются также так называемые мультивезикулярные тельца и тельца сложного строения, содержащие пузырьки и пластинки вещества высокой электронной плотности. Пластинчатые тельца образованы фосфолипидами, секретируются путем экзоцитоза. С ними связан синтез сурфактанта, выделяющегося на альвеолярную поверхность.
Эпителиальные клетки слизисто-серозных желез. Слизисто-серозные железы состоят из секреторных трубочек, собирательных пространств и общего выводного протока. Секреторные трубочки выстланы слизистыми и серозными клетками. Слизистые клетки имеют цилиндрическую форму, заполнены гранулами слизи, оттесняющими ядро к основанию клетки. Серозные клетки выстилают более короткие серозные трубочки, примыкающие к концам слизистых трубочек. Они имеют пирамидальную форму и округлое базально расположенное ядро с гипертрофированным ядрышком. В апикальном отделе цитоплазмы имеется большое количество плотно расположенных мономорфных округлых секреторных гранул.
Собирательные протоки выстланы крупными клетками цилиндрической формы, котоpые содержат большое количество митохондрий, отличаются высокой метаболической активностью, не имеют признаков секреции слизи. Часть из них имеет значительно большие размеры, сходна с онкоцитами. Эти клетки имеют обильную цитоплазму, заполненную крупными митохондриями, и небольшое ядро. Помимо этой основной локализации, онкоциты встречаются также и в других отделах выстилки дыхательных путей. Главный выводной проток выстлан реснитчатыми клетками дыхательных путей.
Происхождение отдельных клеточных популяций эпителия выстилки дыхательных путей и их взаимное превращение до настоящего времени остается предметом дискуссии. В эксперименте было показано, что у животных практически все клетки эпителиальной выстилки дыхательных путей, за исключением зрелых реснитчатых клеток, способны к делению. Поэтому с уверенностью определить камбиальную клетку в настоящее время не представляется возможным.
В последние годы наибольшее распространение получила гипотеза Е.М.McDowell и соавт. (1978), основанная на изучении авторами эпителиальных элементов выстилки дыхательных путей человека и животных в норме, а также при гиперплазии и метаплазии. Авторы полагают, что в норме при делении недифференцированных клеток образуются популяции базальных клеток и клеток с мелкими слизистыми гранулами. При этом допускается, что последние два типа при дальнейшем делении и дифференцировке способны к взаимным превращениям, а избыточная пролиферация базальных клеток и клеток с мелкими слизистыми гранулами обозначается авторами как «базальноклеточная гиперплазия». Возможно также, что популяция примитивных недифференцированных (камбиальных) клеток поддерживается путем деления базальных клеток и клеток с мелкими слизистыми гранулами.
При соответствующей стимуляции клетки с мелкими слизистыми гранулами приобретают способность к выраженному слизеобразованию, превращаясь в бокаловидные клетки. В свою очередь, бокаловидные клетки после эвакуации секрета приобретают сходство с клетками с мелкими секреторными гранулами. По мнению авторов, это свидетельствует о том, что бокаловидные клетки являются одной из разновидностей метаплазии клеток с мелкими слизистыми гранулами, поэтому выделение бокаловидных клеток в отдельную клеточную популяцию является проблематичным. Этот вывод подтверждается тем обстоятельством, что в нормальных условиях бокаловидные клетки в выстилке дыхательных путей до настоящего времени не описаны, а наблюдаются только при внешних воздействиях, стимулирующих пролиферацию эпителиальных клеток.
При определенных условиях деление клеток с мелкими слизистыми гранулами приводит к нарастанию количества кубоидальных или уплощенных клеток, в дальнейшем кератинизирующихся. Это состояние обозначается как плоскоклеточная (эпидермоидная) метаплазия. Плоскоклеточная метаплазия является характерной реакцией бронхиального эпителия на повреждение и наблюдается при различных хронических заболеваниях, таких как бронхоэктазы, хронические абсцессы легких, туберкулез, хроническая пневмония. Р.Вирхов впервые обозначил метаплазию как «переходный процесс с устойчивым существованием клеток, ведущий к изменению характера ткани».
Суммируя данные исследования в области канцерогенеза, К. Muller (1979) к процессам, предшествующим раку легкого, относит следующие патологические состояния:
- Гиперплазия базальных клеток
- легкой степени (3-4 слоя)
- средней степени (4-5 слоев)
- выраженная (6 слоев и более)
- Гиперплазия бокаловидных клеток без или с переходом в метаплазию и дисплазию
- Плоскоэпителиальная (эпидермоидная) метаплазия
- с микропапилломатозом
- Дисплазия
- легкой степени (I)
- средней степени (II)
- выраженная (III)
- Рак in situ
- Микроопухоли (tumorlets)
- Атипия пневмоцитов I типа.
Метаплазия и предшествующие ей процессы наблюдались нами при различных патологических состояниях, таких как хронический бронхит, туберкулез, рак легкого. Изучены данные цитологического исследования, гистологический материал и ультраструктура эпителиальных клеток из участков базальноклеточной гиперплазии и плоскоэпителиальной (эпидермоидной) метаплазии.
2.1.2. Доброкачественные опухоли Папиллома
Опухоль представляет собой доброкачественную пролиферацию эпителия слизистой оболочки бронха. Изолированное поражение у взрослых считается чрезвычайно редким. У пожилых людей опухоль может сочетаться с очагами раннего рака. За рубежом описано 41 наблюдение (M. Aota et al.,1988; M. Hirasawa et al,1991).
Папиллому бронха впервые описал H.B. Orton в 1932 г. Наиболее часто новообpазование локализуется в гортани, особенно у детей. В 2-8% случаев поражение распространяется на трахею и бронхи (D.B. Singer et al.,1966). B. Hitz, E. Oesterlin (1932) считали, что опухоль распространяется на дыхательные пути в порядке «аэрогенного метастазирования». В последние годы этиологию папиллом связывают с инфицированием вирусом папилломы человека из семейства Papovaviridae (L. Gissman et al., 1982). Вирус из пораженных участков бронха типируют как HPV-6 или HPV-11 (J.D.Crissman et al.,1988).
Солитарная папиллома бронха обнаруживается обычно у мужчин старше 40 лет. Папилломатоз с поражением других органов впервые выявляют в среднем к 13,3 годам. Опухоль бронха проявляется кашлем, кровохарканьем, повторными пневмониями одних и тех же сегментов. Анамнез обычно продолжительный. В зависимости от патогенеза, J.M.Drenan, A.Douglas (1965) выделили три вида папиллом дыхательных путей:
- Множественные плоскоклеточные папилломы с поражением гортани, трахеи и бронхов. Обычно встречаются у детей. Склонны к спонтанной регрессии и самоизлечению в период полового созревания.
- Воспалительные полипы: экзофитные образования, покрытые цилиндрическим и реснитчатым эпителием. Ткани вокруг отечны, имеются признаки воспалительной инфильтрации.
- Солитарные плоскоклеточные папилломы, имеющие соединительнотканную строму и выстилку стратифицированным плоскоклеточным эпителием (метаплазия).
В некоторых случаях папилломы растут эндофитно (A.Zimmerman et al.,1980). Описан хронический полостной респираторный папилломатоз: в терминальных участках бронхиального дерева опухоль проявляется в виде кистозных образований. Нарушение вентиляции приводит к образованию абсцессов и крупных кист, выстланных плоским эпителием с множественными папилломами. При электронной микроскопии в клетках опухоли обнаруживаются вирусные частицы (S.W.Kegley et al., 1989). Нередко при выраженной атипии метаплазированного эпителия морфологическую картину ошибочно расценивают как прединвазивный или папиллярный рак. Гипердиагностика обычно связана с повышением содержания ДНК в клетках опухоли.
Вместе с тем, у лиц старше 40 лет в единичных случаях возникает малигнизация папиллом (H. Spencer et al.,1980). Известны модифицирующие влияния облучения на скорость злокачественной трансформации этой опухоли (M. Majoros et al.,1963; N.S.Dallimore et al.,1985).
Больные с папилломами папилломатозом (бронхов) относятся к группе повышенного риска, хотя малигнизации в большинстве случаев не происходит на протяжении длительных сроков (30-40 лет). Светлоклеточная опухоль Светлоклеточную опухоль доброкачественного характера не следует путать со светлоклеточным раком (см. раздел 2.2.4). Ее описали в 1963 г. A.Libow и B.Castleman (4 наблюдения). К 1971 г. они собрали уже 12 наблюдений и настояли на выделении опухоли в отдельную нозологическую форму. Не исключено, что некоторые больные (по крайней мере два наблюдения), включенные Р.И.Вагнером и соавт.(1981) в свой клинический материал по светлоклеточному раку, в действительности страдали доброкачественной светлоклеточной опухолью.Как правило, опухоль проявляется округлым очагом в легком и выявляется случайно при рентгенологическом исследовании. Возраст больных — 30-60 лет. Солитарный узел до 4 см в диаметре хорошо отграничен от окружающей паренхимы легкого. Капсулы нет. На разрезе очаг поражения красновато-коричневого цвета. С бронхом узел не связан.
Гистологическая характеристика. Слои крупных светлых вакуолизированных клеток занимают все поле зрения. Иногда встречаются гигантские многоядерные клетки. Ткань опухоли богато васкуляризирована. Клетки располагаются вокруг капилляров, сосуды гиалинизированы. В цитоплазме ШИК-положительный материал, который окрашивается на гликоген и разрушается диастазой. Опухолевые элементы напоминают нейpогенного пpоисхождения клетки с ацидофильной цитоплазмой и содержат липохромный пигмент. Митозы отсутствуют. Некоторые клетки содержат в ядрах ацидофильные включения из гликогена.
Ультраструктура. 2-5% клеток опухоли содержат гранулы, связанные с мембраной, и напоминают структуры карциноидного типа. Некоторые авторы считают опухоль вариантом карциноида. Накопление гликогена в цитоплазме связывают с отсутствием фермента альфа-глюкозидазы. Опухоль растет очень медленно и никогда не метастазирует. Гистогенез ее связывают с гладкомышечными элементами или с перицитами сосудов.
2.1.3. Гиперплазия базальных клеток
Цитологическая характеристика. Базальные (резервные) клетки в мокроте обычно не дифференцируются, так как даже при патологических процессах, сопровождающихся гиперплазией бронхиального эпителия, с увеличением слоев базального эпителия, последний крайне редко достигает поверхностных отделов выстилки дыхательных путей. Этот процесс чаще наблюдается в главных бронхах, но может встречаться также и в бронхиолах вплоть до терминальных.Базальноклеточная гиперплазия выявляется в цитологическом материале, полученном при бронхоскопическом исследовании и, более редко, в материале трансторакальной игловой биопсии участков пневмосклероза или атипической пневмонии, рентгенологически расцениваемых как рак легкого. Гиперплазия базальных клеток распознается при наличии небольших фрагментов бронхиальной выстилки, состоящих из компактно расположенных мелких однотипных клеток округлой или полигональной формы.
Базальные клетки имеют относительно большое центрально расположенное темноокрашенное, в отдельных клетках сплющенное, ядро с мелкоячеистой структурой хроматина и ровным контуром ядерной мембраны. Ободок цитоплазмы узкий, базофильный, иногда с наличием фасеток на смежных поверхностях клеток. Характерна отчетливо выявляющаяся тенденция к созреванию клеточных элементов по направлению от центра пласта к периферии, где конфигурация клеток более цилиндрическая, ядра более светлые, а ободок цитоплазмы более широкий. Среди этих элементов иногда могут встречаться клетки цилиндрического эпителия с ресничками на апикальной поверхности цитоплазмы. Важно отметить, что фрагментация пластов и наличие изолированных базальных клеток не отмечаются. Вблизи этих пластов часто обнаруживаются бокаловидные клетки. Все перечисленные признаки помогают отличить базальноклеточную гиперплазию от низкодифференцированного рака.
Гистологическая характеристика. Гиперплазия базальных клеток отличается увеличением числа слоев базальных клеток от 3 до 10. Базальные клетки располагаются под цилиндрическим эпителием, где отмечается также гиперплазия бокаловидных клеток. При выраженной пролиферации базальных клеток верхние слои их достигают просвета дыхательных путей.
2.1.4. Плоскоклеточная метаплазия
Цитологическая характеристика. Плоскоклеточная метаплазия без атипии («правильная» метаплазия) характеризуется наличием небольших пластов и отдельных довольно мономорфных эпителиальных клеток размерами несколько крупнее базальных, сходных с элементами шиповатого слоя многослойного плоского эпителия. Характерно, что в пластах эпителиальные клетки располагаются практически в виде монослоя. Ядра в большинстве клеток крупные, округлые, с нежно мелкозернистым хроматином, в отдельных встречаются ядрышки. Поскольку плоскоклеточная метаплазия в известной степени имитирует созревание многослойного плоского эпителия, то обычно обнаруживаются плоскоэпителиальные клетки различной степени зрелости. В связи с этим, ядерно-цитоплазматическое соотношение в различных клетках варьирует от почти нормального до высокого, а цвет цитоплазмы от нежно до интенсивно базофильного.
Гистологическая характеристика. Эпителиальный пласт состоит из базальных клеток, покрытых одним или более слоями полигональных клеток, которые уплощаются по мере приближения к эпителиальной поверхности. Поверхностные клетки имеют уплощенную форму. В некоторых участках имеются признаки ороговения. В препаратах, окрашенных толуидиновым синим, на поверхности ороговевающих клеток, как правило, выявляются короткие микроворсинки. В некоторых местах межклеточные пространства расширены, видны межклеточные цитоплазматические мостики, а в цитоплазме — гранулы «кератогиалина». По соседству с очагами плоскоэпителиальной метаплазии часто обнаруживаются участки покровного эпителия с выраженной гиперплазией бокаловидных клеток (бокаловидноклеточная метаплазия).
В случаях, когда соседние участки представлены реснитчатым эпителием, между ними отмечается четкая граница. В зоне гиперплазии бокаловидных клеток между последними, как правило, выявляются цилиндрические клетки с темной цитоплазмой, лишенные ресничек. При окраске на слизь в апикальных отделах этих клеток выявляются мелкие слизистые гранулы (цилиндрические клетки с мелкими слизистыми гранулами). Hаряду с этим, в соседних участках строение слизистой может подвергаться более выраженным изменениям: над базальными клетками появляется один или несколько слоев полигональных клеток, содержащих мелкие секторные гранулы, а поверхностные слои в этом случае бывают представлены бокаловидными клетками, имеющими кубоидальную форму, либо полигональными клетками с мелкими слизистыми гранулами, либо совместно и теми, и другими.
Реснитчатые клетки в этих случаях встречаются крайне редко. Важно отметить характер распределения слизи в участках, подвергшихся метаплазии. По мере увеличения выраженности стратификации метаплазированного эпителия, гранулы слизи, первоначально обнаруживаемые в клетках всех слоев, кроме базальных, выявляются в поверхностных слоях, причем в самых поверхностных в наименьшей степени. Характер выявляемой слизи при гистохимических окрасках метаплазированных и неизмененных слизесодержащих клеток идентичен.
Ультраструктура. При электронной микроскопии среди пролиферирующих клеток базального типа, не имеющих четко выраженных признаков плоскоэпителиальной или железистой дифференцировки, встречаются полигональные и кубоидальные клетки, имеющие ультраструктуру, сходную с клетками с мелкими слизистыми гранулами. Эти клетки имеют на поверхности микроворсинки, а мелкие гранулы слизи обнаруживаются в апикальных отделах цитоплазмы. Отмечается хорошо развитый эндоплазматический ретикулум и гипертрофированный аппарат Гольджи.
По мере нарастания признаков стратификации появляются признаки эпидермоидной метаплазии. В эпителиальных клетках этих зон отмечается появление и прогрессирующее нарастание количества тонофиламентов, формирующих при выраженной кератинизации широкие разветвляющиеся пучки. Параллельно с этим отмечается уменьшение количества слизистых гранул, а в самых поверхностных слоях — их полное исчезновение. Нередко выраженное ороговение сопровождается в отдельных клетках признаками дисплазии, выражающейся в различной степени атипии ядер, которые принимают неправильную форму с глубокими инвагинациями ядерной мембраны и содержат крупные ядрышки.В главных бронхах и трахее могут встречаться участки, в которых превращение покровного эпителия в плоский происходит другим путем. Цилиндрические реснитчатые клетки пролиферируют без нарастания количества клеток с мелкими слизистыми гранулами. По мере увеличения количества слоев клетки наружного слоя уплощаются, контактируют между собой с помощью цитоплазматических мостиков, а в цитоплазме отмечается прогрессирующее увеличение пучков тонофиламентов.
Таким образом, эти данные свидетельствуют о том, что в основе плоскоэпителиальной метаплазии может лежать как пролиферация и прогрессирующая кератинизация слизепродуцирующих, так и не продуцирующих слизь клеток. Согласно современным представлениям, гиперплазия слизесодержащих клеток является наиболее характерной реакцией бронхиального эпителия на внешние воздействия. Как полагают эти авторы, процесс в конечном итоге завершается превращением слизистых цилиндрических (бокаловидных) клеток в кубоидальные и плоскоэпителиальные с появлением неороговевающего стратифицированного эпителия, а затем плоскоэпителиальной (эпидермоидной) метаплазии с кератинизацией. Взаимосвязь плоскоклеточной метаплазии и бронхогенного рака остается проблематичной. В то же время данные ряда исследователей позволяют рассматривать эпидермоидную метаплазию как одну из ранних стадий развития рака легкого (E. M. McDowell и соавт.,1978).
2.1.5. Дисплазия эпителия
Впервые дисплазия как патологическое состояние бронхиального эпителия была введена в классификацию ВОЗ в 1981 году в одной рубрике с carcinoma in situ, хотя объединение этих двух состояний не вполне правомочно, так как в этих случаях необходимо рассматривать дисплазию как облигатный предрак. Диспластические изменения в бронхиальном эпителии развиваются, как правило, в зоне эпидермоидной метаплазии и характеризуются прогрессирующим нарастанием клеточной и структурной атипии. В связи с этим целесообразно выделять 3 степени дисплазии: легкую, среднюю, выраженную.
Цитологическая характеристика. Цитологически при метаплазии с легкой (слабой) степенью атипии в отличие от «правильной» метаплазии в пластах отмечается нерезко выраженная вариабельность клеток в размерах. При этом отдельные клетки достигают довольно крупных размеров, но они мельче, чем элементы высокодифференцированного плоскоклеточного рака. Ядра крупные, в отдельных клетках гиперхромные, ядерно-цитоплазматическое соотношение отчетливо вариабельное. Ядерный хроматин мелкозернистый, местами отмечается маргинальная конденсация его у ядерной мембраны. Цитоплазма в большинстве клеток темно-базофильная.
При средней степени атипии клетки с одинаковой частотой встречаются в пластах или в виде разрозненных стpуктуp. Размеры клеток и их ядер, а также ядерно-цитоплазматическое соотношение весьма вариабельны. Отмечается наличие метаплазированных клеток, имеющих небольшие размеры (малые метаплазированные клетки). Нарастает количество клеток с гиперхромными ядрами. Ядерный хроматин зернистый, довольно обильный, отмечается тенденция к маргинальной конденсации его. В отдельных клетках отмечаются явления кариопикноза и кариорексиса.
При выраженной атипии в мокроте отмечается преобладание разрозненных клеток с признаками выраженного полиморфизма, а в инструментальном материале встречаются пласты с дискомплексацией клеток. Клеточные элементы более крупные, чем при «правильной» метаплазии. Ядерный хроматин грубозернистый, конденсируется у ядерной мембраны в виде крупных глыбок, наряду с этим отмечается наличие гипертрофированных нуклеол. Именно тяжелую дисплазию целесообразно рассматривать как облигатный предрак, так как по цитологическим критериям эти состояния практически не отличимы. Гистологическая характеристика. При легкой степени дисплазии в базальных отделах метаплазированного участка отмечается умеренно выраженный индивидуально клеточный полиморфизм, гиперхроматоз ядер с увеличением количества и укрупнением ядрышек, появлением митозов. При средней степени, наряду с вышеописанными изменениями, отмечается нарушение чередования слоев, нарастание митотической активности. При тяжелой степени дисплазии эти изменения захватывают все слои метаплазированного бронхиального эпителия; кроме того, отмечается выраженный ядерный полиморфизм, проявляющийся укрупнением ядер, дезагрегацией ядерного хроматина с появлением крупных глыбок и конденсацией их у ядерной мембраны.
2.1.6. Прединвазивный рак (carcinoma in situ)
В последние годы установилось мнение, что развитие рака in situ представляет собой перманентный процесс с нарастанием признаков клеточной анаплазии. Этот процесс был прослежен у одних и тех же лиц на материале, полученном при исследовании мокроты у курящих шахтеров урановых рудников (G. Saccomano и соавт.,1974). Эти данные приведены ниже.
Клеточные критерии различных фаз развития рака легкого ( по G.Saccomano и соавт., 1974) @BDYM = Метаплазия без атипии @BD3 = 1. @BD11 = Все клетки одинакового размера. @BD3 = 2. @BD11 = Ядра одинакового размера с нормальным ядерно-цито-плазматическим соотношением. @BD3 = 3. @BD11 = Ядерный материал нежный, мелкозернистый, с мелкими хромоцентрами, которые отчетливо меньше, чем ядрышки. @BD3 = 4. @BD11 = Цитоплазма обычно базофильная. @BD3 = 5. @BD11 = Клетки обычно встречаются в пластах, но могут быть разрозненными. Метаплазия со слабой атипией 1. @BD11 = Клетки слегка варьируют в размерах. @BD3 = 2. @BD11 = Ядра слегка варьируют в размерах, ядерно-цитоплазматическое соотношение может слегка варьировать. @BD3 = 3. @BD11 = Ядерный материал тонкодисперсный, с редкими гранулами хроматина вблизи ядерной мембраны. 4. @BD11 = Цитоплазма может быть ацидофильной. @BD3 = 5. @BD11 = Клетки обычно встречаются в пластах, но могут быть разрозненными. Метаплазия с умеренной атипией @BD3 = 1. @BD11 = Клетки весьма варьируют в размерах. Некоторые мельче, чем при слабой атипии. 2. @BD11 = Ядра значительно варьируют в размерах. @BD3 = 3. @BD11 = Ядерно-цитоплазматическое соотношение весьма вариабельно. Оно может быть выше или ниже нормального. @BD3 = 4. @BD11 = Ядерный материал тонкодисперсный в большинстве участков, но более обильный, особенно вдоль ядерной мембраны. @BD3 = 5. @BD11 = Отмечается фрагментация ядер, местами с отделением глыбок.@BD11 = @BD3 = 6. @BD11 = Цитоплазма может быть базофильной, но преобладает ацидофилия. @BD3 = 7. @BD11 = Клетки обычно обнаруживаются в пластах, но нарастает число разрозненных клеток. Метаплазия с выраженной атипией @BD3 = 1. @BD11 = Клетки резко отличаются в размерах, но в основном они крупнее, чем при умеренной атипии.@BD3 = 2. @BD11 = Ядерный плеоморфизм отчетливо выражен, ядерный материал грубый, встречается в виде глыбок около ядерных мембран.@BD3 = 3. @BD11 = Ядерно-цитоплазматическое соотношение резко варьирует, может быть выше или ниже нормального.4. @BD11 = Маленькие ядрышки могут быть ацидофильными.5. @BD11 = Преобладают клетки с ацидофильной цитоплазмой.6. @BD11 = Преобладают разрозненные клетки. Рак in situ @BD3 = 1. @BD11 = Клетки варьируют в размерах, но могут быть в 2 раза крупнее, чем при метаплазиях и выраженной атипии. Имеются разрозненные клетки и комплексы, количество последних больше, чем при инвазивном раке.@BD3 = 2. @BD11 = Ядерный хроматин грубый в виде крупных глыбок. Центры крупные, сходны с ядрышками, не всегда ацидофильны.3. @BD11 = Отмечается цитофагия и многоядерность.4. @BD11 = Преобладает ацидофилия цитоплазмы. Инвазивный рак @BD3 = 1. @BD11 = Клетки обычно крупнее, чем нормальные, выражен плеоморфизм, встречаются причудливые формы клеток. Клетки преимущественно разрознены, но обнаруживаются и комплексы.2. @BD11 = Ядерный материал грубый, в виде крупных глыбок.3. @BD11 = Ядрышки крупные, ацидофильные.@BD3 = 4. @BD11 = Ядерно-цитоплазматическое соотношение значительно варьирует, может быть выше или ниже нормального.5. @BD11 = Как правило, отмечается цитофагия и многоядерность.6. @BD11 = Цитоплазма может быть ацидофильной и базофильной.
Следует признать, что большинство исследователей не считают возможным достоверно дифференцировать carcinoma in situ и инвазивный рак на основе только цитологического исследования. К тому же у значительного числа лиц, обследованных G.Saccomano и соавт. (1974), развился в последующем мелкоклеточный рак. К настоящему времени нет опубликованных работ, в которых были бы представлены достоверные данные о частоте, прогрессии и регрессии цитологически умеренной или выраженной клеточной дисплазии или рака in situ, сходные с исследованиями в области предрака или рака шейки матки.
Цитологическая характеристика. В цитологической классификации опухолей (кроме опухолей женского полового тракта) предлагаются следующие опорные признаки для цитологической диагностики бронхогенного рака in situ, при котором встречаются: 1) отдельные злокачественные клетки, отвечающие строению плоскоклеточного рака, возможно менее полиморфные, чем клетки при классической инвазивной форме рака; 2) крупные клетки полигональной или неправильной формы с обильной обычно оранжевофильной или эозинофильной цитоплазмой и укрупненными слегка гиперхромными ядрами; 3) небольшие атипичные клетки плоского эпителия обычно округлой, овальной формы с признаками кератинизации; в последнем случае ядра округлой или несколько неправильной формы с различной степенью гиперхромии и глыбчатости хроматина.
Перечисленные признаки достаточно характерны для плоскоклеточного рака. Тем не менее, цитологические критерии, которые должны быть использованы для дифференциальной диагностики между дисплазией эпителия с выраженной атипией и раком in situ, остаются еще не вполне ясными. По-видимому, в каждом случае с чрезмерно подчеркнутыми признаками дисплазии необходимы повторные исследования мокроты либо бронхоскопия с изучением возможно большего числа образцов для обнаружения участка слизистой бронха, пораженной раком in situ. На наш взгляд, наиболее существенное значение в этой ситуации имеет состояние клеточных ядер.
При переходе дисплазии в рак отмечается ряд признаков, свидетельствующих о дистрофических и некробиотических изменениях структур ядерного хроматина и ядерной оболочки. Часто встречается фрагментация ядер с отшнуровыванием отдельных долек. Ядерный хроматин с участками разрушения и появлением зон просветления в ядрах. Характерно состояние ядерной оболочки. Отмечается неравномерное утолщение ее, местами она как бы сливается с участками маргинальной конденсации хроматина, становится расплывчатой и неразличимой. В других клетках, где отмечаются признаки кариопикноза, границы ядерной мембраны становятся отчетливо неровными, с остроугольными изгибами, инвагинациями и глубокими щелевидными впадинами. Характерны также признаки цитофагии, при этом нередки формирования структур типа «птичьего глаза» (начало формирования раковых жемчужин).
Обращает на себя внимание также и фон препарата. Отсутствие выраженных воспалительных и деструктивных изменений свидетельствует о том, что наблюдаемая атипия не является сопутствующей, например, туберкулезному эндобронхиту, при котором, как правило, наблюдаются выраженные изменения бронхиального эпителия. Чрезвычайно важен также такой признак, как значительное увеличение числа небольших атипичных клеток плоского эпителия. Наличие этих элементов, сходных с парабазальными, свидетельствует о чрезмерной интенсификации пролиферативного процесса, свойственного развитию рака. Гистологическая характеристика. Рак in situ обычно обнаруживается в виде сливающихся участков патологически измененного покровного эпителия, четко отграниченных от неизмененного респираторного эпителия. Опухоль поражает проксимальные отделы внутрилегочных дыхательных путей, особенно сегментарные бронхи, чаще верхних долей легких. Можно выделить 4 варианта рака in situ: рак in situ без признаков микроинвазии, рак in situ в сочетании с признаками микроинвазии, рак in situ в сочетании с микроинвазивной карциномой, поражающей различные участки дыхательных путей, участки прединвазивного рака в сочетании с узлом инвазивного роста.
Пораженный участок слизистой оболочки протяженностью до 4 мм имеет шероховатую поверхность, белесоватый цвет, достаточно четко отграничен от окружающей неизмененной слизистой бронха. В отдельных случаях такие участки могут быть представлены микропапилломатозными разрастаниями. При гистологическом исследовании опухоль имеет строение плоскоклеточного рака умеренной дифференцировки с ороговением поверхностных слоев, либо это высокодифференцированный плоскоклеточный рак с выраженным ороговением.
Следует отметить, однако, что тип дифференцировки рака in situ не имеет решающего значения для формы развивающейся в дальнейшем опухоли. Carcinoma in situ с выраженным ороговением в поверхностных отделах может развиться и в недифференцированный рак. Описанные выше патологические изменения могут захватывать не только слизистую оболочку бронхов, но также и устья, протоки и более глубокие отделы бронхиальных желез. В отдельных случаях опухоль не выявляется на поверхности бронха, а локализуется исключительно в бронхиальных железах. В случаях, когда в срезе попадают дистальные отделы протоков подслизистых желез с прединвазивным раком, это поражение необходимо отличать от инвазивного рака с инвазией подслизистых лимфатических сосудов.Начало инфильтрирующего роста (микроинвазивный рак) может отмечаться как в участках слизистой бронха, так и железах. При этом отмечается нарушение целостности базальной мембраны и проникновение опухолевых элементов в подслизистые отделы стенки бронха, сопровождающиеся воспалительной инфильтрацией окружающей опухоль стромы лимфоцитами и плазматическими клетками. Более выраженный инвазивный рост может сопровождаться и десмопластической стромальной реакцией. К микроинвазии следует относить случаи, в которых опухолевые клетки, инфильтрирующие стенку бронха, не проникают за пределы внутренней поверхности хряща.
L.Woolner и Farrow (1982) предлагают следующую градацию глубины инвазии для ренгенонегативного рака: 1) рак in situ; 2) до 1 мм — интраэпителиальный рак; 3) 2-3 мм — инвазия до бронхиального хряща; 4) 3-5 мм — полная инфильтрация стенки бронха; 5) больше 5 мм (5-10 — перибронхиальная инвазия. Эти степени градации имеют большое значение для клинической практики. Если 2-3 степени можно отнести к категории микроинвазивных форм рака, то при 4-й и, в особенности, при 5-й степени резко возрастает вероятность сосудистой инвазии с регионарным метастазированием. Следует отметить, что при глубине инвазии до 10 мм бронхогенный рак, как правило, является рентгенонегативным, а при глубине инвазии свыше 10 мм с прорастанием в окружающую легочную паренхиму или перибронхиальные лимфатические узлы опухоль становится рентгенопозитивной.
2.1.7. Инвазивный рак и его метастазирование
Макроскопическое исследование препарата после резекции легкого по поводу рака преследует следующие цели: сопоставление макроскопической картины с результатами рентгенологических и эндоскопических данных; определение стадии процесса для корректировки предшествующей клинико-рентгенологической кодификации (по ТNМ). Клинико-анатомической классификацией рака легкого выделены следующие варианты, находящие свое отражение в рентгенологической и эндоскопической картине.
КЛИНИКО-АНАТОМИЧЕСКАЯ КЛАССИФИКАЦИЯ РАКА ЛЕГКОГО (по А.И.Струкову, 1979)
@DYM = По локализации @D4 = прикорневой (медиастинальный, центральный), исходящий из стволового, долевого и начальной части сегментарного бронха @D4 = периферический (в том числе верхушечный), исходящий из периферического отдела сегментарного бронха и его более мелких ветвей, а также из альвеолярного или бронхиального эпителия смешанный (массивный) По характеру роста экзофитный эндофитный По форме: бляшковидный полиповидный эндобронхиальный диффузный разветвленный (перибронхиальный и периваскулярный) узловатый узловаторазветвленный Рак, возникающий из главных, долевых и сегментарных бронхов (центральный), при различных типах роста имеет неодинаковую макроскопическую характеристику. Исключительно экзофитный тип роста встречается только на ранних стадиях развития опухоли, а в дальнейшем (при глубине инвазии стенки бронха более 10 мм), как правило, отмечается смешанный экзо- и эндофитный характер роста.Экзофитно растущая часть опухоли имеет вид белесоватой бляшки или полипа, стенозирующего просвет бронха.
Опухоли проксимальных отделов бронхиального дерева часто вызывают гиповентиляцию и воспалительные изменения в легочной ткани, а локализация в более дистальных отделах нередко осложняется сегментарным ателектазом. В редких случаях рака легкого с выраженным экзофитным ростом опухоли достигают больших размеров, при этом отмечается выраженное растяжение и истончение стенки бронха, приобретающей белесый однородный вид, местами с остатками хрящевых пластинок.
При проксимальном распространении опухоли в отдельных случаях стенка бронха макроскопически может выглядеть неизмененной, а внутренняя поверхность его в пораженных участках тусклая, шероховатая. Выявление таких зон имеет значение для определения истинной распространенности опухолевого процесса при коррекции клинико-рентгенологических данных в соответствии с системой TNM.В большинстве случаев инвазивный рак, исходящий из крупных бронхов, имеет смешанный экзо- и эндофитный характер роста и формирует узел, в зону роста которого вовлекается периферическая легочная ткань и лимфатические узлы.Внешний вид узла при различных гистологических типах рака имеет некоторые характерные особенности.
Первичный очаг плоскоклеточного рака белесоватого или сероватого цвета, обычно довольно плотный за счет сопутствующей десмопластической реакции. Большие опухоли могут содержать обширные участки некроза, иногда с образованием полостей, имитирующих каверны. На разрезе четко определяются разрушенные бронхи, инфильтрированные опухолевой тканью. В отдельных случаях при наличии опухолевого узла имеется выраженное перибронхиальное распространение процесса, при этом стенки бронхов утолщены, белесоваты, просвет их резко сужен. В редких случаях узел макроскопически не выявляется и отмечается только перибронхиальный и периваскулярный разветвленный рост.
Узел мелкоклеточного рака обычно крупный, белесоватый, мясистого вида с обширными некрозами и кровоизлияниями, а иногда с выраженными дегенеративными изменениями, сопровождающимися ослизнением. Располагаясь в зоне крупных бронхов, опухоль обычно окружает их и распространяется вдоль бронха перибронхиально и в подслизистом слое. Крупные опухоли нередко сдавливают просвет бронха, экзофитный компонент, как правило, не выражен.
При периферической локализации рака первичный очаг часто обнаруживается непосредственно под плеврой, а в зоне его роста нередко отмечаются рубцовые изменения. Плевра над опухолью обычно утолщена, отмечается воронкообразное втяжение ее в узел опухоли. Узлы плоскоклеточного и мелкоклеточного рака имеют вид, аналогичный вышеописанным. Аденокарцинома имеет сероватый или темно-серый цвет, может быть мягкой консистенции, ослизненным или различной степени плотности в зависимости от выраженности фиброзных изменений. В крупных новообразованиях встречаются участки некрозов.
Своеобразную макроскопическую картину имеет бронхиолоальвеолярный рак. Узел нечетко отграничен и по цвету часто не отличается от окружающей легочной ткани, некрозы отсутствуют, но в ряде случаев имеются небольшие кисты, выполненные слизью или воздухом, а также прослеживаются неизмененные бронхи. В отдельных случаях определяется несколько узлов различных размеров в пределах одного легкого или его доли.
Keiser и соавт. (1987) путем реконструкции объемной формы опухолевого узла установили, что очаги поражения бывают неправильной причудливой формы с многочисленными кольцевыми выростами (преимущественно при плоскоклеточном раке), эллипсоидной (часто при мелкоклеточном раке), смешенной: эллипсоидной или сфероидальной с несколькими прилежащими к основному узлу дочерними отсевами (обычно при мелкоклеточном и крупноклеточном недифференцированном раке). В очень редких случаях узел имеет форму, приближенную к шаровидной; как правило, это наблюдается при метастатических поражениях легких и при периферическом раке железистого строения.
На практике определение истинного объема опухоли, особенно при центральный локализации, без применения методов реконструкции чрезвычайно затруднительно. Поэтому при морфологической коррекции рентгеноэндоскопических данных особо важное значение придается гистотопографическим взаимоотношениям опухолевого узла с окружающими тканями, так как вовлечение в процесс некоторых анатомических структур легких, даже при небольших размерах узла, усугубляет течение процесса и является прогностически неблагоприятным фактором, что служит основанием для изменения стадии. С этой целью при центральном раке тщательно изучают проксимальные границы поражения бронхов и распространенность обструктивного пневмонита. При субплевральном расположении узла исследованию должна быть подвергнута граничащая с ним висцеральная плевра, а в случае спаяния ее с париетальным листком прилежащие мягкие ткани и экстрапульмональные образования.
Органотропность метастазирования рака легкого не выражена, и отдаленные метастазы могут выявляться в самых неожиданных местах.Мы в своей практике наблюдали метастазирование плоскоклеточного рака в гипернефрому почки и отсев аденокарциномы легкого в зубную лунку премоляра нижней челюсти справа.
С развитием торакальной хирургии особую актуальность приобрела проблема дифференциальной диагностики между первичным периферическим раком легкого и солитарным метастазом злокачественной опухоли в легком. По данным дооперационной морфологии, эта задача может быть решена в отдельных случаях при характерном строении новообразования, свидетельствующем о локализации первичного очага.
Применение иммуногистохимических маркеров расширяет возможности такой диагностики. Согласно данным K.M.Muller (1986), солитарные метастазы чаще поражают нижние доли легких (37%), верхние доли поражаются в 21%. Макроскопическая характеристика метастазов в легком различается по типу их формирования.
2.2 ГИСТОЛОГИЧЕСКИЕ ТИПЫ РАКА ЛЕГКОГО
За 1970-1991 гг. в Российском Научном Центре Рентгенорадиологии обследовали 5772 больных с первичными заболеваниями легких. В 2539 (44%) наблюдениях установлена неопухолевая патология, в 3233 (56%) различные опухоли и опухолевидные процессы.Большую часть (72,9%) онкологических заболеваний легкого представляет рак. Из 2357 больных у 1215 (51,5%) подтвержден плоскоклеточный тип, у 768 (32,6%) — аденокарцинома, у 306 (13%) — мелкоклеточный тип и у 68 (2,9%) другие типы рака.
У 876 (27,1%) больных выявлены относительно редкие новообразования и опухолевидные процессы. Карциноиды диагностированы в 241 (7,4%) наблюдений, опухоли бронхиальных желез — в 203 (6,2%), лимфопролиферативные заболевания — в 129 (4%), неэпителиальные опухоли — в 107 (3,3%), мезотелиомы — в 67 (2%), гамартомы — в 56 (1,7%), папилломы — в 31 (0,9%), остеохондропластическая трахеобронхопатия — в 23 (0,7%), опухоль Абрикосова — в 19 (0,58%).
2.2.1 Плоскоклеточный рак
Плоскоклеточный (эпидермоидный) рак — злокачественная опухоль легкого, имеющая по меньшей мере одно из трех проявлений специфической дифференцировки: индивидуальные признаки кератинизации, формирование роговых жемчужин, наличие хорошо заметных межклеточных мостиков. Выраженность этих признаков является основанием для определения степени дифференцировки опухоли. Плоскоклеточный тип является наиболее часто встречающейся формой рака легкого (до 40%). Отмечено, что на хирургическом материале плоскоклеточный рак выявляется чаще других основных форм — до 71% случаев, а на аутопсийном материале — до 35%.
Цитологическая характеристика. Цитологические проявления плоскоклеточного рака в значительной степени зависят от выраженности в опухоли структурных и клеточных признаков плоскоэпителиальной дифференцировки.К высокодифференцированному плоскоклеточному раку относят новообразования, цитологический материал которых содержит полиморфные опухолевые клетки, имеющие выраженные признаки продукции кератина. В мокроте при этом преобладают элементы из поверхностных отделов опухоли. Это крупные разрозненно лежащие опухолевые клетки, часто располагающиеся по ходу слизистых тяжей среди обильного клеточного и (или) аморфного детрита. Ядра их крупные, гиперхромные, с выраженными признаками альтерации структур ядерного хроматина, кариопикнозом, очагами просветления, кариолизисом.
Следствием этих процессов, протекающих параллельно с накоплением в клетке кератиновых масс, является появление в препарате безъядерных клеток (роговых чешуек). Цитоплазма опухолевых клеток отличается выраженной базофилией, а в отдельных элементах становится очень плотной, стекловидной, по тону и насыщенности окраски иногда сливается с ядром.В бронхоскопическом материале клеточные элементы более сохранны, при этом наибольшую диагностическую значимость имеют зрелые элементы плоскоклеточного рака. Нередко они располагаются параллельными слоями (стратификация), при этом опухолевые клетки уплощенные, вытянутые. Форма их значительно вариабельна. Встречаются клетки овальные, полигональные, лентовидные, булавовидные. В ядрах и цитоплазме выраженные дистрофические изменения, приводящие к появлению базофильного мелкозернистого детрита, нередко занимающие обширные участки.
При трансторакальной пункции очага периферического рака такие участки могут имитировать казеозный некроз. Ошибочное представление о туберкулезном очаге нередко укрепляется вследствие наличия сопутствующей гистиоцитарной реакции с гигантскими многоядерными клетками, сходными с клетками Пирогова-Лангганса. В таких случаях важно определить среди мелкозернистого детрита целые ядра опухолевых клеток и их фрагменты, роговые чешуйки, то есть клеточный характер детрита, что несвойственно туберкулезным очагам.
Сопутствующая клеточная реакция — один из характерных признаков высокодифференцированных форм плоскоклеточного рака. Наиболее часто имеет место реакция нейтрофилов и смешенная нейтрофильно-макрофагальная, реже встречаются лимфоцитарные, плазмоцитарные, гистиоцитарные, эозинофильные клеточные реакции. Для плоскоклеточного рака умеренной дифференцировки характерна выраженная тенденция к формированию обширных пластов. Эта тенденция находит свое отражение и при исследовании мокроты, в которой элементы плоскоклеточного рака умеренной дифференцировки располагаются в виде комплексов. Опухолевые клетки менее полиморфны, чем при высокодифференцированном раке. Они практически однотипны, округлой или полигональной формы с крупным центрально расположенным ядром, нередко содержащим гипертрофированные ядрышки. Цитоплазма базофильна. Характерно наличие в ней мелких группирующихся вакуолей, чаще располагающихся в парануклеарных зонах.
В бронхоскопическом материале между соседними элементами в пластах опухолевых клеток иногда можно видеть межклеточные мостики. В отдельных случаях полиморфизм клеток и их ядер выражен гораздо меньше, чем при высокодифференцированных формах плоскоклеточного рака. Клетки и их ядра имеют округлую форму, признаки ороговения незначительны и выявляются лишь в отдельных элементах. Такие формы умеренно дифференцированного плоскоклеточного рака, в особенности при периферическом его расположении, крайне сложно отличить от умеренно дифференцированной аденокарциномы. Это сходство подчеркивается наличием гипертрофированных ядрышек.
При дифференциальной диагностике необходимо учитывать неправильную форму ядрышек злокачественных клеток, четкую очерченость клеточных границ, удвоение клеточной границы в отдельных элементах, что несвойственно железистому раку.
Прорастание плоскоклеточного рака в плевру нередко сопровождается своеобразными цитологическими изменениями. Новообразование в этих случаях может имитировать мезотелиому и характеризуется наличием крупных, нередко многоядерных опухолевых клеток, появлением в цитоплазме многочисленных крупных вакуолей (гидропическая вакуолизация), пролиферацией мезотелиальных элементов. При развитии плеврита элементы плоскоклеточного рака в жидкости также часто приобретают несвойственные им признаки. Появление многоядерных клеток, гипертрофия ядрышек, увеличение объема цитоплазмы и вакуолизация ее делают невозможной идентификацию гистологического типа рака.
Плоскоклеточный рак низкой дифференцировки — опухоль, склонная к деструктивным изменениям. Мокроте этой формы плоско клеточного рака сопутствует обильное количество клеточного детрита, среди которого могут выявляться небольшие скопления клеток, с трудом идентифицируемые как опухолевые и практически не отличимые от недифференцированного рака. В бронхоскопическом материале низкодифференцированный плоскоклеточный рак представлен округлыми или несколько вытянутыми довольно мономорфными опухолевыми клетками, имеющими более крупные размеры, чем клетки недифференцированного рака.
Ядра клеток крупные, расположены центрально, ядерный хроматин грубозернистый, ободок цитоплазмы узкий. Ядерный хроматин чрезвычайно чувствителен к механическому воздействию и нередко отмечается растяжение его в отдельных «голоядерных» клетках. В этих случаях он приобретает каплевидную форму или встречается в виде тяжей и нитей. Иногда клеточные элементы опухоли отличаются выраженной анаплазией, располагаются разрозненно, ядра обеднены хроматином — такие новообразования трудно дифференцировать от анапластического рака.
Гистологическая характеристика. Дифференцированные формы плоскоклеточного рака легкого обычно представлены ячейками и пластами опухолевых клеток, разделенными в разной степени стромой. В очаге высокодифференцированного плоскоклеточного рака паренхиматозный компонент представлен преимущественно крупными светлыми полигональными клетками, напоминающими элементы шиповатого слоя эпидермиса. Клетки имеют округлые ядра с четко контурированными ядрышками, цитоплазма обильная с различной степенью ацидофилии. Атипические митозы единичны.
Клетки соединяются между собой хорошо различимыми межклеточными мостиками, наличие которых лучше выявляется при использовании зеленого светофильтра. В зоне контакта межклеточных мостиков имеется уплотнение цитоплазмы, межклеточные пространства расширены. В раковых клетках отмечается послойное расположение клеток (стратификация), при этом базальные отделы представлены более мелкими темными клетками с отчетливой полярной ориентацией (анизоморфизмом). При этом отмечаются признаки нарушения чередования слоев с появлением отдельных ороговевающих элементов среди клеток базального и парабазального слоев (дискератоз).
Клеточные элементы с выраженными признаками ороговения характеризуются небольшим пикноморфным ядром и обильной ацидофильной цитоплазмой. Характерно формирование концентрических напластований шиповатых клеток, уплощающихся к центру, с нарастающими признаками ороговения, роговых жемчужин. Встречаются также жемчужины с неполной кератинизацией и скопления кератина в виде гомогенных масс, а в отдельных участках — группы ороговевших клеток, которые не формируют комплексы и располагаются изолированно.
Для умеренно дифференцированного плоскоклеточного рака характерно наличие более обширных пластов и тяжей из крупных полиморфных клеток типа шиповатых с большим округлым ядром. Встречаются митозы. Признаки стратификации в пластах сохраняются, а периферические отделы представлены более мелкими базальными клетками с анизоморфным их расположением. В отдельных пластах клеточные элементы типа базальных преобладают над шиповатыми в зоне инфильтрирующего роста. Процессы ороговения выражены слабее, но сохраняются признаки дискератоза. Наблюдается формирование жемчужин, однако полного ороговения в них не происходит. В таких опухолях, как правило, встречаются и более дифференцированные участки с отчетливо выраженным признаками ороговения. Опухоль оценивается как умеренно дифференцированный плоскоклеточный рак в случае, когда дифференцированные участки занимают в общем объеме менее 50%.
Недифференцированный плоскоклеточный рак представлен малодифференцированными клетками небольших размеров, отличающимися выраженным полиморфизмом. Клетки имеют полигональную, овальную или вытянутую форму, ядра их округлые или вытянутые. Отмечается большое количество патологических митозов. Злокачественные клетки растут в виде пластов, по периферии которых может наблюдаться полярная ориентация опухолевых элементов. Межклеточные мостики, как правило, не обнаруживаются, однако могут встречаться отдельные клетки с признаками ороговения, лучше выявляющиеся с помощью окраски по Крейбергу. В отдельных пластах имеются признаки стратификации. В новообразованиях этой группы часто встречаются деструктивные изменения: кровоизлияния, обширные поля некрозов.Среди вариантов строения плоскоклеточного рака следует отметить веретеноклеточный плоскоклеточный рак и плоскоклеточный рак типа светлоклеточного.
Веретеноклеточный (плоскоклеточный) рак встречается как компонент плоскоклеточного рака, но обычно опухоли, имеющие веретеноклеточное строение, растут в виде полипа (И.Г.Ольховская, 1982). При этом участки типично плоскоклеточного рака могут не обнаруживаться, и опухоль, вследствие выраженного клеточного полиморфизма и большого количества патологических митозов, может имитировать саркому. В таких случаях следует учитывать макроскопический вид опухоли и применять дополнительные методы исследования (электронная микроскопия) для подтверждения эпителиальной природы новообразования.
Плоскоклеточный рак светлоклеточного типа при светооптическом исследовании напоминает метастаз гипернефромы. Клетки растут в виде пластов, имеют относительно мелкие центрально расположенные ядра и обильную оптически пустую цитоплазму. Большое значение для дифференциальной диагностики этих опухолей имеет электронная микроскопия, выявляющая признаки плоскоклеточной дифференцировки (тонофиламенты).
Выраженность инфильтрирующего роста плоскоклеточного рака зависит от длительности существования опухоли и степени ее дифференцировки. Этот тип рака может прорастать в лимфатические узлы, крупные сосуды, а также сливаться с метастатическими узлами, образуя единый конгломерат. Распространение опухоли происходит как путем простого прорастания в соседние ткани, так и по сосудам перибронхиальной лимфатической сети. Периферические отделы плоскоклеточного рака характеризуются отсевами, располагающимися рядом или на некотором отдалении от опухоли, придающим узлу причудливую форму и выявляющимися на рентгенограммах в виде спикул различной ширины и протяженности.
Высокодифференцированные подтипы плоскоклеточного рака характеризуются хорошо развитой стромой, нередко с признаками выраженной коллагенизации и образованием бесклеточных участков (десмопластическая реакция). Иногда среди обширных полей встречаются как бы замурованные в ней небольшие раковые альвеолы, клеточные элементы которых имеют выраженные дистрофические изменения.Одним из характерных признаков плоскоклеточного рака легкого является сопутствующая воспалительная реакция, проявляющаяся в виде преимущественно лейкоцитарной и (или) лимфоидноклеточной инфильтрации стромы. В зоне дистрофических или деструктивных изменений нередко обнаруживаются гигантские многоядерные клетки типа инородных тел. Центральному раку нередко сопутствуют вторичные легочные изменения в виде ателектазов, бронхоэктазов, абсцессов, параканкрозных пневмоний, а также эндобронхиты. Наряду с наличием основного узла опухоли, в пораженном и соседних бронхах обнаруживаются участки плоскоклеточной метаплазии, иногда с формированием в этих зонах очагов рака.
Ультраструктура. Опухоль имеет строение, аналогичное плоскоклеточному раку других локализаций, то есть содержит все признаки плоского эпителия: филаменты, тонофибриллы, десмосомы, фрагменты базальной мембраны.При высокодифференцированном плоскоклеточном раке преобладают пласты крупных дифференцированных клеток, содержащих грубые пучки тонофиламентов и хорошо развитые десмосомы. Клетки полигональной формы с крупными овальными или округлыми ядрами. Цитоплазма обильная, содержит рибосомы и полисомы, митохондрии, профили шероховатого и гладкого эндоплазматического ретикулума.
При умеренно дифференцированном раке также преобладают крупные полигональные клетки с гладкой цитолеммой, плотно примыкающие друг к другу, контактирующие посредством хорошо развитых десмосом. Цитоплазма клеток хорошо развита, количество филаментов и тонофибрилл в различных клетках варьирует, однако в целом их меньше, чем в высокодифференцированном раке. Наряду с плоскоклеточной дифференцировкой, в умеренно дифференцированном плоскоклеточном раке могут встречаться клетки с признаками железистой дифференцировки: между соседними клетками образуются просветы с обращенными в них микроворсинками, в отдельных клетках встречаются серозные секреторные гранулы.
Для низкодифференцированного плоскоклеточного рака характерно преобладание мелких клеток. Ядра овальные, с инвагинациями, хроматин крупноглыбчатый. В цитоплазме преобладают рибосомы и полисомы, другие органеллы развиты слабо. Тонофиламенты представлены небольшими разрозненными пучками. Сохраняются только отдельные десмосомальные контакты.
2.2.2. Мелкоклеточный рак
В гистологической классификации опухолей легких ВОЗ (1981) мелкоклеточный рак представлен тремя вариантами: овсяноклеточный рак, рак из клеток промежуточного типа и комбинированный овсяноклеточный рак. Мелкоклеточный тип составляет от 20 до 25% всех эпителиальных новообразований легкого и является высокозлокачественной опухолью, состоящей из мелких довольно однотипных клеток со скудной цитоплазмой и нежным диффузно распределенным по всему ядру хроматином, иногда выявляются гипертрофированные ядрышки.
Как правило, при светооптическом исследовании в опухолевых клетках не выявляются какие-либо признаки дифференцировки, хотя при электронной микроскопии в отдельных случаях обнаруживаются единичные или небольшие группы клеток, имеющих признаки плоскоэпителиальной или железистой дифференцировок. Эта группа опухолей характеризуется также продукцией различных гормонов, таких как АКТГ, серотонин, антидиуретический гормон, кальцитонин, соматотропный гормон, меланоцитостимулирующий гормон, эстрогены.В последние годы в литературе особенно подчеркивается, что группа мелкоклеточного рака неоднородна и представлена вариантами, различающимися по характеру роста, антигенному составу, продукции биомаркеров, цитогенетическими признаками, экспрессией и амплификацией онкогенов, различной чувствительностью к противоопухолевой терапии. Наиболее общим и характерным биологическим признаком является продукция в клетках 4 маркеров, два из которых являются ферментами APUD-системы (L-ДОФА-декарбоксилаза, нейронспецифическая енолаза), остальные — пептидный гормон бомбезин (гастрин-рилизинг пептид) и ВВ изоэнзим креатин-киназы.
Мелкоклеточный рак отличается выраженной склонностью к метастазированию уже на ранних стадиях развития опухоли, плохим прогнозом и малой продолжительностью жизни больных.
Таким образом, мелкоклеточный рак легкого характеризуется наличием следующих основных признаков: мелкие размеры клеток, отсутствие светооптических признаков дифференцировки, быстрый рост, раннее и обширное метастазирование, высокая чувствительность к специфической терапии, наличие специфических биомаркеров, продукция различных гормонов. Первые пять признаков отличают мелкоклеточный рак легкого от гормонпродуцирующих немелкоклеточных типов рака легкого и карциноидов.
В настоящее время существуют две точки зрения относительно гистогенеза мелкоклеточного рака легкого.Согласно первой гипотезе мелкоклеточный рак легкого развивается из клеток диффузной эндокринной системы (APUD-системы), которые в эмбриональном периоде мигрируют в легкие из неврального гребешка.
Вторая гипотеза утверждает, что эта группа опухолей возникает из клеток бронхиальной выстилки, имеющих энтодермальное происхождение и обладающих теми же морфологическими и биохимическими признаками, что и клетки мелкоклеточного рака.
Сторонники первой точки зрения обосновывают свою гипотезу тем, что в элементах мелкоклеточного рака легкого обнаруживают морфологические структуры (нейроэндокринные гранулы размерами от 50 до 500 нм), а также биохимические маркеры, свойственные клеточным элементам APUD-системы, происхождение которых связывают с невральным гребешком. У человека доказано наличие таких клеток в бронхиальных железах, крупных бронхах и бронхиолах. Эти данные обусловили широкое распространение мнения о том, что мелкоклеточный рак легкого относится к опухолям APUD-системы и является крайне агрессивной разновидностью злокачественного карциноида. При этом постулируется, что нейроэндокринная дифференцировка присуща только клеткам — производным неврального гребешка.
Сторонники второй гипотезы полагают, что мелкоклеточный рак легкого, также как и другие гистологические типы, развивается из клеток энтодермального происхождения. Эта гипотеза подтверждается наличием в элементах мелкоклеточного рака легкого общих признаков, свойственных всем гистологическим типам, отличием мелкоклеточного рака легкого от других нейроэндокринных новообразований. Кроме того, экспериментальные данные свидетельствуют о том, что признаки нейроэндокринной дифференцировки могут быть присущи и клеточным элементам, имеющим энтодермальное происхождение.
В последние годы в ряде экспериментальных работ было показано, что энтерохромаффинные клетки желудочно-кишечного тракта, островковые клетки поджелудочной железы, ранее рассматривающиеся как производные нейроэктодермы, на самом деле имеют энтодермальное происхождение — общее с другими эпителиальными элементами этих систем.
В настоящее время считается, что APUD-клетки желудочно-кишечного тракта не являются производными неврального гребешка. Пока мы не располагаем убедительными данными относительно миграции клеток неврального гребешка в легкие. В то же время нейроэндокринные гранулы нередко обнаруживаются в слизепродуцирующих клетках нормальной бронхиальной выстилки. Однако полностью отрицать возможность миграции элементов нейроэктодермы в легкие нельзя, так как в пользу этого свидетельствует развитие в легких такой опухоли, как меланома.
К перечисленным фактам следует добавить, что мелкоклеточный рак легкого существенно отличается от карциноида ( в том числе, от его атипической разновидности) этиологическими факторами ( курение, лучевое воздействие, воздействие хлор-метил-метилового эфира). Нередко при мелкоклеточном раке легкого опухолевые элементы с нейроэндокринной дифференцировкой сочетаются с неэндокринными злокачественными клетками с признаками плоскоэпителиальной или железистой дифференцировки (G.Saccomаno et al.,1974). Такая гетерогенность может свидетельствовать о наличии для всех типов рака легкого единой стволовой клетки (A.Gazdar et al.,1985).В то же время для опухолей APUD-системы гетерогенность не характерна. Мелкоклеточный рак легкого обычно не встречается как проявление синдрома множественной эндокринной неоплазии. Что касается морфологического сходства мелкоклеточного рака легкого с другими опухолями APUD-системы, то нейроэндокринные гранулы выявляются также в небольшом количестве опухолевых клеток немелкоклеточного рака легкого, количество гранул в клетках мелкоклеточного типа меньше и они имеют небольшие размеры. Важно подчеркнуть, что клеточные элементы многих опухолей, расцениваемых клинически и морфологически как мелкоклеточный рак легкого, вообще не содержат нейросекреторных гранул, а имеют хорошо развитые десмосомы и тонофиламенты, то есть, по сути дела, являются низкодифференцированными плоскоклеточными формами рака (Mackay и соавт.,1977). Помимо этого показано, что секреция гормонов присуща не только мелкоклеточному, но и другим типам рака легкого.
Таким образом, достаточно убедительных данных, свидетельствующих о приоритете первой или второй гипотезы, в настоящее время не имеется. В связи с этим, следует рассматривать мелкоклеточный рак легкого как разновидность бронхогенного рака, происходящую из бронхиального эпителия, но имеющую биохимические и ультраструктурные признаки, сходные с опухолями APUD-системы.
Цитологическая характеристика. При исследовании мокроты наиболее характерным цитологическим признаком мелкоклеточного рака является небольшой размер опухолевых клеток (примерно в 1,5-2 раза крупнее лимфоцита), располагающихся либо в виде массивных скоплений, либо цепочками («гуськом») по ходу тяжей слизи. В бронхоскопическом материале часто обнаруживаются своеобразные гроздевидные скопления опухолевых клеток. Ядра клеток округлые, овальные, полулунные или неправильной треугольной формы с наличием уплощений или вдавлений на соприкасающихся поверхностях соседних клеток, обозначаемых «фасетками» или «конгруэнтными площадками». Этот признак можно считать патогномоничным для мелкоклеточного рака.
Важно отметить, что применение различных красителей (тканевых или гематологических) дает различные результаты окраски ядерного хроматина. При окраске по методу Папаниколау (или его модификаций) ядра элементов мелкоклеточного рака гиперхромные с сетчатым или грубозернистым хроматином. При окраске по методу Паппенгейма хроматин в ядрах представляется тонкодисперсным,ядра бледные, оптически пустые. Именно этот признак позволяет достоверно отличить данную опухоль от низкодифференцированного плоскоклеточного рака. Ободок цитоплазмы очень узкий, в большинстве опухолевых клеток практически не выявляется. Особые трудности возникают при дифференциальной диагностике этой формы рака с лимфобластным вариантом лимфосаркомы в случаях, когда имеет место метастатическое поражение лимфатических узлов средостения без выявленного в легких первичного очага.
Другим вариантом мелкоклеточного рака является рак из клеток промежуточного типа. Мы диагностируем этот вариант, когда материал представлен анаплазированными опухолевыми клетками, ядра которых по размеру приблизительно равны ядрам овсяноклеточного рака, но хроматин более компактный, гранулярный или тяжистый, а ободок цитоплазмы довольно широкий. В клетках этой опухоли, как правило, большое количество патологических митозов, что отличает ее от низкодифференцированного плоскоклеточного рака. Следует подчеркнуть, что в метастатически пораженных лимфатических узлах средостения при овсяноклеточном раке нередко обнаруживаются участки рака, состоящие исключительно из клеток промежуточного типа.
Цитологическая характеристика комбинированного овсяноклеточного рака основывается на одновременном присутствии признаков, характерных для овсяноклеточного рака и плоскоклеточного рака или аденокарциномы.
Гистологическая характеристика. Овсяноклеточный рак состоит из довольно мономорфных, небольших по размеру клеток округлой, полигональной или вытянутой формы. Однако может иметь место умеренный полиморфизм в размерах и форме клеток. Как правило, клетки в два раза крупнее лимфоцита, содержат центрально расположенное ядро с тонкодисперсным хроматином и непостоянными ядрышками. Отдельные клетки имеют более плотные гиперхромные ядра, особенно в полях с дегенеративными и некротическими изменениями. Цитоплазма скудная, обычно базофильная. Несмотря на быстрый рост опухоли, митозы выявляются редко.Клеточные элементы располагаются, как правило, рыхло, строма скудная, отсутствует лимфоцитарная или другая воспалительная инфильтрация, даже в областях с некротическими изменениями. Обычно опухоль растет в виде широких тяжей, в отдельных участках отмечается наличие трабекулярных, альвеолярных структур или палисадообразно расположенных клеток вокруг нежных кровеносных сосудов — псевдорозетки. Некротические и дегенеративные изменения в опухоли имеют характерный вид: вдоль стенок сосудов и других соединительнотканных структур отмечается накопление базофильного вещества вследствие отложения ядерного материала, что не встречается в других типах рака легкого и карциноидах.
Рак из клеток промежуточного типа представлен довольно полиморфными опухолевыми элементами полигональной или веретенообразной формы, более крупными, чем при классическом мелкоклеточном раке, размеры клеток в три раза больше лимфоцита. Ядра этих клеток содержат заметное количество глыбок хроматина и непостоянные ядрышки. Часть клеток имеет скудную цитоплазму, в других отмечается более выраженная нежнобазофильная или светооптически прозрачная цитоплазма. В клетках этого типа отмечается выраженная митотическая активность.
В отдельных новообразованиях, наряду с мелкоклеточным раком, могут выявляться участки, где опухолевые элементы имеют строение плоскоклеточного или железистого рака различной дифференцировки комбинированный овсяноклеточный рак.
Наибольшие трудности в дифференциальной диагностике мелкоклеточного рака легкого с другими гистологическими типами возникают при оценке материала бронхобиопсии, где опухолевые элементы вследствие большой чувствительности к механическому воздействию могут быть сильно разрушены и напоминать лимфоцитарные скопления или воспалительную инфильтрацию. Особые трудности возникают при дифференциальной диагностике мелкоклеточного рака легкого с атипическим карциноидом и другими малодифференцированными формами бронхогенного рака.
Наиболее часто мелкоклеточный рак приходится дифференцировать с низкодифференцированным плоскоклеточным раком, клетки которого, как правило, имеют обильную четко очерченную цитоплазму. С помощью зеленого светофильтра в отдельных участках можно выявить и межклеточные мостики. Ядра более гиперхромные, а цитоплазма эозинофильная, что указывает на эпидермоидную дифференцировку. В отдельных же случаях без применения специальных методов исследования дифференциальный диагноз мелкоклеточного рака легкого с другими микроскопически сходными опухолями практически невозможен. Ультраструктура. Выявляются мелкие округлые, овальные или вытянутые клетки,лежащие отдельно или мелкими группами в коллагенволокнистой строме. Ядра неправильной формы с крупноглыбчатым хроматином. Цитоплазма скудная с небольшим количеством органелл (рибосомы, полисомы, мелкие митохондрии, короткие профили ШЭР) и единичными округлыми или полиморфными нейросекреторными гранулами. Единичные нейросекреторные гранулы могут встречаться в немелкоклеточных типах рака, состоящего преимущественно из более крупных недифференцированных клеток и элементов со слабыми признаками железистой дифференцировки (микроворсинки). Цитоплазма в этих клетках более обильная, содержит рибосомы, полисомы, митохондрии, множественные профили шероховатого и гладкого эндоплазматического ретикулума.
Клеточные элементы опухоли этого типа формируют тубулярные, ацинарные или папиллярные структуры. Одной из характерных особенностей злокачественных клеток является также способность к продукции слизи, более или менее хорошо выраженная. Однако в части новообразований слизистая секреция не выявляется. При определении степени дифференцировки аденокарциномы учитывается степень выраженности тубулярных, ацинарных или сосочковых структур, при этом характер и объем слизистой секреции могут быть различны.
Опухоли, формирующие тубулярные, ацинарные или сосочковые структуры практически во всем объеме, относятся к умеренно или высокодифференцированным подтипам аденокарциномы. Солидные образования, построенные из крупных клеток и формирующие немногочисленные ацинарные структуры, должны рассматриваться как низкодифференцированная аденокарцинома. К этой же категории относятся новообразования из крупных клеток с небольшим количеством внутриклеточной слизи, ранее рассматривавшиеся как крупноклеточный недифференцированный рак.
Аденокарцинома обнаруживается в 20-25% всех случаев рака легкого и составляет наибольшую часть очагов поражения паренхимы легкого (периферический рак). Наиболее ранние исследования J.Walter и D. Pryce (1955) показали, что аденокарцинома составляет 40% случаев периферической локализации и обычно не встречается в крупных бронхах. Jackman и соавт. (1969) подтвердили железистый рак у 49% больных с периферическими солитарными узлами в легких, среди них 71% — женщины.
A.Gazdar (1986), исследовав большую группу больных немелкоклеточным раком, в том числе и аденокарциномой, отметил выраженную гетерогенность этих новообразований с наличием более чем 12 клеточных фенотипов, большинство из которых являются дериватами метаплазированного слизесекретирующего бронхиального эпителия, часть происходит из клеток Клара и отдельные из пневмоцитов II типа.Предопухолевые состояния и ранние стадии развития аденокарцином еще плохо изучены. Ряд авторов предполагают наличие патогенетической связи между развитием аденокарциномы и рубцовыми изменениями в легких. По данным разных авторов, такая связь при периферическом раке легкого наблюдается в 15-20% случаев (Auerbach и соавт.,1979) до 80-95% (У.А.Коган и соавт.,1988; R. Haupt, 1973), причем чаще при аденокарциноме. Этот феномен был впервые описан G.Friedrich в 1939 году, а P. Rossle (1943) обозначил эту патологию как «narbenkrebs» — рак в рубце («sсar carcinoma» по английской терминологии). Происхождение рубцовых изменений, связанных с опухолью, может быть различным и обусловленным последствиями туберкулеза, инфаркта, пневмокониоза, хронического пневмонита, фиброзирующего альвеолита и т.д.
При исследовании небольших очагов поражения отмечено, что рак локализуется вначале по периферии рубца. M. Raeburn и H. Spencer (1953) предположили, что источником развития опухоли является регенераторный эпителий на границе поврежденного и интактного легкого, подвергающийся метапластическим и диспластическим изменениям. Эта точка зрения имеет большое количество сторонников и в настоящее время. В последние годы гипотеза «рака в рубце» подвергнута критической ревизии. Показано, что рубец, ассоциирующийся с раком, может быть следствием десмопластической реакции на опухоль.
S.A.Barsky и соавт. (1986) изучили рубцовые изменения, связанные с опухолью, и склеротические изменения методом экстракции коллагена, ультраструктурного и иммуноцитохимического анализа для идентификации межклеточного вещества с целью уточнения генеза соединительной ткани. Эти исследования выявили существенные различия в клеточном и биохимическом компонентах. Так, для «рака в рубце» характерно большое количество миофибробластов, составляющее более 40% клеток стромы, высокий относительно уровень коллагена типа Y. Эти параметры идентичны со скирром молочной железы и коррелируют с длительностью существования опухоли.
В то же время в зрелых рубцах количество миофибробластов не велико (0-10%), отмечается низкий относительный уровень коллагена типа Y, что свидетельствует о длительном существовании рубца. Эти данные хотя и не позволяют опровергнуть гипотезу «рака в рубце», в большой степени подтверждают вторичный характер рубцовых изменений в легких.
Цитологическая характеристика. Группа железистого рака легкого наиболее вариабельна в цитологических проявлениях. Важно отметить, что цитологическую картину аденокарциномы могут имитировать различные патологические состояния, стимулирующие гиперплазию и гипертрофию клеток бронхиального эпителия.К наиболее характерным признакам аденокарциномы легкого, отражающим особенности железистой дифференцировки, относятся следующие: расположение клеток в виде ацинарных, тубулярных и сосочковых структур; базальное расположение клеточных ядер, отражающее полярную дифференцировку клеток; слизистая секреция. Следует отметить,что все эти признаки в большей степени характерны для высокодифференцированных подтипов рака. Со снижением степени дифференцировки возможности достоверной цитологической верификации типа опухоли существенно уменьшаются.
Высокодифференцированная аденокарцинома (ацинарный тип). При исследовании мокроты клеточные элементы высокодифференцированной аденокарциномы ацинарного типа по сравнению с плоскоклеточным раком менее полиморфны. Выявляются комплексы из довольно крупных, рыхло расположенных, практически однотипных по величине клеток, формирующих железистоподобные структуры. Клетки чаще имеют округлую форму, ядра также округлые, расположены эксцентрично, обильная цитоплазма нередко вакуолизирована. Характерно, что фон мазка более «чистый», чем при плоскоклеточном раке. Сопутствующая клеточная реакция, как правило, не выражена.
В материале, полученном при инструментальных методах исследованиях, можно выявить более тонкие детали строения высокодифференцированной аденокарциномы. Опухолевые клетки чаще располагаются в виде комплексов, реже одиночно. Форма клеток вариабельна, нередко даже в пределах одной опухоли. Преобладают округлые и призматические клетки, но встречаются и опухоли с клетками цилиндрической формы, напоминающими бокаловидные.
Ядра с равномерно распределенным мелкозернистым хроматином и крупными четко очерченными ядрышками, часто встречаются двуядерные клетки. В отличие от плоскоклеточного рака, в хорошо сохранившихся злокачественных клетках, как правило, не отмечается маргинация хроматина, контур ядерной мембраны ровный. Цитоплазма в клетках высокодифференцированной аденокарциномы обширная, отличается меньшей плотностью и менее гомогенная, чем при плоскоклеточном раке. Края цитоплазмы нечетко очерчены, иногда волнистые, с наличием на поверхности внеклеточной слизи.
Межклеточные границы плохо различимы. Цвет цитоплазмы при использовании гематологических красителей, как правило, базофильный, но в отдельных случаях при диффузном распределении слизи в цитоплазме последняя может приобретать оксифильную окраску. Внутриклеточная слизь может воспринимать как базофильную, так и оксифильную окраску. В одних случаях она встречается в виде гранул и скоплений, имеющих тенденцию к накоплению в апикальной части цитоплазмы, в других — слизистая секреция проявляется в виде мелких или крупных вакуолей, придающих цитоплазме пенистый вид. Следует подчеркнуть, однако, что выраженные признаки слизистой секреции не характерны для высокодифференцированных аденокарцином.
Умеренно дифференцированный подтип аденокарциномы практически никогда уверенно не подтверждается. В большинстве случаев трудности возникают и при исследовании материала, полученного инструментальным путем. Элементы опухоли располагаются в виде комплексов, имитирующих структурную организацию плоскоклеточного рака. Опухолевые клетки округлой формы с крупными округлыми ядрами. Сходство с плоскоклеточным раком усиливается тем, что при снижении степени дифференцировки цитоплазма злокачественных клеток приобретает интенсивную базофильную окраску, степень насыщенности которой особенно усиливается при деструктивных изменениях в опухоли.
Тем не менее, некоторые характерные признаки позволяют провести дифференциальную диагностику. В комплексах умеренно дифференцированной аденокарциномы, как правило, обнаруживаются двуядерные клетки. Ядерный хроматин грубозернистый, но маргинальная конденсация его выражена в значительно меньшей степени, чем при плоскоклеточном раке и обычно соответствует деструктивным изменениям в опухоли. Ядрышки крупные, нередко множественные, четкие, имеют правильную округлую форму. Края цитоплазмы четкие, но межклеточные границы плохо различимы.
С наибольшей уверенностью умеренно дифференцированная аденокарцинома легкого диагностируется в тех случаях, когда имеют место признаки слизистой секреции, иногда интенсивно выраженной. В этих случаях округлые, однотипные («штампованные») клетки, формирующие массивные пласты, содержат большое количество внутриклеточной и внеклеточной слизи. В нашей практике имели также место случаи, когда слизепродуцирующие умеренно дифференцированные подтипы аденокарциномы содержали клетки типа перстневидных. Эти клетки имеют овальной или бобовидной формы смещенное к периферии ядро и крупную, заполненную оксифильной или базофильной слизью, вакуоль. Слизь компактная, гомогенная, что отличает эту опухоль от метастазов перстневидноклеточного рака желудка, где слизь в вакуолях, как правило, хлопьевидная, либо отмечается наличие прозрачной вакуоли.
Папиллярная аденокарцинома распознается в тех случаях, когда в мокроте или материале, полученном инструментальным путем, обнаруживаются сосочковые структуры. Злокачественные клетки, формирующие сосочки, как правило, имеют различные размеры, и в одних и тех же структурах выявляются более крупные и более мелкие элементы, что отражает многоядерный характер сосочков. Весьма характерно наличие округлых мелких гиперхромных клеток по соседству с гораздо более крупными.
Клеточные элементы папиллярной аденокарциномы и их ядра имеют округлую форму. Ядерный хроматин грубозернистый с участками маргинальной конденсации, границы ядерной мембраны четкие. Объем цитоплазмы может быть различным, но, как правило, небольшой. В более мелких клетках ядра и цитоплазма интенсивно базофильные, в более крупных различной степени базофилии. В опухолях смешанного строения (ацинарно-сосочковых), наряду с папиллярными структурами, иногда встречаются более крупные слизепродуцирующие клетки.
Гистологическая характеристика. Аденокарциномы отличаются выраженной вариабельностью строения, нередко в пределах одной опухоли. Для всех опухолей этой группы, за исключением бронхиолоальвеолярного рака, чрезвычайно характерна десмопластическая реакция.
Высокодифференцированные новообразования состоят из крупных цилиндрических, призматических или кубических клеток, формирующих тубулярные, ацинарные, сосочковые или смешанные структуры. В тубулярных и ацинарных структурах клетки обычно имеют полярное расположение ядер. Ядра клеток крупные, светлые, округлые или несколько вытянутые, содержат гипертрофированные ядрышки. Цитоплазма светло окрашенная, содержит вариабельное количество слизи. В отдельных случаях имеет место избыточная секреция слизи и в опухоли встречается большое количество клеток типа перстневидных. В периферических отделах опухоли клетки могут расти вдоль межальвеолярных перегородок, имитируя бронхиолоальвеолярный рак.
Папиллярный подтип аденокарциномы формирует крупные сосочки, строма которых нередко избыточно развита, местами гиалинизирована. Выстилка сосочков в большинстве участков многорядная. Характерна склонность опухолевых клеток к расположению в виде трехмерных групп с общими границами. Возможно наличие в таких опухолях псаммомных телец.
Умеренно дифференцированная аденокарцинома характеризуются обширными участками солидного строения. Клетки в этих участках округлой или полигональной формы, имеют меньшие размеры и более мономорфны, чем злокачественные элементы ацинарных и папиллярных структур. Ядра клеток округлые, нередко гиперхромные, цитоплазма хорошо выражена, в отдельных случаях содержит небольшое количество слизистых вакуолей. Характерно заметное учащение митозов.
Низкодифференцированная аденокарцинома — опухоль преимущественно солидного строения. В отдельных случаях такие опухоли состоят из крупных клеток с обильной секретирующей слизь цитоплазмой — солидный рак с образованием слизи. Наличие признаков слизистой секреции, иногда слабо выраженной, позволяет отличить эту разновидность от крупноклеточного недифференцированного рака.
Ультраструктурная характеристика. Организация аденокарциномы легкого отличается большим разнообразием, обусловленным различными типами клеток бронхиального эпителия и дифференцировкой злокачественных клеток в том или ином направлении. В одной опухоли могут встречаться как недифференцированные элементы, так и клетки с одной, двумя и более типами дифференцировки в различных сочетаниях.Дифференцировка в сторону реснитчатых клеток характеризуется группами клеток, располагающихся в один или несколько рядов на базальной мембране и образующих широкие слизистые просветы. Поверхности клеток, обращенные в просвет, покрыты множественными различной величины и формы ресничками и микроворсинками. Цитоплазма клеток развита умеренно, содержит рибосомы и полисомы, митохондрии, короткие профили шероховатого и гладкого эндоплазматического ретикулума. Секреторные гранулы, как правило, не определяются.
Дифференцировка в сторону бокаловидных клеток характеризуется слизистой секрецией: большая часть их цитоплазмы заполнена крупными, оптически светлыми гомогенными или мелкозернистыми слизистыми гранулами. Ядра в этих клетках оттиснены к периферии, нередко неправильной формы из-за вдавлений. Свободные участки цитоплазмы выглядят темными, содержат большое количество рибосом, профилей шероховатого эндоплазматического ретикулума, митохондрии. Плазмолемма, как правило, гладкая. На участках, обращенных в железистые просветы, имеются отдельные микроворсинки.
Дифференцировка в сторону секреторных клеток: комплексы клеток, окруженных базальной мембраной, контактирующих между собой посредством десмосом, ограничивают межклеточные просветы. Поверхность клеток, обращенная в эти просветы, покрыта микроворсинками. Ядра клеток округлой формы, нередко с инвагинациями, содержат одно или два крупных ядрышка. Цитоплазма хорошо развита, содержит большое количество органелл, а также то или иное количество секреторных гранул, окаймленных однослойной мембраной, с матриксом различной плотности. Гранулы скапливаются в апикальной части клеток. Дифференцировка в сторону пневмоцитов II типа: в цитоплазме этих клеток содержатся различных размеров и формы осмиофильные тельца. Цитоплазма хорошо развита, содержит профили шероховатого эндоплазматического ретикулума, много митохондрий. На поверхности, обращенной в просвет, образуется большое количество развитых микроворсинок.
При высокодифференцированной аденокарциноме железистые просветы широкие, клетки, образующие просвет, упорядоченно располагаются на базальной мембране. Злокачественные клетки образуют солидные поля. Межклеточные просветы узкие, неправильной формы, могут определяться мелкие внутриклеточные железистые просветы. Чаще встречаются клетки неправильной формы с изрезанными ядрами и многоядерные клетки.
Низкодифференцированный рак с железистой дифференцировкой представлен полями мелких клеток с крупными неправильной формы ядрами с одним или несколькими гипертрофированными ядрышками.
Цитоплазма развита в различной степени, чаще слабо. Количество органелл обычно небольшое. В отдельных клетках могут встречаться мелкие секреторные гранулы или осмиофильные тельца, щелевидные железистые просветы с единичными микроворсинками.
Псевдомезотелиоматозная аденокарцинома .легкого проявляется значительным утолщением плевры. Обычно нет указаний на воздействие асбеста в анамнезе. Клиническая симптоматика и течение также напоминает мезотелиому.Макроскопически определяются сероватые фиброзные ткани, заполняющие плевральную полость, однако гистологически опухоль представляет собой несомненную аденокарциному. Злокачественные клетки диффузно распространяются по поверхности плевры.
При плевральной пункции определяются многочисленные круглые клетки с макроядрышками, располагающиеся в виде сосочковых пластов, поэтому этот тип аденокарциномы необходимо дифференцировать с мезотелиомой по данным биопсии, не полагаясь на цитологическое исследование. Бронхиолоальвеолярный рак: опухоль обычно локализуется вне макроскопически видимых бронхов, в периферических отделах паренхимы легких. Клеточные элементы растут вдоль стенок альвеол, используя их в качестве стромы с сохранением альвеолярного рисунка.
Цитологическая характеристика опухолевых клеток может быть различной. Опухоль встречается в локализованной или диффузной форме. Часто сочетается с рубцами (в 25-50% по данным разных авторов). Первое описание этой разновидности рака легкого принадлежит L.Malassez (1876), который дал морфологическую характеристику двух вариантов роста опухоли: фокального и мультилобулярного. Masser (1903) и Ravenna (1909) описали пневмониеподобный вариант строения.
В гистологической классификации опухолей легких ВОЗ (второе издание,1981) бронхиолоальвеолярный рак рассматривается как высокодиффернцированная аденокарцинома. Отдельные авторы (C.Тао и соавт.,1978) на основании цитологической характеристики опухолевых элементов выделяют секретирующие, несекретирующие и малодифференцированные варианты бронхиолоальвеолярного рака. Известно, что при солитарных узлах опухоли из секретирующих или несекретирующих слизь клеток отмечается хороший прогноз, у больных с мультицентрической формой — наихудший.
Наиболее злокачественны солитарная и мультицентрическая формы бронхиолоальвеолярного рака, состоящие из малодифференцированных клеток. Другие авторы (J. T. Manning и соавт.,1984) как неблагоприятные факторы прогноза рассматривают выраженную слизистую секрецию в опухолевых клетках и наличие комплексов злокачественных клеток в просветах альвеол вне основного узла, что расценивается как аэрогенная диссеминация. В то же время Clayton и соавт. (1986) полагают, что вид опухолевых клеток не имеет значения для прогноза и неблагоприятным прогностическим фактором являются только признаки аэрогенной диссеминации.
Заболеваемость бронхиолоальвеолярным раком по данным разных авторов различна — от 1,1 до 9% (F. Edgerton и соавт.,1981) всех случаев рак легкого, что отражает нечеткую очерченность на сегодняшний день критериев морфологической диагностики данной патологии. Фенотипическая характеристика клеточных элементов бронхиолоальвеолярного рака сходна с таковыми в других подтипах аденокарциномы легкого. структуры, очертаний бронхиолоальвеолярного рака.
Опухоль отличается медленными темпами роста: время удвоения ее объема составляет 350-300 дней. Узел, как правило, располагается в субплевральных отделах легких. Форма небольшого очага нередко полигональная, звездчатая. Контуры опухоли обычно неровные, с тяжами по периферии, более широкими в направлении к костальной плевре. Отчетливо прослеживаются неизмененные бронхиальные ветви на всем протяжении: от корня до края опухоли и нередко на ее фоне.
Проведенные рентгено-морфологические сопоставления показали, что характерные для бронхиолоальвеолярного рака просветления связаны не с деструкцией опухоли, а с наличием в новообразовании отдельных непораженных участков легочной ткани, с формированием полостей, выполненных воздухом и слизью, пересеченных утолщенными альвеолярными перегородками. Более мелкие просветления являются отображением поперечных сечений интактных бронхиол и мелких бронхов.
Неровность и тяжистая деформация контуров объясняется более активным ростом опухоли по периферии, с распространением в окружающую ткань по тонким альвеолярным перегородкам, а также наличием отсевов в виде свободно лежащих в просветах альвеол комплексов злокачественных клеток (В.П.Харченко и соавт.,1989).
Цитологически можно выделить интенсивно продуцирующий слизь (высокодифференцированный) и слабо продуцирующий слизь (низкодифференцированный) варианты бронхиолоальвеолярного рака. Для продуцирующего слизь варианта характерно обильное количество жидкой слизистопенистой мокроты. В препаратах отмечаются многочисленные сосочковые структуры из опухолевых клеток, имеющих более мелкие размеры, чем альвеолярные макрофаги. Фон препарата чистый, не содержит элементов воспаления и детрита. Папиллярные структуры имеют несколько вытянутую форму, составляющие их клетки практически однотипные: призматические или цилиндрические.
Ядра округлые, смещены к основанию клетки, ядерный хроматин компактный, имеет интенсивно базофильную окраску, иногда выявляются гипертрофированные ядрышки. Цитоплазма хорошо выражена, с признаками слизистой секреции. При бронхоскопии в материале, получаемом путем катетеризации или браш-биопсии, цитологическая характеристика опухолевых элементов идентична описанным выше.
Опухолевые клетки встречаются в виде сосочковых структур, но идентификация их затруднительна вследствие незначительного полиморфизма и выраженного сходства с элементами базальноклеточной гиперплазии и метаплазии.
Отдельные опухолевые клетки практически невозможно дифференцировать как злокачественные, так как они мало отличаются от бронхиального эпителия или мелких гистиоцитов. Важно отметить, что наличие цитологических признаков, расцениваемых как базальноклеточная пролиферация при отсутствии элементов воспаления и детрита, всегда должны вызывать подозрение на бронхиолоальвеолярный рак. Слабо продуцирующие слизь варианты опухоли характеризуются формированием папиллярных структур из кубических опухолевых клеток. Ядра их гиперхромные, располагаются центрально, имеют округлую форму, объем базофильной цитоплазмы незначительный.
В материале трансторакальной игловой биопсии, наряду с папиллярными структурами, нередко обнаруживаются также группы опухолевых клеток, не формирующие сосочки. Эти опухолевые элементы из выстилки альвеол. Характерно, что они имеют несколько более крупные размеры, чем элементы папиллярных структур. Встречаются клетки как кубической, так и призматической формы. Часто отмечаются признаки дистрофических изменений в виде интенсивной вакуолизации ядра и цитоплазмы.Гистологически в опухоли преобладает характерный тип пролиферации клеточных элементов. Высокие продуцирующие слизь цилиндрические, призматические или не продуцирующие слизь кубоидальные клетки в один ряд выстилают стенки предсуществующих альвеол и инфильтрируют легочную паренхиму без отчетливых признаков ее деструкции. Объем цитоплазмы различен: от обильной в высоких цилиндрических до незначительной в кубоидальных клетках. Также различен объем и характер слизистой секреции. Слизь выявляется либо диффузно во всей цитоплазме, либо в апикальных ее отделах. В этих случаях слизь может содержаться и в просветах альвеол.
Ядра клеток крупные, светлые, смещенные к основанию в цилиндрических клетках или гиперхромные, центpально расположенные в кубоидальных. Обнаруживаются гипертрофированные ядрышки, митозы редки. В отдельных участках опухоли обнаруживаются папиллярные структуры, выступающие в просвет альвеол. В просветах альвеол нередко встречаются отдельные, иногда плавающие в слизи, одиночные клетки или комплексы клеток.
В опухоли могут обнаруживаться очаги плоскоклеточной метаплазии, в участках с большим количеством сосочковых структур могут встречаться псаммомные тельца. Весьма характерным является состояние легочной стромы, сосудов и бронхов в зоне роста опухоли. Стенки альвеол практически не повреждены, что хорошо выявляется с помощью окрасок на соединительную ткань. В отдельных участках стенки альвеол могут быть несколько утолщены за счет разрастания фиброзной ткани, в основном в центральных отделах опухоли или в участках, построенных из малодифференцированных клеток.
Иногда в строме отмечается нерезко выраженная лимфоидная инфильтрация. Центральные отделы опухоли могут содержать гиалиновый или коллагеновый рубец и небольшие участки некроза. В отдельных новообразованиях просветы альвеол местами расширены с формированием полостей различных размеров, содержащих различное количество слизи, либо пустых, напоминающих эмфизематозные.Легочные сосуды в зоне роста опухоли остаются интактными и прослеживаются во всем ее объеме. Бронхи, вовлеченные в зону роста опухоли, сохранены, просветы бронхов мелкого калибра могут быть несколько расширены, в мелких бронхиолах внутренняя поверхность выстлана одним слоем опухолевых клеток. Эти черты гистологического строения характерны для всех вариантов (узлового, многоузлового, пневмониеподобного) роста бронхиолоальвеолярного рака.
Для уверенной диагностики бронхиолоальвеолярного рака необходимо использовать следующие диагностические критерии: исключить метастатическое происхождение опухоли, так как метастазы некоторых форм рака других органов (желудочно-кишечного тракта, яичника и т.д.) в легком могут имитировать бронхиолоальвеолярный тип роста; с уверенностью определить периферическую локализацию опухоли в паренхиме легкого; должны отсутствовать деструктивные и выраженные фиброзные изменения в зоне роста опухоли; сочетание бронхиолоальвеолярного типа роста с аденокарциномой другого строения исключает бронхиолоальвеолярный рак.
Ультраструктурная характеристика опухолевых элементов бронхиолоальвеолярного рака идентична другим подтипам аденокарциномы легкого.
2.2.4. Крупноклеточный рак
Крупноклеточный рак — злокачественная эпителиальная опухоль, построенная из крупных полиморфных клеток, не имеющих светооптически различимых признаков дифференцировки. Согласно гистологической классификации ВОЗ (1967), крупноклеточный рак подразделялся на следующие подтипы: солидный тип (с муциноподобными веществами и без них), гигантоклеточный рак и светлоклеточный рак.
Опухоли солидного типа являются недостаточно четко очерченной подгруппой, в отдельных участках как бы смыкающейся при светооптическом анализе с вариантами мелкоклеточного рака из клеток переходного типа, отличаясь от них отсутствием нейроэндокринной дифференцировки. Следует также отметить, что нередко опухоли, расцениваемые как умеренно и низкодифференцированный плоскоклеточный или железистый рак, содержат различные по объему участки из крупных недифференцированных клеток. В этих случаях, согласно рекомендациям ВОЗ, с учетом признаков специфической дифференцировки, опухоль должна быть расценена как плоскоклеточный или железистый рак. Только в том случае, если эти признаки не выявляются светооптически, опухоль может быть расценена как крупноклеточный недифференцированный рак.
Таким образом, вероятность такого диагноза зависит от количества участков опухоли, подвергнутых гистологическому исследованию. Выделение этой разновидности бронхогенного рака в самостоятельную нозологическую форму сомнительно, так как при ультраструктурном анализе выявляются признаки либо плоскоклеточной, либо железистой, либо диморфной дифференцировки, вследствие чего во втором издании гистологической классификации ВОЗ (1981) солидный крупноклеточный рак не выделяется. Однако мы считаем необходимым привести и эту форму крупноклеточного рака легкого, так как в практической работе врачу-патологоанатому приходится встречаться с подобными вариантами рака легкого.
Крупноклеточный рак солидного типа цитологически представлен разрозненными или небольшими группами крупных полиморфных клеток без признаков плоскоэпителиальной или железистой дифференцировки. Как правило, выражены деструктивные изменения. Характерно наличие двух- или многоядерных клеток. Четко выражены крупные нуклеолы. Границы ядерной мембраны извилистые, нередко с инвагинациями. Границы цитоплазмы нечеткие. Характерно наличие сопутствующей лимфоцитарной реакции.
Гистологически крупные клетки опухоли растут в виде широких пластов или полей, не имеющих каких-либо признаков структурной организации. Злокачественные элементы при компактном расположении довольно мономорфны, а при рыхлом — отличаются полиморфизмом, границы их хорошо очерчены. Цитоплазма клеток бледная, обычно гомогенная, в отдельных клетках — слегка зернистая. Форма ядер вариабельна, могут встречаться отдельные многоядерные клетки. Десмопластическая реакция, как правило, не выражена.
Гигантоклеточный рак отличается от крупноклеточного не только своеобразной гистологической структурой, но и очень высокой злокачественностью. Впервые гигантоклеточный рак описан Nash и Stout (1958). Не все морфологи выделяют эту опухоль в отдельный тип, поэтому за рубежом описано более 40 наблюдений. Тем не менее, считается, что эта форма составляет 4% злокачественных поражений легких (Kallenberg и соавт.,1979).
В отличие от крупноклеточного рака солидного типа, при гигантоклеточном раке гистологический диагноз строится не на исключении других вариантов новообразований, а по характерным чертам: особо высокий полиморфизм с преобладанием необычных гигантских клеток. Многие морфологи отмечают, что подобные структуры иногда обнаруживаются в виде участков при плоскоклеточном и железистом раке. Но в этих случаях нельзя говорить о гигантоклеточном раке как нозологической форме.Средний возраст больных — 54 года, но встречается в любом возрасте. Большинство больных — мужчины. Характерно быстрое увеличение размеров опухоли, экстраплевральное распространение, раннее лимфогенное и гематогенное метастазирование. Прогноз неблагоприятный, однако описаны случаи необычайно высокой чуствительности гигантоклеточного подтипа опухоли к цитостатикам (цисплатина,випезид,ифосфамид). После курса неоадъювантной химиотерапии и полной ремиссии возможна радикальная операция с хорошим отдаленным результатом (Nastasi G.et al.,1990).
Узлы опухоли (иногда мультицентрического характера) чаще располагаются в легочной паренхиме и редко прорастают крупные бронхи. Обычно отмечается инфильтрация грудной стенки, диафрагмы, средостения. Гистологическая характеристика. Очень крупные многоядерные клетки располагаются среди более мелких злокачественных клеток. Нет никаких признаков плоскоклеточной или железистой диффернцировок. Ядра гигантских клеток крайне полиморфны, необычного вида, с неравномерным распределением хроматина и четко определяющимися гипертрофированными ядрышками. Обильная цитоплазма слегка эозинофильна, часто пенистая или с вакуолями. Митозы редки или отсутствуют.
Характерно захватывание мелких злокачественных клеток и нейтрофилов гигантскими опухолевыми клетками. N.S.Wang и соавт. (1976) рассматривали это явление не как фагоцитоз, а как миграцию более молодых клеточных элементов в старые, гигантские (emperiolesis). Небольшие опухолевые клетки могут иметь веретенообразную форму, тогда опухоль напоминает рабдомиосаркому. Однако нет поперечной исчерченности клеток. Эпителиальная принадлежность гигантоклеточного рака доказана методом эксплантации культуры тканей. При дифференциальной диагностике следует учитывать, что гигантоклеточный рак может имитировать также метастазы рака коры надпочечников, злокачественной фиброзной гистиоцитомы и некоторых других опухолей с высокой степенью анаплазии.
Ультраструктурная характеристика. Клетки опухоли характеризуются неправильной формы уродливыми ядрами с крупными глыбками гетерохроматина и четкими гипертрофированными ядрышками. В цитоплазме встречаются своеобразные включения в виде агрегатов нескольких пар центриолей и скопления гранул размером 55-75 нм. Эндоплазматический ретикулум выражен слабо, но много митохондрий. Тонофибриллы 6-8 нм толщиной образуют плотные концентрические завихрения. Видны межклеточные контакты и связь с базальной мембраной. Микроворсинок на поверхности клеток нет.Природа включений в злокачественные клетки не установлена. Высказывается предположение о их вирусном происхождении.
Светлоклеточный рак впервые описан в 1955 г. Walter и Price. В нашей стране (16 наблюдений) эта опухоль изучена Р.И.Вагнером и соавт.(1981). Частота светлоклеточного подтипа среди других злокачественных новообразований легкого составляет 0,9%.Некоторые авторы не видят необходимости в выделении этого исключительно редкого типа опухоли в отдельную группу, так как участки такого строения можно иногда встретить среди полей немелкоклеточного рака легкого. Другие авторы считают светлоклеточный рак разновидностью крупноклеточного рака легкого.
Предполагают, что опухоль возникает либо из нейроэндокринных клеток выстилки дыхательных путей, либо из гладкомышечных элементов их стенки. Gliedl (1979) высказал точку зрения, что гистогенез светлоклеточного рака легкого связан с клетками Клара, содержащими много гликогена и секреторных гранул. Функция клеток Клара заключается в секреции ферментов липазы и фосфатазы в просвет бронхиол. Ферменты эти вызывают распад сурфактанта и играют важную роль в метаболизме последнего. Гликоген является признанным маркером светлоклеточного рака легкого.
Узлы опухоли 2-11 см в диаметре чаще располагаются в средних долях легкого, имеют фестончатые четко очерченные контуры. Первичное поражение крупных бронхов встречается редко. Иногда в опухоли определяется полость распада. Прорастание сосудов указывает на особо неблагоприятный прогноз. Гистологическая характеристика. Основными злокачественными элементами являются крупные полигональные или округлые прозрачные («пустые») клетки с обильной сетчатой цитоплазмой, содержащие небольшое центрально расположенное светлое ядро с гиперхромным ядрышком. В цитоплазме определяется ШИК-положительный материал и гликоген. Кроме того, в опухоли может быть значительная примесь полиморфных и гигантских клеток,которые образуют скопления и пласты с характерным центральным некрозом.
Строма опухоли представлена хорошо развитыми соединительнотканными прослойками. Подобные структуры легко принять за метастаз гипернефроидного рака, однако в отличие от него клетки светлоклеточного рака легкого не содержат жир. Нередко светлоклеточный рак классифицируют как низкодифференцированный плоскоклеточный или железистый рак, в зависимости от выявленных участков дифференцировки. Но наиболее важно отличить эту форму рака от доброкачественной светлоклеточной опухоли легкого, клетки которой также содержат большое количество гликогена («sugar» tumor). Ультраструктура. Крупные полигональные клетки плотно прилежат друг к другу, имеют в отдельных местах десмосомальные контакты. Ядра круглые, хроматин мелкодисперсный, диффузно распределен по всей кариоплазме. Ядрышки мелкие, плотные, зернистого характера.
В светлой цитоплазме — незначительное количество митохондрий, профили шероховатого эндоплазматического ретикулума, микрофиламенты, рибосомы и много гранул гликогена. Прогноз при светлоклеточном раке легкого зависит от размеров первичного очага и характера метастазирования опухоли. При размерах очага более 5 см результаты лечения обычно плохие. У таких больных прогноз мало отличается от такового при других типах недифференцированного рака легкого.
2.2.5. Железисто-плоскоклеточный рак
Опухоль, представленная элементами плоскоклеточного рака и аденокарциномы, составляет около 1% злокачественных поражений легкого. В отдельных новообразованиях проявляются отчетливые признаки дифференцировки в двух направлениях. Большинство же комбинированных поражений является преимущественно крупноклеточным недифференцированным раком, содержащим в отдельных участках группы ороговевших клеток («раковые жемчужины»).
В других случаях изредка обнаруживаемые межклеточные мостики указывают на плоскоэпителиальную дифференцировку, а участки железистой дифференцировки или наличие слизи — на аденокарциному. Клиническое же поведение железисто-плоскоклеточного рака в большей степени сходно с аденокарциномой. Опухоли обычно локализуются в периферических отделах легкого и имеют выраженную тенденцию к метастазированию, причем метастазы нередко обнаруживаются уже к моменту выявления новообразования.
Согласно наблюдениям H. Spencer (1968), многие формы периферического рака, связанные с рубцом, при тщательном исследовании оказываются комбинированным железисто-плоскоклеточным раком. В то же время важно отметить, что небольшие по объему железистоподобные структуры, выявляющиеся в зоне роста плоскоклеточного рака, могут быть остатками предсуществующей легочной паренхимы, что подтверждается при электронно-микроскопическом исследовании.
2.2.6. Лимфоэпителиоидный рак (опухоль Шминке)
Лимфоэпителиома — (опухоль Шминке; синцитиальный, переходноклеточный рак) злокачественная опухоль эпителиального происхождения с примесью различного количества реактивных лимфоидных инфильтратов. Встречается чаще у мужчин в возрасте 30-50 лет.
Хотя впервые опухоль описана в носоглотке, наиболее богатой лимфоидной тканью (по классификации ВОЗ — 3-й тип рака носоглотки) лимфоэпителиоидный рак возникает в различных органах, особенно в дыхательных путях. Однако это случается исключительно редко. Описаны единичные наблюдения поражения околоносовых пазух, гортани, глотки, трахеи и легкого (Frank D.K. с соавт.,1995).
Как нозологическую форму, лимфоэпителиому впервые выделил A Schmincke в 1921 г. и считал ее комбинацией лимфосаркомы и переходноклеточного рака верхних дыхательных путей. На примере 5 наблюдений он достаточно подробно коснулся проблем гистогенеза заболевания, а также вопросов диагностики и лечения.
Лимфоэпителиома состоит из эпителиальных клеток и различных форм лимфоцитов, в частности малых лимфоцитов. Никакого систематического разъединения этих двух морфологических элементов межуточной тканью или мембраной не существует. Оба вида клеток находятся в непосредственном взаимном соприкосновении — «лимфоидный симбиоз».
Второй особенностью образования является полное отсутствие ороговения эпителиальных клеток. Третья особенность — высокая чувствительность ко всякой лучевой энергии (даже от небольших доз низковольтного рентгеновского облучения).
Лимфоэпителиома имеет ретикулоэндотелиальное строение. Главную массу составляют различных размеров клетки с неясными очертаниями, с бледной цитоплазмой. Они то сливаются в сплошные массы, то соприкасаются цитоплазматическими отростками, образуя сетчатый фон и промежутки между отростками цитоплазмы. Ядра обычно круглые, большинство с митозами атипичного характера. Промежутки между отростками ретикулоэндотелиального строения более или менее густо и неравномерно заполнены лимфоцитами. Типичная ошибка морфологов — распознавание опухоли как «лимфосаркомы».
Опухоль чрезвычайно радиочувствительна — «тает на глазах» в процессе лучевой терапии. Во многих случаях (примерно у каждого второго больного) удается добиться стойкой и полной ремиссии. У 9% больных обнаруживаются метастазы в регионарных лимфатических узлах.
Лимфоэпителиоидный рак — недифференцированная или низкодифференцированная плоскоклеточная злокачественная опухоль из эпителия дыхательных и пищеварительных путей с выраженной инфильтрацией лимфоидными элементами.
В России первые 5 случаев поражения глотки лимфоэпителиоидным раком описал А.О.Верещинский (1933). В последующем описано еще 24 наблюдения [Розенгауз Д.Е., Левин Я.Р.,1956]. В последние годы описаны также лимфоэпителиоидный рак слюнной и вилочковой железы, матки и кожи.
Лимфоэпителиоидный рак легкого впервые описал L.R.Begin сравнительно недавно — в 1987 г. К настоящему времени известно о 23 наблюдениях [Chan J.K.C. с соавт.,1995]. При использовании современных методов исследования (серологические реакции, гибридизация, амплификация ДНК и др.) доказана связь опухоли с вирусом Эпштейна-Барр, особенно у жителей юго-восточной Азии.
A. Butler и соавт. (1989) привели четыре наблюдения лимфоэпителиоидного рака легкого у больных 56-72 лет. Опухоли выявлены случайно при рентгенологическом исследовании в виде периферических узлов. В двух наблюдениях серологические реакции указывали на инфицированность вирусом Эпштейна-Барр. В клетках опухоли доказана гибридизация с геномом вируса. В лимфоцитах стромы и здоровых тканей признаков гибридизации с вирусом не выявлено. В одном наблюдении произведено электронно-микроскопическое исследование, обнаружены признаки плоскоэпителиальной дифференцировки опухолевых клеток. При тщательном обследовании и последующем наблюдении поражения носоглотки не выявлено. После лобэктомии 3 больных живы без рецидива 2-9 лет. У одной больной через 18 месяцев — рецидив опухоли в плевре.
На ранних стадиях опухоль бронха имеет вид округлого полипообразного образования, которое покрывает интактная слизистая оболочка. На разрезе — опухоль бледно серого цвета. Консистенция плотноэластическая. При поражении носоглотки в поздних стадиях поверхность лимфоэпителиомы имеет тенденцию к распаду и изъязвлению. В отличие от дифференцированных форм рака опухоль отличается очень высокой радиочувствительностью.
Гистологическая структура. Опухоль построена из крупных пластинчатых клеток, лежащих разрозненно или в виде гнезд, рыхло связанных тяжами. Клетки имеют разную форму, контуры их могут быть неотчетливыми. Цитоплазма бледная, иногда отростчатая. Ядра крупные, светлые, обычно округлой или овальной формы с фуксинофильными ядрышками.
Клетки опухоли располагаются небольшими пластами или гнездами среди инфильтратов, состоящих из лимфоцитов и плазмоцитов. Недифференцированные эпителиальные элементы теряются среди лимфоидной ткани, значительное количество которой делает опухоль похожей на лимфому.
Таким образом, при отсутствии некрозов и изъязвлений опухоли отмечается относительно благоприятное течение заболевания. Возможно полное выздоровление после только лучевой терапии. При изъязвленных формах прогноз неблагоприятен при любом виде лечения.
Хотя лучевую терапию следует считать обязательным компонентом лечения, опыт применения этого метода при поражении дыхательных путей ограничен. Это связано с трудностями диагностики заболевания, истинная природа которого выясняется только после удаления опухоли. Кроме того, играет роль выраженный стеноз просвета трахеи.
За последние годы особое внимание уделяется этой группе новообразований, имеющих сходство с элементами вилочковой железы: гамартоматозная тимома, внутрищитовидная эпителиальная тимома, эктопическая тимома шеи, веретенноклеточная опухоль с тимусоподобными элементами, рак щитовидной железы с признаками тимомы, рак с тимусоподобными элементами. Гистологически эти первичные опухоли не отличимы от лимфоэпителиомы. С другой стороны, известны цитологические критерии дифференциальной диагностики, позволяющие с достаточной точностью подтвердить диагноз лимфоэпителиоидного рака щитовидной железы [Ng W.K.с соавт., 1996, Shek W.H. с соавт.,1996].
Torii Y. с соавт. (1994) описали аутопсийный случай лимфоэпителиоидного рака средостения у больного 67 лет. При медиастиноскопии установлен диагноз «недифференцированный рак» и проведена лучевая терапия. Через 6 месяцев возник рецидив опухоли. Хотя химиолучевая терапия сопровождалась явной положительной динамикой, больной умер от пневмонии. На вскрытии обнаружена типичная картина лимфоэпителиоидного рака. Носоглотка и вилочковая железа оказались интактными.
Таким образом, лимфоэпителиоидный рак дыхательных путей встречается чаще, чем это принято считать.
Точная диагностика опухоли до операции трудна, и заболевание протекает под маской низкодифференцированной опухоли. При дифференциальной диагностике необходимо помнить о возможности вторичного поражения трахеи лимфоэпителиоидным раком щитовидной железы.
Глава 3. Опухоли из бронхиальных желез
Опухоли бронхиальных желез известны еще с конца ХIХ — начала ХХ веков, хотя первые авторы (H. Muller,1882; O. Horn, 1907; Heck, 1916 и др.) рассматривали эти новообразования дыхательных путей как своеобразные более медленно протекающие варианты рака легкого. R. Kramer (1930) обозначил их термином «аденома бронха». В литературе фигурируют также и другие обозначения: эпицистома, то есть опухоль, ведущая к закупорке бронха (N. Delarue, 1951), полиповидная опухоль (P. Santy и соавт.,1953).
Однако термин «аденома» бронха довольно часто уптреблялся в литературе, хотя и включал в себя различные по гистогенезу, гистологическому строению и даже степени злокачественности опухоли. Так, R. Jensik и соавт.(1974), J. Nitschke и соавт. (1978) среди «аденом» выделяли группу потенциально злокачественных («полузлокачественных») новообразований. H.Leschke (1956,1957) различал три группы «аденом»: 1) истинно доброкачественные; 2) морфологически доброкачественные, но с инфильтрирующим ростом и возможным метастазированием в региональные лимфатические узлы; 3) истинно злокачественные с гистологическими и клиническими признаками злокачественности.
Д.И.Головин (1975) и L. Kreyberg (1967), учитывая пестроту клинических проявлений этих опухолей, не рекомендовали применение термина «аденома». Однако, большинство хирургов продолжали выделять «аденомы» бронхиальных желез, считая, что лечебная тактика при этих новообразованиях существенно отличается от тактики при раке.
D.Gullino (1970) пишет, что под термином «аденома» бронха понимают различные по гистологическому строению опухоли, характеризующиеся в отличие от бронхогенного рака относительно медленным ростом с постепенным сужением просвета крупного бронха и развитием в дальнейшем бронхо-обструктивного синдрома, который является ведущим в клиническом течении заболевания. К сказанному следует добавить, что в более редких случаях отмечена периферическая локализация «аденом», возникающих в субсегментарных бронхах.
По мере накопления опыта значительно расширился перечень новообразований, обозначаемых термином «аденома». Первоначально классическим представителем этой группы считали аденокистозный рак (цилиндрому), а затем-мукоэпидермоидную опухоль.В дальнейшем стали выделять 4 основные разновидности новообразований бронхиальных желез: аденокистозный рак, мукоэпидермоидную опухоль, цистаденому и плеоморфную аденому-смешанную опухоль.Анализ литературы и собственный опыт показал, что существуют и другие разновидности «аденом» бронха, имеющие свои аналоги среди новообразований слюнной железы: ацинозноклеточная опухоль, папиллярная цистаденома, мономорфная (тубулярная) аденома.
Следует отметить также неоднородную по гистогенезу группу новообразований, которые фигурируют в литературе как «светлоклеточные опухоли». Некоторые авторы среди светлоклеточных новообразований легкого различают онкоцитарную, или оксифильную аденому (H. Spencer, 1979; A.Warter и соавт.,1981; T. Cwierzyk и соавт.,1985). Они подчеркивали, что эти опухоли отличаются по клиническому течению (онкоцитарная аденома, как и цистаденома, истинно доброкачественное новообразование), однако их морфологическая дифференциальная диагностика крайне сложна. Достаточно сказать, что светлоклеточные опухоли легких нередко ошибочно диагностируют как бронхогенный рак или метастаз рака почки в легкое. Некоторые авторы (Е.А.Смирнова и соавт.,1984) справедливо считают, что дифференциальная диагностика светлоклеточных опухолей возможна только при использовании электронной микроскопии.
Таким образом, в группу опухолей трахеальных и бронхиальных желез в настоящее время включают: аденокистозный рак, мукоэпидермоидный рак (высоко- и низкодифференцированный варианты), плеоморфную аденому («смешанную опухоль») и редко встречающийся ее злокачественный аналог, а также другие более редко встречающиеся новообразования(ацинозноклеточная опухоль, онкоцитарная или оксифильная аденома, мономорфная аденома-цистаденома).
Опухоли бронхиальных желез по частоте занимают третье место после карциноидов, значительно уступая бронхогенному раку. Они составляют от 1 до 12% от общего количества случаев онкологической патологии легких. При оценке только новообразований трахеи это соотношение существенно меняется. Среди новообразований бронхиальных желез 34,4-38,4% наблюдений составляет аденокистозный рак, 28,6-30,8%-мукоэпидермоидный рак, до 37%-другие варианты новообразований (H. Spencer, 1979; R. Radke и соавт., 1979). Наиболее редко встречается онкоцитарная аденома и ацинозноклеточная опухоль. Однако редкость этих форм новообpазований бpонхиальных желез в значительной мере обусловлена ошибочной морфологической диагностикой и неосведомленностью специалистов.
Опухоли бронхиальных желез, по мнению большинства исследователей, несколько чаще возникают у женщин, которые составляют 55-77% от общего числа больных. Так, на материале Б.В.Петровского с соавт. (1978) среди 155 больных было 98 женщин (63,2%). Следует подчеркнуть, что бронхогенный рак чаще возникает у мужчин ( в 82-99%, по данным различных авторов).Опухоли бронхиальных желез в отличие от бронхогенного рака выявляются у лиц более молодого возраста (возраст больных варьирует от 1 года до 76 лет). Средний возраст больных находится в пределах 44-46 лет (И.В.Двораковская и В.Л.Толузаков, 1978; Schmid de Gru- neck с соавт.,1977).
Характерно, что опухоли бронхиальных желез нередко возникают у лиц молодого возраста и у детей. Сказанное в большей степени относится к мукоэпидермоидному раку. Описаны и другие разновидности опухолей бронхиальных желез у детей: ацинозноклеточная опухоль, онкоцитарная аденома ( D. Katz и соавт., 1976; A. Santos-Briz и соавт., 1977 и др.). По данным J. Mullins и соавт. (1979) лица моложе 20 лет составляют 6-8% от общего числа больных с опухолями бронхиальных желез. Бронхогенный рак у лиц моложе 30 лет обнаруживается крайне редко, причем в части таких случаев речь идет о мукоэпидермоидном или аденокистозном раке, ошибочно диагностированных как рак легкого.
Эти показатели, то есть средний возраст, соотношение мужчин и женщин, в основных разновидностях опухолей бронхиальных желез несколько отличаются. Мукоэпидермоидный рак возникает в более молодом возрасте: средний возраст 30-35 лет; средний возраст больных аденокистозным раком варьирует в пределах 46-48 лет. Более отчетливое преобладание лиц женского пола отмечают среди больных мукоэпидермоидным раком.Опухоли бронхиальных желез возникают преимущественно (в 90-98% случаев) в главных бронхах и проксимальных отделах долевых бронхов. На нашем материале у 4 больных они встретились в периферических отделах легких. По данным M. Paetz и K. Wetzer (1969), И.В.Двораковской ( 1979) частота периферических поражений достигает 11-28%. Характерно, что правое легкое (обычно среднедолевой бронх) поражается в несколько раз чаще, чем левое (Б.В.Петровский и соавт., 1978; M. Donev и соавт., 1973).
Выявлялись случаи первичной множественности этих новообразований, однако чаще они обнаруживаются синхронно или метахронно с карциноидами. По нашему опыту для смешанной опухоли довольно характерно одновременное поражение главного бронха и трахеи.
Опухоли бронхиальных желез, независимо от того, являются они доброкачественными или злокачественными, обладают тремя типами роста: 1) экзофитный-опухоль растет в просвет бронха; 2) эндофитный-перибронхиальный, узловой; 3) смешанный, при котором нередко бывает рентгенологическая картина «айсберга».Форма роста в значительной степени зависит от гистологического типа опухоли. Экзофитный рост отмечается у 49% больных, эндофитный-у 7%, смешанный-у 44% больных. При любой форме роста в клинической картине доминируют симптомы обтурации просвета крупного бронха или трахеи. На нашем материале чисто экзофитный рост опухоли определялся только при цистоаденоме, ацинозноклеточной опухоли и онкоцитоме.
Период от появления первых симптомов (кашель, повторные пневмонии, гриппозные состояния) исчисляется годами-от нескольких месяцев до 18 лет и более. Как правило, больные длительно и безуспешно лечились от бронхиальной астмы, хронического бронхита, эмфиземы легких, туберкулеза, хронической пневмонии. В среднем этот период длится 6,5 года и обычно зависит не от гистологических особенностей опухоли, а от квалификации лечебных учреждений, оснащенности их современными методами исследования легких. За последние годы латентный период сократился до 3,5 года.
При бронхоскопии опухоли бронхиальных желез имеют вид мягко-эластического образования, но иногда могут быть рыхлыми, хрупкими. Чаще они покрыты слизистой оболочкой розовато-красного цвета, иногда с синюшным оттенком. Некоторые их типы склонны к изъязвлению. Эндоскопическая биопсия у некоторых больных может быть опасна из-за кровотечения.
При бронхоскопии удается установить гистологический тип опухоли приблизительно у 80% больных. Тем не менее, после операции нередко уточняются особенности поражения. Довольно часто мукоэпидермоидную опухоль принимают за плоскоклеточный рак у больных зрелого возраста. Наиболее трудна дифференциальная диагностика периферических поражений.
За последние годы все большей популярностью пользуются эндоскопические резекции опухолей бронхиальных желез. Показания к таким вмешательствам: 1) подвижная опухоль на тонкой ножке (следует учитывать, что у 45% больных возможны локальные рецидивы); 2) частичное удаление опухоли проводят с целью восстановления проходимости бронха, что позволяет в дальнейшем выполнить радикальную операцию; 3) при противопоказаниях к радикальному лечению в связи с возрастом или общим состоянием больного. До операции следует тщательно изучить функциональные легочные резервы. Нередко после органосохраняющих резекций дыхательная недостаточность уменьшается.
Оценивая показания к радикальному лечению, необходимо учитывать гистологический тип опухоли. При аденокистозном раке объем резекции обычно соответствует радикальной операции при бронхогенном раке. Раньше эту форму считали радиорезистентной и лучевую терапию не применяли. В настоящее время имеется опыт свидетельствующий о положительном эффекте комбинированного лечения с использованием дополнительного облучения.
Прогноз также зависит от гистологической структуры. В целом 5-летняя выживаемость после радикального лечения достигает 85%. При аденокистозном раке этот показатель ниже (60-70%). Рецидивы могут возникать через 15 лет после радикального лечения. У больных мукоэпидермоидным раком прогноз также менее благоприятный.
Данные литературы о частоте метастазирования основных форм опухолей бронхиальных желез противоречивы, но все же свидетельствуют о том, что аденокистозный и мукоэпидермоидный типы должны быть отнесены к злокачественным новобразованиям, хотя степень малигнизации (частота метастазирования) варьирует в значительных пределах и зависит от многих факторов: длительности существования опухоли, ее размеров, степени морфологической атипии.
3.1. АДЕНОКИСТОЗНЫЙ РАК
Эндобронхиальную опухоль с цилиндроматозной структурой описал впервые R.Heschl в 1877 г. Подобное новообразование слюнной железы наблюдал еще в 1853 г. Robin. Термин «цилиндрома» принадлежит Т.Бильроту. С 1952 г. принят новый термин «аденокистозный рак», который лучше отражает злокачественную природу заболевания и принят сейчас повсеместно (см. раздел 1.1). Аденокистозный рак составляет 0,1-0,2% первичных солидных новообразований легкого и в среднем 12% (8-21%) всех новообразований бронхиальных желез. Дискутабельным остается вопрос о его миоэпителиальном происхождении.
Первичный очаг аденокистозного рака обычно располагается в крупных бронхах и особенно часто в верхней трети трахеи. Бронхи поражаются чаще всего в проксимальных отделах. Средний возраст больных-50-60 лет. Опухоль не связана с курением сигарет.Обычно при аденокистозном раке определяется отчетливый экзофитный компонент. Опухоль имеет вид выбухающих в просвет бронха бугристо-узловатых разрастаний. Иногда это полиповидный вырост. Ткань опухоли мягко-эластической консистенции, умеренной плотности, однородная, серого цвета, без участков некроза. В отличие от карциноида эта форма рака распространяется на значительном расстоянии проксимально и дистально, вызывая полуциркулярное утолщение стенки дыхательной трубки.
Аденокистозный рак может распространяться в пределах слизистого слоя трахеи, не образуя четко различимых узлов опухоли. Иногда процесс охватывает трахею циркулярно в виде утолщения слизистой оболочки. В последующем опухоль инфильтрирует межхрящевые мембраны и соседние структуры. Характерна инфильтрация периневральных пространств и нервов с последующим распространением на перикард, крупные сосуды или корень легкого. Метастазы в регионарных лимфатических узлах выявляются в 10% наблюдений при первом обследовании больного. Отдаленные метастазы возможны в легких, печени, органах брюшной полости, а также в костях.
Гистологическая характеристика. В целом опухоль аналогична микроскопическому строению аденокистозного рака слюнной железы. Выделять какие-либо варианты мы считаем нецелесообразным, так как в одной опухоли можно обнаружить участки различного строения. Исключение представляет аденокистозный рак с гиалинозом стромы.
Опухоль в основном состоит из однотипных мелких темных клеток со скудной цитоплазмой и мономорфными гиперхромными ядрами. Атипические митозы отсутствуют. Эти клетки формируют солидные, трабекулярные, солидно-альвеолярные, мелкие железистоподобные структуры, образующие обширные поля ажурного (криброзного) строения. Более крупные кисты встречаются значительно реже, чем в аналогичной опухоли слюнной железы. Кроме темных клеток можно встретить крупные клеточные элементы со светлой цитоплазмой. Эти клетки окаймляют просветы некоторых железистоподобных образований. В некоторых участках аденокистозного рака выражен гиалиноз. Часто в одной и той же опухоли можно видеть все перечисленные выше морфологические структуры.
Аденокистозный рак с выраженным гиалинозом состоит из мелких опухолевых клеток, замурованных в виде островков или анастомозирующих тяжей в гиалинизированной строме. Подобный вариант аденокистозного рака четко отграничен от ткани легкого фиброзной капсулой. Однако, он, как правило, обладает отчетливым инфильтрирующим ростом с распространением опухолевых комплексов за пределы местами сохранившейся капсулы в паренхиму легкого. Выраженный перибронхиальный рост, инвазия в ткань легкого, обнаружение опухолевых элементов в просвете сосудов являются признаками неблагоприятного прогноза и гематогенной диссеминации.
Цитологическая характеристика. Клеточные элементы аденокистозного рака, как правило, с мокротой не выделяются. Цитологическая диагностика опухоли возможна по отпечаткам с биоптата в связи с весьма характерной картиной. Мелкие клетки опухоли округлой и овальной формы довольно мономорфны, гиперхромны, располагаются скоплениями среди оксифильного мелкозернистого межуточного вещества. Характерны шаровидные скопления межуточной субстанции, вокруг которых располагаются опухолевые клетки.
При дифференциальной диагностике с аденокарциномой следует учитывать отсутствие выраженного клеточного полиморфизма и признаков секреторной активности клеток этой опухоли. В отличие от анапластического мелкоклеточного рака митозы встречаются редко.
Ультраструктура. Клетки имеют хорошо выраженную базальную мембрану с многочисленными расслоениями и ответвлениями по типу гирлянд. Своеобразно взаимное расположение клеток. В одних участках они располагаются компактно, контактируя посредством десмосом. Местами между клетками остаются небольшие пространства. Кое-где отмечается расширение межклеточных пространств с образованием полостей, свободная поверхность которых имеет микроворсинки. В просвете иногда можно обнаружить хлопьевидные массы.
Большая часть клеток низкой дифференцировки с небольшим количеством органелл: отдельные митохондрии, вакуоли, полирибосомы. Клетки, непосредственно ограничивающие просвет, имеют более светлую цитоплазму, многочисленные десмосомы, светлые вакуоли, а также скопления филаментозных структур типа тонофиламентов, фокальные уплотнения отсутствуют.
О характере секрета, обнаруживаемого в просвете криброзных структур и по их периферии, высказаны неоднозначные мнения. Некоторые авторы различают два вида секрета: слизь (внутри железистых трубок) и гиалин (по периферии криброзных структур). Некоторые отмечают слабоположительную реакцию слизеподобных масс при окраске альциановым голубым, который окрашивает также и вещество вокруг криброзных и тубуло-трабекулярных структур. Но большинство исследователей считают, что клетки опухоли не обладают признаками экзо- и эндосекреции, а содержимое криброзных и протокоподобных структур расценивают как продукт деградации базальной мембраны. Гиалиноподобное вещество по тинкториальным свойствам нельзя считать слизистым.
Гистогенез аденокистозного рака остается спорным. Первоначально предполагалось, что эта опухоль, как и карциноид, относится к новобразованиям нейроэндокринной системы (F. Feyrter, 1961; D.Gullino, 1970; F.Cataliotti и соавт., 1972). В дальнейшем на основании электронномикроскопического исследования данная точка зрения была отвергнута.
В настоящее время установлено, что аденокистозный рак гистогенетически связан с бронхиальной железой. Однако по вопросу о том, какие элементы железы служат источником опухолевого роста, высказываются различные мнения: эпителий выводных протоков, секреторные элементы, миоэпителиальные клетки или же, как считает S. Markel и соавт. (1964), недифференцированные клетки эпителия бронхов. Многие исследователи подчеркивают, что аденокистозный рак гистогенетически связан с клетками выводных протоков желез, причем указывают на миоэпителий как источник роста опухоли. Y. Hoshino и J. Yamamoto (1970) наблюдали в опухоли два типа клеток: миоэпителиальные и эпителиальные. Однако И.В.Двораковская (1979); Г.А.Галил-Оглы и соавт. (1981); J. Varley и K. Hollman (1975) приводят другие данные: аденокистозный рак состоит из низкодифференцированных эпителиальных клеток без признаков какой-либо секреции. При этом И.В.Двораковская (1979) не исключает гистогенетической связи данного новообразования с миоэпителием выводных протоков бронхиальных желез.
3.2. МУКОЭПИДЕРМОИДНЫЙ РАК
Мукоэпидермоидную опухоль с двойным метапластическим потенциалом P.Masson, L.Berger (1924) первоначально обнаpужили в слюнной железе. Сразу было отмечено, что наряду с доброкачественным вариантом опухоли, существуют формы, склонные к рецидивированию и метастазированию. H. Smetena и соавт.(1952) описали такие же опухоли, исходящие из клеточных элементов бронхиальных желез. Эти образования длительный период относили к «аденомам» бронхов. Однако, довольно скоро стало ясно, что эти опухоли ведут себя как злокачественные новообразования (A.Turnbull и соавт., 1979; S. Borsky и соавт., 1983). В последние годы «мукоэпидермоидный рак» является общепринятым термином.
Опухоль составляет около 2% онкологических поражений легкого и 6% (3-9%) случаев опухолей бронхиальных желез. Встречается в возрасте 9-78 лет (в среднем 34,8 года). Около 50% больных-моложе 30 лет. Связи опухоли с табакокурением не отмечено.Мукоэпидермоидный рак имеет вид эндофитного или экзофитного образования, размерами 0,8-6,0 см в диаметре. Опухоль располагается чаще в крупном бронхе и покрыта гладкой слизистой оболочкой.
Гистологическая характеристика. Мукоэпидермоидный рак представлен тремя типами клеток: 1) эпидермоидные элементы (без ороговения и межклеточных мостиков) образуют солидные поля или выстилают кисты; 2) железистые элементы (иногда типа бокаловидных) могут выстилать кисты или образовывать папиллярные выросты (в просвете-слизистые массы); 3) промежуточные элементы типа базальных клеток с пустой светлой цитоплазмой.
Опухоль характеризуется пестрым микроскопическим строением за счет сочетания двух эпителиальных компонентов, эпидермоидного и железистого, различной степени дифференцировки клеток в каждом из компонентов и разнообразия клеточных группировок и формируемых ими структур.
Железистый компонент представлен то однородным уплощенным эпителием ( без продукции слизи), то кубическим или цилиндрическим типа бокаловидных клеток со светлой слизесодержащей цитоплазмой. Эти клетки образуют железистоподобные структуры и кисты, выполненные слизью. Некоторые железы образованы мелкими со скудной цитоплазмой и гиперхромными ядрами клетками, в которых не выявляется продукция слизи. Эти клетки, возможно, являются менее дифференцированными элементами железистого компонента. Следует подчеркнуть, что в участках, где преобладает железистый компонент, всегда можно видеть скопления элементов плоского эпителия в виде гнезд, ячеек или окаймляющих мелкие кисточки.
Эпидермоидный компонент также разнообразен. Наиболее характерны в плане диагностики скопления крупных плоскоэпителиальных клеток с отчетливой цитоплазмой. Эти клетки образуют небольшие ячейки, располагающиеся в фиброзной строме, или выстилают кисты с наличием в них слизи. Обращают на себя внимание скопления среди плоского эпителия клеточных элементов, содержащих в цитоплазме слизь. В отдельных участках крупные мономорфные клетки плоского эпителия образуют солидные разрастания, однако ни в одной опухоли мы не обнаружили признаков ороговения. Вместе с тем, в опухоли можно встретить солидно-альвеолярные скопления из мелких эпителиальных клеток типа базалоидных. Клетки опухоли иногда располагаются по периферии солидных разрастаний из крупных плоскоэпителиальных клеток.
В пластах из эпидермоидных клеток также обнаруживается слизь. Нередко морфологи принимают опухоль за плеоморфную аденому. Следует учитывать, что в мукоэпидермоидных новообразованиях в строме отсутствуют миксоидные и хондроидные (остеоидные) изменения.Много споров вызывает вопрос: является ли мукоэпидермоидная опухоль бронхов доброкачественным или злокачественным новообразованием? Аналогичные опухоли слюнных желез подразделяют на высоко- и низкодифференцированные варианты. Высокодифференцированная мукоэпидермоидная опухоль слюнных желез-новообразование с непредсказуемым прогнозом, то есть может метастазировать (Т.А.Белоус, 1982).
Высокодифференцированная мукоэпидермоидная опухоль бронхов, по мнению И.Г.Ольховской (1982); J. Mullins и соавт.(1979); H. Wellons и соавт.(1976)-доброкачественное новообразование. Другие исследователи считают, что высокодифференцированная мукоэпидермоидная опухоль иногда может давать метастазы не только в региональные лимфатические узлы, но и в отдаленные органы, то есть является высокодифференцированным раком (И.В.Двораковская, 1979; H. Spencer, 1979). В последнее время мукоэпидермоидную опухоль большинство исследователей обозначают как мукоэпидермоидный рак, подразделяя его на две группы опухолей: с низкой и высокой степенью злокачественности (H. Leonardi и соавт., 1978; G.Bonnaud и соавт., 1979; P. Klacsmann и соавт., 1979; R. Breyer и соавт., 1980 и др.).
Интерес представляет попытка некоторых исследователей (И.В.Двораковская, 1979; P. Klacsmann и соавт., 1979) выявить макро- и микроскопические различия между высоко- и низкодифференцированными вариантами этой опухоли. Высокодифференцированный мукоэпидермоидный рак обычно pастет в виде экзофита (в просвет бронха) с выраженным слизеобразованием, с преобладанием железистых (бокаловидных) клеток. Низкодифференцированный вариант характеризуется чаще эндофитным ростом, отчетливым преобладанием эпидермоидного компонента за счет большого количества базалоидных клеток.В метастазах выявляют и эпидермоидный, и железистый компоненты, однако некоторые исследователи отмечают, что метастазирует в основном плоскоклеточный компонент различной степени дифференцировки. Цитологическая характеристика. Цитологически дифференцировать мукоэпидермоидный рак от умеренно дифференцированного бронхогенного рака практически невозможно.При исследовании отпечатков с биоптата опухоль можно распознать, если цитологическая картина имеет следующие особенности: элементы базального и реже шиповатого слоя эпидермиса формируют довольно массивные скопления, присутствуют слизьсекретирующие опухолевые клетки типа цилиндрических, элементы с железистой дифференцировкой встречаются также в виде отдельных клеток, клеточных групп и железистоподобных структур. Размеры и форма железистых клеток существенно варьирует в зависимости от количества слизи в цитоплазме. В мазках иногда обнаруживаются группы своеобразных опухолевых клеток с вакуолизированной или пенистой цитоплазмой, наличие которых чрезвычайно характерно для мукоэпидермоидного рака.
Ультраструктура. Первый тип клеток мукоэпидермоидной опухоли представлен группами слизеобразующих клеток, формирующих железистые щели, в просвет которых обращены микроворсинки. В цитоплазме содержится большое количество секреторных вакуолей, отграниченных мембраной и заполненных светлым однородным веществом. Вакуоли как бы ориентированы в направлении просвета. Слизьсекретирующие клетки имеют хорошо выраженный комплекс Гольджи и профили шероховатого эндоплазматического ретикулума, но тонофибриллы отсутствуют.Второй тип клеток характеризуется признаками плоскоэпителиальной дифференцировки: клетки крупные, с отчетливой цитоплазмой и многочисленными тонофибриллами в виде пучков; видны также межклеточные мостики и десмосомы. Признаки кератинизации в этих элементах не обнаруживаются.
Иногда встречаются небольшие компактные скопления мелких непродуцирующих слизь клеток, формирующих узкие щели. В просвете щелей выбухают единичные мелкие цитоплазматические выросты. В цитоплазме много митохондрий, лизосом и крупных, окруженных мембраной гранул до 200 нм в диаметре с гомогенной сердцевиной. Между мембраной и сердцевиной виден пояс просветления. В цитоплазме рассеяны мелкие пучки тонофибрилл, а между клетками, в зоне их контакта, обнаруживаются десмосомы. Клетки миоэпителия обычно отсутствуют.Возможно, опухоль возникает из низкодифференцированного эпителия бронхов, способного формировать и плоскоклеточные и слизепродуцирующие элементы (И.В.Двораковская, 1979). Но, более вероятно, гистогенез связан с клеточными элементами протоков секреторных желез или эпителием междольковых протоков, в которых отсутствует миоэпителий (Н.Т.Райхлин и соавт.,1981; Т.А.Белоус, 1982).
3.3. ПЛЕОМОРФНАЯ АДЕНОМА
Поражение слюнной железы плеоморфной аденомой (смешанной опухолью) впервые описал Minssen в 1874 г. Заболевание характеризуется в целом благоприятным прогнозом. В связи с относительной редкостью этого варианта опухоли особенности его недостаточного глубоко изучены. Остается сомнительным вопрос о существовании злокачественных форм плеоморфной аденомы (D. Gullino, 1970; F. Vadill-Bricend и соавт., 1970; H. Spencer, 1979). Можно считать, что разногласия происходят в связи с диагностическими ошибками: за аденому принимают другие дизонтогенетические опухоли, в частности карциносаркому или мукоэпидермоидную опухоль.
Гистологическая характеристика. Плеоморфная аденома бронхов по строению аналогична плеоморфной аденоме слюнной железы. Опухоль имеет пестрое микроскопическое строение: разрастания плоского эпителия с признаками ороговения, ячейки из мелких с гомогенной цитоплазмой клеток (миоэпителиальные), обилие структур с двуядерной эпителиальной выстилкой (имитация протоков), железистоподобные структуры из светлых, богатых гликогеном клеток (цитоплазма их содержит секреторные гранулы), и, наконец, миксоматозные, богатые мукополисахаридами участки в строме с наличием в ней хондроидных и хондроматозных включений.
Опухолевые элементы располагаются то в плотной фиброзной ткани, то в миксоидных или хондроидных участках, то среди веретенообразных клеток, сгруппированных в переплетающиеся пучки. Специфичными для плеоморфной аденомы считаются участки ослизнения, богатые мукополисахаридами с отрицательной реакцией на альциановый голубой и муцикармин.
Слизистая оболочка бронха обычно не изъязвляется. Опухолевые ячейки, трубочки и железы располагаются в толще стенки бронха, распространяясь за пределы хрящевых пластинок. Деструкции хряща и инвазия в легочную ткань не наблюдаются.
Ультраструктура. При электронной микроскопии выявляются секреторные железистые клетки, элементы плоского эпителия, большое количество миоэпителиальных клеток и мезенхимальные элементы стромы.
Миоэпителиальные клетки располагаются группами вокруг щелей с аморфным содержимым. Содержание миофиламентов может быть в значительном количестве, тогда они в виде продольных пучков оттесняют ядро к периферии. Органелл при большом количестве миофиламентов мало. Базальная мембрана и десмосомы отчетливо определяются. Характерно, что в зоне скопления миоэпителия межклеточное вещество имеет нежно-фибриллярный рисунок.
Элементы плоского эпителия-с различной степенью дифференцировки. В некоторых из них отмечается обилие тонофибрилл, отчетливые десмосомы, много рибосом. Преобладают клетки с отчетливой плоскоэпителиальной дифференцировкой. Железистые клетки имеют крупные ядра, хорошо развитый шероховатый эндоплазматический ретикулум с различным количеством секреторных вакуолей, отграниченных мембранами. В целом, и в плеоморфной аденоме и в мукоэпидермоидной опухоли плоскоклеточные и железистые элементы имеют сходную ультраструктурную организацию. Однако в аденоме есть типичные соединительнотканные и хрящевые клеточные элементы.
Гистогенез «смешанной» опухоли, а также возможность ее трансформации в рак, как правило, связаны с эпителием и миоэпителием протоков (резервные клетки), а изменения в строме-результат воздействия «секрета» миоэпителия (И.В.Двораковская, 1979; Н.Т.Райхлин и соавт., 1981; Т.А.Белоус, 1982).
3.4. ЦИСТАДЕНОМА
Цистаденома бронхиальных желез-истинно доброкачественная опухоль, которую иногда ошибочно диагностируют как мукоэпидермоидный рак или высокодифференцированную бронхогенную аденокарциному. Подобная опухоль бронхов известна давно, но впервые ее выделили как самостоятельную нозологическую единицу D. Kroe и J. Pitocock (1967). В дальнейшем цистаденома бронхов была описана рядом авторов (И.В.Двораковская,1979; И.Г.Ольховская,1982; L. Brethner, 1976).
Опухоль растет в виде полипа в просвет бронха, эпителий которого, однако, не изъязвляется. Базальные отделы опухоли четко отграничены, некоторые комплексы цистаденомы находятся в контакте с бронхиальными железами, но за пределы хрящевых пластинок опухоль не распространяется.
Гистологическая характеристика. Опухоль состоит из железистых трубок и полостей, образованных цилиндрическим и уплощенным кубическим эпителием. Клетки с умеренно гиперхромными ядрами располагаются в базальных отделах, митозы отсутствуют. Цитоплазма клеток отчетливая, гомогенная, содержит слизь. Некоторые опухолевые элементы со светлой пустой цитоплазмой, что придает им сходство с бокаловидными клетками. Полости компактно расположены, неправильной формы, в просветах определяются слизистые массы, в некоторых встречается слущенный дистрофический эпителий с мелкозернистой или вакуолизированной цитоплазмой. Между полостями-соединительнотканные прослойки, нередко с явлениями миксоматоза. Можно встретить участки ослизнения стромы в результате нарушения целостности некоторых кист.
Своеобразный вариант цистаденомы, описанный H.Spencer (1979) и характеризующийся папиллярными структурами, иногда ошибочно диагностируют как бронхиолоальвеолярный рак.
Ультраструктура. Опухолевые клетки цистаденомы обнаруживают ультраструктурное сходство с мукоцитами бронхиальных желез (P.Pitchett и B. Key, 1978), в цитоплазме их содержится большое количество секреторных гранул, ядро оттеснено к основанию.Основываясь на ультраструктурной характеристике опухолевых клеток, гистогенез цистаденомы следует связывать с элементами ацинусов слизистых бронхиальных желез.
3.5. АЦИНОЗНОКЛЕТОЧНАЯ ОПУХОЛЬ
Ацинозноклеточная опухоль — редко встречающееся новообразование, которое описывали раньше как аденоматоидную бронхиальную опухоль (L.Weiss и M. Ingram, 1961) или включали в группу светлоклеточных новообразований легких (A. Liebow и B. Castleman, 1963). Более подробно морфологическое строение ацинозноклеточной опухоли бронхов описали R.Fechner и cоавт.(1972); D. Katz и соавт.(1976), которые подчеркнули, что она имеет аналог среди новообразований слюнной железы.
Гистологическая характеристика. Опухоль состоит из мономорфных клеток с просветленной мелкозернистой цитоплазмой, сходных с серозными клетками ацинусов. Эти элементы формируют солидно-альвеолярные скопления, тяжи и криброзные структуры. Иногда опухоль образуется мелкими клетками с «темной», гомогенной цитоплазмой и довольно гиперхромными ядрами, однако патологические митозы не встречаются. Цитоплазма опухолевых клеток содержит ШИК-положительные включения, но слизь и липиды в ней отсутствуют.
Ультраструктура. Преимущественно в темных клетках можно обнаружить ШИК-положительные гранулы 600-800 нм со светлым широким ободком. В клетках карциноида нейросекреторные гранулы мельче: до 150 нм. Ацинозноклеточная опухоль гистогенетически связана с элементами серозных бронхиальных желез, а именно с эпителиальными и миоэпителиальными клетками протоков (резервные клетки).Описанные в литературе ацинозноклеточные опухоли бронхов рассматриваются как доброкачественные новообразования с местнодеструирующим ростом. Однако ацинозноклеточная опухоль слюнной железы имеет злокачественный аналог-ацинозноклеточный рак (Г.А.Галил-Оглы с соавт.,1973).
3.6. ОНКОЦИТАРНАЯ (ОКСИФИЛЬНАЯ) АДЕНОМА
Онкоцитома — доброкачественная опухоль из эпителия бронхиальных желез. Под термином «онкоцитома» многие авторы описывают не только онкоцитарную аденому, но и другие светлоклеточные опухоли легкого, в частности, онкоцитарный карциноид . Различия в группе светлоклеточных опухолей легкого, как справедливо пишет P. Bock и соавт. (1977), более отчетливо видны при исследовании на ультраструктурном уровне.
Подробная характеристика онкоцитарной аденомы бронхиальных желез дана только в единичных работах (A. Santos-Briz и соавт., 1977; H.Spencer, 1979; A. Warter и соавт.,1981). Эти авторы отмечают, что данная опухоль имеет свой аналог среди новообразований слюнных желез, описанный рядом исследователей ( Т.А.Белоус, 1982; К. Шамунгаматанам и Л.Г. Собин, 1982; B. Тandler и соавт., 1970).
Гистологическая характеристика. Опухоль состоит из крупных светлых клеток с оксифильной, иногда мелкозернистой, цитоплазмой и центрально расположенными довольно крупными умеренно гиперхромными ядрами, причем митозы не обнаруживаются. Клетки располагаются компактно, образуют крупные ячейки, которые разделены соединительнотканными прослойками, но иногда могут формировать железистоподобные и протоковые структуры с образованием папиллярных выростов. Некоторые ячейки представлены клетками со светлой пустой цитоплазмой, так что картина напоминает метастаз гипернефроидного рака.Цитоплазма содержит ШИК-положительные включения и, иногда, слизь (муцикармин).
Ультраструктура. Характерная черта ультраструктурной организации клеток-обилие «набухших» плеоморфных митохондрий с разрушенными кристами, других органелл мало, так как клетка заполнена митохондриями почти полностью (Н.Т.Райхлин и соавт.,1981; P. Bock и соавт., 1977; A. Warter и соавт., 1981). Нейросекреторные гранулы, свойственные клеткам морфологически сходного онкоцитарного карциноида, в опухолевых элементах онкоцитарной аденомы отсутствуют.
Эта опухоль гистогенетически связана с эпителием бронхиальных желез, содержащих онкоциты и в протоках, и в ацинусах (K. Matsuba и cоавт., 1972).
3.7. АДЕНОЛИМФОМА (ОПУХОЛЬ УОРТИНА)
Сосочковую cystoadenoma lymphomatosum впервые описали немецкие морфологи Albrecht и Arzt в 1910 г. В 1929 г. А.С.Уортин (A.S.Warthin) представил 2 наблюдения этой опухоли и выделил ее как отдельную нозологическую форму. С тех пор аденолимфому стали выявлять значительно чаще. В последние годы опухоль Уортина считается обычной доброкачественной опухолью, которая поражает чаще всего слюнные железы (8-10% новообразований этой локализации). Значительно реже опухоль возникает из других слюнных желез и очень редко в слизистой оболочке неба, щеки, языка, гортаноглотки.
Поражение легкого считается казуистическим, однако истинная частота этого заболевания, по-видимому, недооценивается и в некоторых случаях может протекать под маской других новообразований. Описано сочетание рака легкого с множественными очагами опухоли Уортина. Разработана методика выявления аденолимфомы при сцинтиграфии с использованием карбогидратного антигена CA 19-9, меченного иодом-131. Очаги периферического рака этот онкомаркер не накапливают (T. Kazumoto et al.,1991). Аденолимфома достоверно чаще втречается у курильщиков сигарет (S.P. Ebbs, A. J. Webb, 1986; C. A. Kotwall, 1992).Хотя опухоль считается доброкачественной, могут наблюдаться рецидивы.
Гистологическая характеристика. Аденолимфома имеет особую структуру, которая довольно легко распознается на светооптическом уровне. Определяются характерные кисты, выстланные онкоцитами или солидные гнезда различных размеров, разделенные лимфоидными инфильтратами. Часто имеется фиброз стромы, некрозы и метаплазия эпителия бронхиальных желез, что может симулировать плоскоклеточный или мукоэпидермоидный рак.
Нередко определяются сосочковые структуры, которые пролабируют в просвет бронха. Кистозные пространства выстланы эозинофильным эпителием, что затрудняет дифференциальную диагностику с онкоцитарной аденомой. Некоторые авторы сомневаются в опухолевой природе поражения, так как процесс больше походит на онкоцитарную гиперплазию (I.Friedmann, 1953; A. P. Griffiths, P. Dekker, 1991). Эпителий обычно двухслойный, причем внутренние клетки высокие цилиндрические с обильной цитоплазмой. Редко встречаются бокаловидные клетки со слизистой секрецией или группы сальных клеток. Степень образования сосочков, кист и количество лимфоидной ткани в этих опухолях весьма вариабельны.
Клетки опухоли выделяют онкомаркеры РЭА и СА 19-9 и накапливают свободные антигены в просвете кист. Отмечается положительная окраска на CD3 (T-клеточный связанный антиген) и L 26 (В-клеточный связанный антиген). При проведении иммуногистохимического анализа необходимо учитывать особенности клинической ситуации.
Аденолимфома-доброкачественная опухоль, состоящая из железистых и кистозных структур, иногда с сосочковыми образованиям, выстланных характерным эозинофильным эпителием. Строма содержит различные количества лимфоидной ткани с фолликулами.
3.8. БРОНХОГЕННЫЙ РАК И ОПУХОЛИ БРОHХИАЛЬHЫХ ЖЕЛЕЗ: ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Цистоаденому, лимфоаденому, «смешанную» и мукоэпидермоидную опухоли необходимо дифференцировать с теми формами рака легкого, которые представляются в виде экзофитно растущих образований. Обычно речь идет о высокодифференцированном плоскоклеточном и железистом, а также аденосквамозном раке. В дифференциальной диагностике цистоаденом и высокодифференцированной аденокарциномы в пользу последней говорит совокупность морфологических признаков: наличие инфильтративного роста ( при гистологическом исследовании), умеренно выраженный полиморфизм ядер и наличие атипических митозов, формирование солидных ячеек и слабо выраженная продукция слизи.
Высокодифференцированный плоскоклеточный рак отличается от «смешанной» опухоли по следующим признакам: отсутствием хондроидных включений и структур, имитирующих протоковые образования (основной эпителиальный компонент «смешанной» опухоли), а также отсутствием, как это видно при электронно-микроскопическом исследовании, разрастаний миоэпителиальных клеточных элементов. Дифференциальная диагностика мукоэпидермоидной опухоли и аденосквамозного рака затруднительна. Однако есть ряд признаков, на основании которых можно высказаться в пользу аденосквамозного рака. Это отсутствие полостей, образованных плоским эпителием с наличием слизьсодержащих клеток; более мономорфный состав железистого компонента (отсутствуют, в частности, «бокаловидные»клетки, характерные для мукоэпидермоидной опухоли); слабо выраженная способность к продукции слизи клетками железистого компонента.
Комплексная морфологическая диагностика «светлоклеточных» опухолей легких позволила прийти к заключению, что эта группа новообразований представлена различными по гистогенезу и клиническому течению патологических процессов, которые на светооптическом уровне (гематоксилин-эозин) трудно различимы. Характерная черта онкоцитарной аденомы (обилие «плеоморфных» митохондрий) сходна с онкоцитарным карциноидом, однако в клетках последнего определяются нейросекреторные гранулы.
Встречаются также формы рака легкого (светлоклеточный, плоскоклеточный, аденокарцинома), которые представлены компактно расположенными четко контурированными, сравнительно мономорфными клетками со «светлой», слегка мелкозернистой цитоплазмой. Сказанное относится иногда и к солитарному метастазу рака почки.Опухолевые элементы «светлоклеточного» рака содержат большое количество гликогена, но в отличие от онкоцитарной аденомы в них нет «набухших» митохондрий; не обнаружено в клетках каких-либо признаков плоскоэпителиальной или железистой дифференцировок. На отдельных участках все же можно отметить полиморфизм клеток, что не характерно для онкоцитарной аденомы.
Диагностика плоскоклеточного рака из «светлых» клеток основана на обнаружении в единичных его клетках кератина (метод Крейберга), а главное, ультраструктурных признаков плоскоэпителиальной дифференцировки.
Распознавание бронхогенной аденокарциномы солидного строения из «светлых» клеток будет достоверным, если в них можно выявить признаки секреции слизи (редко), хотя при электронномикроскопическом исследовании более отчетливо видны признаки железистой дифференцировки (внутриклеточные канальцы, наличие ворсинок и др.)
Метастаз гипернефроидного рака характеризуется наличием в цитоплазме клеток липидов (однако это не постоянный признак) и ультраструктурным сходством с элементами проксимального отдела нефрона ( в частности, присутствием «щеточной» каемки).
Глава 4. Карциноидные опухоли легкого
Карциноиды — опухоли низкой степени злокачественности, развивающиеся из элементов выстилки дыхательных путей или бронхиальных желез и имеющие признаки нейроэндокринной дифференцировки. Эти образования встречаются с одинаковой частотой у лиц обоего пола в молодом и среднем возрасте.
4.1. ТИПИЧНЫЕ КАРЦИНОИДЫ
Карциноиды составляют не более 1-2% всех опухолей нижних дыхательных путей. Как и для других образований, относящихся к опухолям APUD-системы, для карциноидов легких характерна продукция биологически активных веществ, таких как 5-окситриптамин (серотонин), АКТГ, меланоцитостимулирующий гормон, инсулин, глюкагон, катехоламины, кинины.
Термин впервые ввел Oberndorfer в 1907 году . Он использовал при описании необычных новообразований кишечника. В последующем описаны карциноиды дыхательных путей, в том числе гортани и трахеи [ Goldman N.C. с соавт.,1969, Casolino D. с соавт.,1990, Marzuoli L. с соавт., 1993]. За последние годы в связи с развитием иммуногистохимических методов исследования, расширения спектра морфологических онкомаркеров и совршенствования методов электронной микроскопии, количество сообщений о карциноидах ЛОР-органов стало быстро нарастать. К 1989 г. на 8469 случаев рака гортани описано 56 карциноидов [Wenig B.M. с соавт., 1989] Эмбриологически первичная передняя кишка дает начало гортани, трахее, бронхам и желудку. Мезогастральный отдел — кишечнику, аппендиксу, слепой кишке. Карциноиды, резвивающиеся из передней кишки, чаще всего имеют атипичную структуру.
Описаны также варианты гистологического строения карциноидов: муцинопродуцирующий карциноид, онкоцитарный карциноид, меланоцитарный карциноид.
Меланоцитарный карциноид трахеи. В мировой литератруое ранее описаны два наблюдения пигментосодержащих карциноидов бронха, своеобразие которых заключалаось в том, что наряду с типичными структурами карциноида в новообразованиях содержался меланин. Наличие двух типов дифференцировки в обеих случаях подтверждено иммуногистохимическим и электронномикроскопическим методами. В связи с исключительной редкостью этой патологии трахеи приводим собственное наблюдение пигментированной опухоли трахеи [Cebelin M. с соавт.,1980; Ferraro S. с соавт,1987]. Больной 51 года обследован в связи с нарастающими признаками стеноза трахеи. Рентгенологически в начальном отделе дыхательной трубки выявлена тень опухоли неправильной полуокруглой формы, 1,5 см в диаметре, ниже которой видно ее продолжение в виде площадки протяженностью 7 мм и толщиной 4 мм с четкими неровными контурами. На 2 см ниже описанного узла имелась тень второй опухоли 1,7 см в диаметре, исходящей из передней и правой стенок трахеи. Контур стенок на уровне поражения не просматривался.
При фибротрахеоскопии в области передней стенки на уровне перстневидного хряща обнаружено экзофитное образование темной окраски, покрытое неизмененной слизистой оболочкой, в виде сросшихся узлов диаметром 0,8 и 1,5 см. Второе образование, располагавшееся на 3,5 см ниже первого, имело вид бугристой опухоли, перекрывающей просвет трахеи. 28.07.86 г. произведена комбинированная резекция передней стенки шейного отдела трахеи и подскладочного отдела гортани.
Гистологически опухоль представлена полями округлых, довольно полиморфных, небольших по размеру клеток, окруженных скудной стромой с сосудами синусоидного типа. Местами формируются нечетко контурирующиеся альвеолярные и розеткообразные структуры. Большая часть клеток, особенно по периферии альвеол, содержат мелкие пылевидные частицы коричневого пигмента, дающего отрицательную окраску на железо. Отмечается выраженный инфильтрирующий рост опухоли с прорастанием мембранозной части трахеи. В поверхностных отделах новообразования среди опухолевых клеток и воспалительных элементов встречались остатки трахеиальных желез.
При элестронной микроскопии видны комплексы небольших полигональных клеток, разделенные неширокими прослойками коллагеновых волокон. Внутри комплексов клетки раположены компактно, однако специфические контакты отсутствуют. Ядра клеток круглоовальные, с неглубокими инвагинациями. Хроматин крупноглыбчатый, часто встречаются гипертрофированные ядрышки. Цитоплазма клеток хорошо развита, содержит множественные, нередко гипертрофированные и расширенные профили шероховатого эндоплазматического ретикулума; крупные митохондрии, встречаются хорошо развитые комплексы Гольджи. Вокруг последних в отдельных клетках видны скопления секреторных гранул диаметром 40-80 нм, ограниченных однослойной мембраной, со светлым «гало» и электронноплотным центром. Одновременно в части клеток обнаруживаются скопления крупных плотных гранул диаметром 800 нм с нечеткой однослойной мембраной и неоднородным электронноплотным содержимым — меланосомы. Количество гранул обоих типов в разных клетках варьирует, встречаются клетки, содержащие гранулы только одного типа, и клетки, свободные от гранул.
Окончательный диагноз с учетом гистологического и электронномикроскопического исследований: злокачественный меланоцитарный карциноид с мультифокальным ростом. Через 10 лет после операции и курса лучевой терапии больной жалоб не предъявляет, рецидива и метастазов не обнаружено. Таким образом, в период эмбрионального развития во время роста гортанно-трахеального зачатка меланобласты могут отрываться от первичного эпителия ротоглотки в случае, если миграция нейроэктодермальных элементов происходит до формирования примордиальной дыхательной трубки. Еще большую редкость представляют опухоли, в которых меланоцитарная дифференцировка сочетается с нейроэндокринной. Несмотря на продукцию сходных биогенных аминов, меланоциты и нейроэндокринные клетки значительно различаются по многим признакам. Наблюдение пигментосодержащих карциноидов представляет большой интерес вплане дискуссии о происхождении карциноидных поражений дыхательных путей.
Гистологическая характеристика. Большая часть карциноидных опухолей легких однотипна по строению: опухоль состоит из мономорфных четко контурированных клеток — округлых или полигональных, с мелкозернистой интенсивно окрашенной эозином цитоплазмой и гиперхромным ядром с равномерным распределением хроматина. Клетки образуют альвеолы, трабекулярные структуры, тяжи и ячейки, реже участки солидного строения, а иногда формируют «розетки» (И.В.Двораковская, 1979; И.Г.Ольховская, 1982). В цитоплазме клеток иногда выявляются двоякопреломляющие липиды и во всех случаях при окраске по методу Гримелиуса — аргирофильные включения, соответствующие нейросекреторным гранулам, видимым при электронномикроскопическом исследовании.
Хотя, по мнению многих авторов, карциноидные опухоли примыкают к мелкоклеточному раку легкого по гистогенезу, считалось, что они существенно отличаются от него по биологическим свойствам и прогнозу. Однако прежние установки на доброкачественность течения заболевания за последние годы изменились.
Тщательное изучение карциноидных новообразований легкого позволило выявить среди них опухоли с явно злокачественной динамикой роста. Оказалось, что опухоли нейроэндокринной системы образуют широкий спектр постепенно увеличивающейся злокачественности от медленно растущих отграниченных или местнодеструирующих образований до агрессивно растущих и метастазирущих, по прогнозу приближающихся к мелкоклеточному раку. Соответственно клиницисты вынуждены были изменить складывавшиеся десятилетиями взгляды на лечение этой опухоли. В свете вышесказанного проблема морфологической дифференциальной диагностики приобрела большую актуальность. Учет особенностей структуры карциноида дает возможность с достаточной точностью предсказывать прогноз.
4.2. АТИПИЧНЫЕ КАРЦИНОИДЫ
В последней гистологической классификации ВОЗ новое понятие «атипичные карциноиды» не выделяется. Но в современной литературе этим термином широко пользуются. Предложившие его в 1972 г. Arrigoni и соавт. разработали морфологические дифференциальнодиагностические критерии данного новообразования.
Атипичные карциноиды — звено, соединяющее доброкачественные и злокачественные нейроэндокринные опухоли одинакового генеза. Они составляют около 25% образований карциноидного типа. Макроскопически существенных различий между типичными и атипичными карциноидами не существует, однако последние несколько больше по размерам. Диаметр их часто превышает 3 см. Опухоли хорошо отграничены, имеют плотную консистенцию и серо-желтую окраску.
Микроскопическая структура атипических карциноидов значительно варьирует не только у разных больных, но и в пределах одной опухоли. Опухоль напоминает типичные карциноиды, однако клетки более крупные, более полиморфные, с частыми митозами. Могут встречаться многоядерные опухолевые клетки. Иногда определяются розетки или палисадообразные структуры, трабекулы в виде лент из вытянутых клеток. Характерны участки некрозов. Атипичные карциноиды часто относят к крупноклеточному и реже к мелкоклеточному недифференцированному раку.
Наиболее трудна дифференциальная диагностика атипичного карциноида с мелкоклеточным раком при выявлении веретеноклеточного компонента. Следует учитывать, что клетки карциноида имеют обильную цитоплазму, менее отчетливые изменения ядер и меньшее количество митозов. Заслуживает внимания метод определения содержания ДНК в опухоли с целью дифференциальной диагностики карциноидов (L. DeCaro и соавт.,1983).
Ультраструктура. При электронной микроскопии почти во всех клетках карциноида выявляются плотные нейросекреторные гранулы диаметром в среднем 130 нм. В атипичных карциноидах они не так многочисленны.
Кроме светооптической и ультраструктурной характеристики карциноидов, следует учитывать и другие биологические признаки.
Следует учитывать также наличие лимфогенных и гематогенных метастазов, которые при типичных карциноидах встречаются в 5,6 % случаев, при атипичных — в 70% случаев. Карциноидный синдром встречается в 2-7% наблюдений и характерен для распространенных форм карциноидов с отдаленными метастазами, особенно в печени (C. Ricci et al.,1972). Нередко повышенный уровень серотонина и гормональная активность опухоли не проявляются клинически. N.Okike и соавт. (1978) предложили тест на экскрецию 5-оксииндолилуксусной кислоты считать показателем отдаленного метастазирования.
Глава 5. Опухоли плевры
Серозные оболочки (плевра, перикард, брюшина, оболочки яичка, маточных труб) состоят из слоя эпителиальных клеток — мезотелия, расположенного на базальной мембране и пластинке рыхлой соединительной ткани. Первичные опухоли из мезотелиальной выстилки серозных оболочек обозначают как мезотелиомы. Наиболее часто это новообразование развивается в плевре и брюшине, реже в перикарде, оболочке яичка и в области маточных труб (аденоматоидная опухоль).
Первое сообщение об опухоли плевры встречается в 1767 г. у Lietand (2 наблюдения на 3000 аутопсий). Однако первое достоверное гистологическое описание дано E. Wagner в 1870 г. Некоторые морфологи долго не признавали возможность первичного поражения плевры, например, H. Robertson (1924) расценил описанную им эндотелиому плевры как метастаз из невыявленного первичного очага. Наиболее полное описание опухолей плевры и классификацию их гистологических вариантов сделали P. Klemperer и C. Robin (1931); они выделили доброкачественный вариант мезотелиомы и подразделили ее на эпителиальную и саркоматозную формы. A. Maximov (1927); A. Stout и M. Murray (1942) изучили гистогенез опухоли методом культуры тканей и доказали, что мезотелий в культуре тканей может давать рост эпителиальным и фибробластическим элементам.
В 1943 г. H. Glatzel отметил повышение числа новообразований плевры в приморских городах. Позднее была обнаружена связь злокачественной мезотелиомы с асбестозом (F. Leicher, 1954). J. Wagner и соавт. (1974) доказали, что развитие диффузной мезотелиомы связано с продолжительным воздействием асбеста (кроцидолита). В настоящее время канцерогенное воздействие асбеста ни у кого не вызывает сомнений. Немаловажная роль в развитии опухоли принадлежит также плевральным спайкам.По гистологической структуре различают мезотелиомы монофазные и бифазные. В бифазной мезотелиоме отмечают разнообразное сочетание эпителиального и фиброзного компонентов. Последний представлен веретенообразными клетками и напоминает фиброму или фибросаркому. Эпителиальный компонент образует различные структуры: железистоподобные, тубулярные, папиллярные, смешанные. По клиническому течению выделяют доброкачественную форму мезотелиомы (локализованную) и злокачественную (как правило, диффузную).
5.1. ВНЕПЛЕВРАЛЬНАЯ СОЛИТАРНАЯ ФИБРОЗНАЯ ОПУХОЛЬ (локализованная мезотелиома)
Солитарная (локализованная) фиброзная опухоль (СФО) обычно возникает из плевры, поэтому ранее называлась локализованной (доброкачественной) мезотелиомой. Впервые она описана в 1870 г. E.Wagner. Довольно долго считали, что она происходит из мезотелиальных клеток (Stout A.P., Murrey M.P.1942). Тем не менее, еще P. Klemperer и C. Robin (1931) выделили доброкачественный вариант мезотелиомы и предположили, что она исходит из субмезотелиальной соединительной ткани. Ряд авторов (К.К.Порошин и соавт.,1981; M. Brisselly и соавт.,1981) придерживались той же точки зрения и предлагали обозначить это новообразование как субплевральную (субмезотелиальную) фиброму и выделяли его из группы мезотелиом.
Терминология. Результаты современных исследований с использованием электронной микроскопии, эксплантации, иммуногистохимических методов довольно твердо указывают на мезенхимальное происхождение СФО, а не эпителиальное или мезотелиальное (Перевощиков А.Г.и др., 1993; England D.M. et al.,1984; Fukunaga M., 1997).
Однако терминологическое разнообразие до сих пор не упорядочено. С одной стороны, некоторые исследователи относят опухоль к обычным фибромам (Hernaudez F.J. et al.,1974; Burrig K.T. et al.,1984). Другие авторы подчеркивают, что почти всегда в СФО обнаруживаются абортивные элементы мезртелиаольной дифференцировки. Они рекомендуют сохранить название «мезотелиома», учитывая особенности роста, характерную клиническую картину и прогноз (Kienzle H.T. et al.,1987$ Liewal F.L. et al.,1989).
А.Г.Перевощиков и др.(1993) пользуются термином «очаговая»(?) фиброзная мезотелиома. Довольно часто встречаются определения «доброкачественная», ограниченная», «локализованная». Анализ результатов лечения не позволяет применять большинство представленных терминов. СФО следует считать нормативным.
За последние годы СФО стали находить в легком, придаточных пазухах носа, средостении, брюшной полости, верхних дыхательных путях, глазнице, щитовидной железе, печени и мягких тканях (4-17). Макроскопически внеплевральная СФО хорошо изолирована от окружающих тканей, но не имеет капсулы. Может инфильтрировать соседние структуры. На разрезе определяется серо-белая и гомогенная, плотная или резиноподобная ткань. Нередко обнаруживаются участки некроза и кровоизлияний.
В отечественной литературе СФО серозных оболочек уделено недостаточно внимания, а изолированные органные поражения не описаны совсем. Наше наблюдение очень поучительно с точки зрения клинической и морфологической дифференциальной диагностики, а также эффективного применения современных методов обследования.
Больной Х.,69 лет (и/б 664/98) 16.02.98 г. поступил в Московскую городскую больницу № 62 с жалобами на сухой кашель, субфебрильную температуру. Заболевание началось 4 месяца назад с «простуды». Обследовался в противотуберкулезном диспансере № 2, специфическое поражение легких не подтверждено. С диагнозом «периферический рак левого легкого» направлен в больницу № 62.
Рентгенологически в заднемедиальных отделах нижней доли обнаружена шаровидная тень до 5 см в диаметре, четко очерченная, относительно гомогенная, нижним полюсом примыкающая к диафрагме. За 3 месяца существенной рентгенологической динамики процесса не отмечено. При компьютерной томографии на фоне умеренного пневмосклероза в 10 сегменте левого легкого выявлен крупнобугристый неоднородный узел с нечеткими контурами, размерами 5,2х4,1 см (плотность образования от +23 до +63 ед. Хаунсфилда). Узел приближается к медиастинальной плевре, но отделен от нее участком тяжистой легочной ткани. Корни сохраняют структуру, левый несколько расширен за счет мелких бронхопульмональных лимфатических узлов. Средостение — без особенностей. При фибробронхоскопии, эзофагодуоденоскопии, ирригоскопии и абдоминальной эхографии патологии не обнаружено. Онкомаркеры плазмы крови: РЭА — 4,6 нг/мл, СА 125 — 19,0 ед/мл, CYFRA 21-1 — 1-1,8 нг/мл.
Сопутствующая патология: атеросклеротический коронарокардиосклероз с недостаточностью кровообращения, аденома предстательной железы I-II ст., язвенная болезнь 12-перстной кишки. Результаты комплексного обследования указывали на неэпителиальное периферическое образование в 10 сегменте левого легкого, но нельзя было исключить саркому и в еще меньшей степени рак В качестве заключительного этапа диагностики 17.03.98 г. больному выполнена торакоскопия слева.
Патологии висцеральной, париетальной, диафрагмальной и медиастинальной плевры не обнаружено. Сразу же произведена торакотомия по 5 межреберью слева. Плотная опухоль до 6 см в диаметре располагалась в 10 сегменте легкого. Плевра над ней не изменена. Связи образования с медиастинальной плеврой также не выявлено. При цитологическом исследовании пунктата опухоли обнаружены лимфоидные элементы без признаков злокачественности . С помощью аппарата УКЛ-40 выполнена клиновидная резекция легкого. Послеоперационный период протекал без осложнений.
При исследовании удаленного препарата (дать подробное описание гистологической картины) № 722/6791-6804 (консультация проф. И.Г.Ольховской) — СФО нижней доли правого легкого.
Больной обследован в декабре 1998 г. рецидива опухоли не выявлено.
Таким образом, использование современных диагностических методов (компьютерная томография, исследование онкомаркеров, торакоскопия, цитологическая пункция) позволило усомниться в стандартном диагнозе «периферический рак легкого» и выбрать правильную тактику лечения, а также адекватный объем операции.
Фиброзная опухоль (локализованная мезотелиома, локализованная фиброма плевры, субмезотелиальная фиброма) представляет собой локализованное образование в виде узла, исходящее, как правило, из висцеральной и, значительно реже, из париетальной плевры. Новообразование встречается в 3 — 4 раза реже, чем злокачественные мезотелиомы. Возраст больных колеблется от 50 до 70 лет. Поражение плевры наблюдается преимущественно у женщин.
Диагностика СФО основывается на данных КТ. Однако следует учитывать, что этот метод даже в сочетании с ангиографией может привести к тяжелым диагностическим ошибкам (Kienzle H.,1987). Цитологическая чрескожная пункция обычно не проясняет диагноз, подтверждение которого возможно только при исследовании всего удаленного препарата. При внутриплевральных СФО точный диагноз удается поставить до операции с помощью торакоскопии. Этот метод предложен еще в 70-х гг. и в настоящее время является ведущим в определении взаимоотношений опухоли и плевры (Харченко В.П., Кузьмин И.В.,1994; Bonsky S.F.,1978; Liewald F. Et al.,1989).
S.A.Yousem с соавт. (1988) описали 3 случая (2 — у женщин) внутрилегочной СФО у больных 55-82 лет. У одного из них нельзя было исключить эндофитный рост опухоли из плевры, но у двух СФО располагалась глубоко в легочной паренхиме. Внеплевральное поражение легкого описано также M. Van de Rijin с соавт. (1994).
Умозрительно можно представить два объяснения внутрилегочного роста СФО: 1) предсуществование межсегментарного отростка субплевральной мезенхимы или эктопические гнезда субмезотелиальной ткани в паренхиме легкого, включая инвагинацию висцеральной плевры; 2) рост СФО из фибробластов легочной паренхимы.
Не исключено, что ранее описанные «фиброаденомы» легкого имеют то же происхождение.
Веретенноклеточные элементы обрастают альвеолярный эпителий, образуя своеобразные гистологические структуры (Klemperer B., Rabin C.B.,1931; Foster E.A. et al. 1960; Dalton W.T. et al.,1960). Таким образом, в отличие от СФО, связанных c плеврой, по периферии очага могут встречаться легочные структуры: альвеолы, пневмоциты, мелкие бронхиолы. В таких случаях опухоль опухоль можно легко принять за карциносаркому или аденокарциному с веретеноклеточной метаплазией. В случае, если обнаруживаются более зренлые мезенхимальные элементы (хрящи, жир), образование может быть расценено как гамартома.
Иногда затруднения с диагнозом возникают при плазмоклеточных гранулемах в хронических легочных инфильтратах, которые отличаются насыщением плазмоцитами, гистиоцитами и ксантомными клетками. Наиболее часто в СФО выявляют виментин и CD34 (антиген предшественников гематопоэтических клеток).
В отдельных участках могут определяться мышечные маркеры и десмин, в редких случаях нейронспецифическая енолаза и leu 7. Клетки СФО не окрашиваются на цитокератины. При электронной микроскопии элементы СФО напоминают незрелые элементы мезенхимы или фибробласты. Клетки содержат веретенообразное или овальное ядро с неправильным контуром, иногда видны мелкие ядрышки. В цитоплазме определяются рибосомы, митохондрии и растянутый эндоплазматический ретикулум. Количество органел может широко варьировать, но чаще их мало. На поверхности клеток обычно определяются удлиненные переплетенные отростки цитоплазмы. Вокруг — коллагеновый матрикс.
Поверхностные микроворсинки, десмосомы, тонофиламенты выявить обычно не удается.
Наиболее трудна дифференциальная диагностика с гемангиоперицитомой, опухолями оболочек нервов, фиброзной гистиоцитомой и злокачественной мезотелиомой. Гемангиоперицитома в отдельных участках содержит маркер CD34, что говорит о неполной мышечной дифференцировке. В связи с этим нужно использовать несколько разных методов морфологической диагностики, включая электронную микроскопию. Иногда трудно исключить фибросаркому легкого, которая описана J.G.Guccion в 1972 г. Для этой опухоли характерен рисунок типа «скелета селедки», часто определяются участки некроза и >5 митозов на 10 полей зрения. Но для фибросаркомы не характерны отложения гликогена.
N.Okike et al. (1978) предложил различать два варианта СФО: доброкачественный — плотная инкапсулированная дольчатая опухоль, в кторой редко можно встретить обызвествление, некрозы и кровоизлияния; злокачественный — гомогенная мягкая опухоль с гладкой поверхностью на разрезе, со значительным количеством участков некрозов и геморрагий. Последний подтип СФО гистологически может быть представлен ацинарные и сосочковые структуры, напоминающие фибросаркому. Из 60 больных (37 женщин) у 8 (13,3%) оказался злокачественный вариант СФО, который проявлялся локальными симптомами, прорастанием в грудную стенку и даже деструкцией ребер. Синдром «барабанных пальцев» отмечался только при доброкачественном варианте опухоли. После радикальной операции системные проявления исчезали и возвращались при рецидивировании. Гистологическая структура рецидива могла иметь вполне доброкачественный характер (Utley J.R.,1973; Okike N. Et al.,1978).
Таким образом, прогноз при СФО всегда сомнителен. У 10-15% больных возникает рецидив, поэтому очаг поражения следует удалять полностью. Тем не менее, при внеплевральном поражении органов иногда приходится удалять опухоль путем кускования с хорошими отдаленными результатами (Zukerberg L.R. et al.,1991).
5.2. ЗЛОКАЧЕСТВЕННАЯ МЕЗОТЕЛИОМА
Злокачественная мезотелиома плевры (диффузная мезотелиома, целомический рак, саркоматозная эндотелиома) — опухоль, характеризующаяся диффузным инфильтрирующим ростом. В нашей стране эпидемиологии этого новообразования не уделяется достаточно внимания. Между тем, по литературным данным, заболеваемость злокачественной мезотелиомой в США, где воздействию асбеста на работе подвергаются 7-8 млн. человек, составляет 0,1-0,2 на 100 тысяч жителей, причем брюшина и плевра поражаются одинаково часто.
В последние годы заболеваемость злокачественной мезотелиомой плевры у мужчин в США увеличивается на 13% в год. Опухоль стала чаще развиваться и у женщин. Fraire и соавт. (1988) обращают внимание на учащение диффузной мезотелиомы у детей в 16 странах (80 наблюдений) и связывают это явление с внутриутробным воздействием асбеста и изониазида, а также облучения. Если в целом мезотелиома, как причина смерти, регистрируется в 0,06% случаев, то среди рабочих, связанных с производством полирующих материалов, — в 8,8%, у рабочих асбестовых заводов — в 6,9%, у шахтеров — в 0,19% (Y. McDonald и A. McDonald, 1977). Во Франции с 1976 г. мезотелиому считают профессиональным заболеванием (B. Сaillard и соавт.,1977).
Асбестоз наиболее часто встречается в местах добычи минерала (ЮАР, Турция). Кроцидолит (голубой асбест), основная канцерогенная форма асбеста, вызывает 90% всех злокачественных поражений плевры. Частота асбестоза высока на судоверфях и асбестовых фабриках, где упаковочные работы проводят женщины. В индустриальных странах асбестоз обнаруживают в 0,2-0,7% аутопсий. В США за последние годы отмечено снижение частоты асбестоза благодаря ужесточению федерального трудового законодательства. Однако даже при полном исключении воздействия асбеста, рост заболеваемости мезотелиомами в ближайшие годы будет продолжаться. Латентный период злокачественной мезотелиомы колеблется от 20 до 30 лет. Средний возраст больных 50-70 лет.
В этиологии опухоли немаловажное значение имеют также бериллий, хроническое воспаление, наследственные факторы. У животных доказана роль вирусов.
Патогенез мезотелиомы изучен недостаточно. Считается, что волокна асбеста имеют тропность к серозным оболочкам. Из желудочно-кишечного тракта и бронхов они мигрируют в плевру и брюшину, где могут накапливаться в значительных количествах и служить пусковым механизмом для развития опухоли. Диффузная мезотелиома вовлекает в процесс париетальный и висцеральный листки плевры. Это связано с тем, что ток лимфы направлен в сторону париетальной плевры, клетки опухоли имплантируются в ней, распространяясь постепенно по всей поверхности. Циркуляция лимфы быстро нарушается и она накапливается в плевральной полости.
Макроскопически диффузная мезотелиома может быть представлена сливающимися узлами различного размера, имплантирующими утолщенную висцеральную плевру и выбухающими в плевральную полость. Опухолевые разрастания мягкие, беловатые, с сальным блеском, участками желтоватого или красноватого цвета. В дальнейшем такие же разрастания возникают на париетальной плевре. Опухолевая ткань распространяется также в междолевые щели. Наиболее редко опухоль поражает нижние отделы плевральной полости. В плевральной полости наблюдается скопление серозно-фибринозного или геморрагического экссудата.
Однако чаще опухоль имеет вид плотного инфильтрата, окутывающего в виде футляра все легкое, прорастающего также париетальный листок плевры. Толщина опухолевого инфильтрата колеблется от нескольких миллиметров до 15 см.
Если полость плевры остается полностью или частично свободной от опухолевых масс, то в ней наблюдается скопление экссудата. Плевральная жидкость при мезотелиомах характеризуется высоким содержанием гиалуроновой кислоты (от 0,2 до 0,8 мг/л). Гиалуроновая кислота делает жидкость желеобразной. Однако этот признак характерен не только для мезотелиом, он может наблюдаться в отдельных случаях и при воспалительных процессах, а также при выпоте метастатической природы.Нередко отмечается прорастание мезотелиомы в перикард, средостение, грудную стенку, диафрагму и брюшину. Почти всегда отмечаются метастазы в трахеобронхиальные лимфатические узлы, средостение, плевру противоположного легкого. В 50-70% аутопсий отмечается метастазирование по лимфатическим путям, реже могут наблюдаться гематогенные метастазы в отдаленных органах. Такое распространение опухоли более характерно для саркоматозного типа мезотелиомы. В редких случаях отмечается обызвествление метастазов.В настоящее время используют кодификацию мезотелиомы по стадиям. Она необходима в оценке прогноза и для определения показаний к различным методам лечения (E. G. Butchart et al., 1977).
Стадии диффузной мезотелиомы плевры
I. Опухоль в пределах пораженного легкого (листка плевры) или перикарда.
II. Поражение грудной стенки, органов средостения и/или внутригрудных лимфатических узлов.
III. Поражение диафрагмы, метастазирование в лимфатические узлы вне грудной стенки.
IV. Отдаленные гематогенные метастазы.
Обычно I стадию выявляют у 18% больных, II стадию — у 50%, III — у 28%, IV — у 40% (R.J.Pisаni et al., 1988). Ведущая роль в определении распространенности мезотелиомы принадлежит компьютерной томографии. Уточнить диагноз гистологически не всегда представляется возможным. Нередко в диагностике мезотелиом приходится использовать только клинические данные и результаты цитологического исследования.
Цитологическая характеристика. Точная диагностика мезотелиом при цитологическом исследовании плеврального выпота вызывает значительные трудности. Это объясняется тем, что реактивные изменения мезотелиальных клеток сопровождаются выраженным полиморфизмом, вследствие чего отличить их от опухолевых клеток очень сложно. Кроме того, злокачественные клетки могут отсутствовать в экссудате, не говоря уже о возможности отсутствия выпота. Довольно часто наличие злокачественных клеток в пунктате не вызывает сомнений, но доказать их принадлежность мезотелиоме трудно.
Цитоплазма опухолевых клеток может быть эозинофильной и базофильной, ядра часто имеют вид пузырьков. Ядрышки содержат гранулы. Отмечается полиморфизм мезотелиальных клеток, наличие многоядерных клеточных элементов, гиперхромия ядер. Обнаруживается много клеток, промежуточных между нормальными мезотелиальными и опухолевыми.
G.Pedio и U.Lardolt-Weber (1988) выделяют 8 цитологических признаков злокачественной мезотелиомы:
- однородность клеточной популяции, злокачественные клетки с различной степенью атипии;
- злокачественные клетки разрознены, изолированы или образуют морулоподобные структуры;
- злокачественные клетки часто многоядерные, с выраженными ядрышками;
- формирование между двумя соседними клетками межклеточного пространства, называемого «окном»;
- цитоплазма клеток оптически плотная и ее окраска варьирует от базофильной до эозинофильной;
- феномен «клетка в клетке»: более мелкие клеточные элементы внедряются в более крупные;
- фенестрация цитоплазмы, обусловленная образованием мелких светлых вакуолей по периферии цитоплазмы;
- наличие микроворсинок на поверхности клеток.
Многие цитологи ставят диагноз диффузной мезотелиомы по одному цитологическому признаку при соответствующей клинической и рентгенологической картине. Это приводит к ложноположительным заключениям и снижает точность цитологического исследования.В связи с трудностями цитологической диагностики диффузной мезотелиомы решающее значение принадлежит гистологическому исследованию. Наиболее надежный диагностический метод — торакоскопия с биопсией, которая дает возможность определить тип мезотелиомы и ее распространенность. Менее надежна игловая биопсия. Диагностической торакотомии по возможности следует избегать, так как мезотелиомы склонны к имплантационному метастазированию (R. Edge, S. Choudry, 1978). Имплантация клеток опухоли в области пункционных каналов встречается в 10-20% наблюдений.
Гистологическая характеристика. Строение диффузных мезотелиом разнообразно. Выделяют 4 типа опухоли: эпителиальный (тубуло-папиллярный), фиброзный (саркоматозный, веретеноклеточный), недифференцированный полигональноклеточный и смешанный. Тубулярный вариант представлен трубочками и тяжами из кубических или призматических клеток, расположенных в фиброзной, часто гиалинизированной строме. Папиллярный вариант характеризуется выростами клеточно-волокнистой стромы, покрытыми кубическими или призматическими клетками. Саркоматозный тип состоит из пучков веретенообразных клеток. Ткань содержит незначительное количество щелей, выстланных мезотелием. Иногда опухоль почти полностью представлена структурами, напоминающими фибросаркому, злокачественную шванному или лейомиосаркому. Реже встречается десмопластический вариант новообразования с избыточным количеством коллагена и ростом клеток в виде пластов.
Дифференциальная диагностика наиболее трудна при недифференцированном полигональноклеточном типе мезотелиомы, который очень напоминает бронхиолоальвеолярный рак или метастаз аденокарциномы. Клетки опухоли образуют солидные скопления или гнезда, окруженные фиброзной стромой с выраженной пучковостью и преобладанием коллагеновых волокон.
Смешанный вариант представлен различным сочетанием эпителиального и саркоматозного вариантов мезотелиомы (бифазная мезотелиома).
Дифференциальная диагностика между эпителиальными вариантами мезотелиомы и аденокарциномой представляет значительные трудности. Для различения этих новообразований используют гистохимические окраски. Наиболее информативны нижеследующие три метода:
- Обработка препарата диастазой для удаления гликогена. Остается мукополисахарид, реагирующий с ШИК-реактивом. Мезотелиома дает положительную реакцию до обработки диастазой, но реакция становится отрицательной после удаления гликогена. Аденокарцинома дает положительную ШИК-реакцию в 50% наблюдений до и после обработки диастазой.
- Обработка гиалуронидазой с последующей окраской альциановым голубым. В 30-50% случаев мезотелиома дает положительную реакцию с альциановым синим, но после обработки гиалуронидазой реакция становится отрицательной. При аденокарциноме реакция остается положительной.
- Обработка муцикармином. Нейтральный муцин содержится в 50% наблюдений аденокарциномы, за исключением рака предстательной железы и гипернефроидного рака. Особенно характерно внутриклеточное содержание в виде шариков. При мезотелиоме реакция, как правило, отрицательная.
При иммуногистохимическом исследовании эпителиальный тип мезотелиомы, как и рак молочной железы, дает резко выраженную положительную реакцию на цитокератины, в то время как аденокарциномы подобной реакции не дают или окрашиваются слабо (J. Corson, G. Pincus, 1982).
РЭА выявляется в аденокарциноме, при мезотелиоме реакция слабая или отрицательная. Моноклональные антитела, специфичные для мезотелиом плевры, пока не обнаружены.
Учитывая трудности дифференциальной диагностики при микроскопическом исследовании (включая гистохимические и иммуноморфологические методы), диагноз мезотелиомы должен основываться на исключении первичной опухоли в желудке, легком и т.д.
Ультраструктура. Клетки мезотелиомы эпителиального типа отличаются от структур аденокарцином. Видны хорошо выраженные длинные разветвленные микроворсинки. Цитоплазма бедна органеллами, не содержит каких-либо секреторных гранул. Волокна асбеста могут быть обнаружены в плевре, но в опухолевой ткани их обычно нет.
Источник: remedium.ru
Параканкрозная пневмония при бронхо-альвеолярной карциноме
Инв. №:
Оптимизация методов лечения хирургических осложнений при рак е лёгкого [Текст] / А. И. Арсеньев [и др.] // Вопросы онкологии : «Эскулап», 2012. — Том 58, N 5. — С. 674-678. — Библиогр.: с. 677-678
Рубрики: Легких рак —лечение
Кл.слова (ненормированные):
Рак лёгкого — Хирургическое лечение — Осложнения
Доп.точки доступа:
Арсеньев, А.И.; Нефедов, А.О.; Левченко, Е.В.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Расширенная левосторонняя плевропневмоноэктомия с резекцией и протезированием гркдной аорты и легочного ствола по поводу рак а легкого [Текст] / В. Д. Паршин, Ю. В. Белов, Р. Н. Комаров // Хирургия. Журнал имени Н.И. Пирогова. — 2013. — № 5. — с. 53-56 : рис. — Библиогр. в конце ст. . — ISSN 0023-1207
Кл.слова (ненормированные):
РАК ЛЁГКОГО — ИСКУСССТВЕННОЕ КРОВООБРАЩЕНИЕ — РЕЗЕКЦИЯ ЛЕГОЧНОГО СТВОЛА
Доп.точки доступа:
Паршин, В.Д.; Белов, Ю.В.; Комаров, Р.Н.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Полиморфизм гена XRCC1 ARG399GLN у больных рак ом лёгкого с различными клиническими ха рак теристиками опухоли [Текст] / И. А. Кузнецова, К. И. Янкович, А. И. Дмитриева // Туберкулёз и болезни лёгких. — 2013. — N 4. — с. 46-49 : табл. — Библиогр. в конце ст. . — ISSN 2075-1230
Кл.слова (ненормированные):
РАК ЛЁГКОГО — ПОЛИМОРФИЗМ — ГЕНЫ РЕПАРАЦИИ ДНК
Доп.точки доступа:
Кузнецова, И.А.; Янкович, К.И.; Дмитриева, А.И.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Морфологические, иммуногистохимические и спектральные ха рак теристики дисплазий, преинвазивных и инвазивных форм центрального рак а лёгкого [Текст] / А. И. Арсеньев, А. А. Барчук, Е. А. Желбунова // Вестник хирургии имени И.И. Грекова. — 2013. — Том 172, N 5. — С. 16-20. — Библиогр.: с.19-20 . — ISSN 0042-4625
Кл.слова (ненормированные):
рак лёгкого — бронхоскопия — биопсия
Доп.точки доступа:
Арсеньев, А.И.; Барчук, А.А.; Желбунова, Е.А.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Метастатическое поражение сердца как проявление злокачественного новообразования легкого [Текст] / В. А. Ахмедов, И. А. Сезина, А. Н. Кузовкин // Пульмонология. — 2013. — N 5. — с. 101-102 : рис. — Библиогр. в конце ст. . — ISSN 0869-0189
Кл.слова (ненормированные):
рак лёгкого — метастаз в сердце
Доп.точки доступа:
Ахмедов, В.А.; Сезина, И.А.; Кузовкин, А.Н.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Хирургическое лечение больных с злокачественными новообразованиями лёгкого и средостения с массивной инвазией в грудную аорту с использованием экст рак орпорального кровообращения [Текст] / В. В. Андрущук, В. В. Жарков, Ю. П. Островский // Вестник хирургии имени И.И. Грекова. — 2013. — Том 172, N 6. — С. 72-77 : рис. — Библиогр.: с.77 . — ISSN 0042-4625
Кл.слова (ненормированные):
Рак лёгкого — Рак вилочковой железы — Грудная аорта
Доп.точки доступа:
Андрущук, В.В.; Жарков, В.В.; Островский, Ю.П.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Влияние плотности микрососудов в опухоли на прогноз у больных с I-II стадией немелкоклеточного рак а лёгкого после проведенного хирургического лечения [Текст] / А. П. Колесник, А. П. Шевченко, В. А. Туманский // Вопросы онкологии. — 2013. — Том 59, N 6. — с. 435-739 : рис. — Библиогр. в конце ст. . — ISSN 0507-3758
Кл.слова (ненормированные):
рак лёгкого — плотность микрососудов опухоли — выживаемость
Доп.точки доступа:
Колесник, А.П.; Шевченко, А.П.; Туманский, В.А.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Лаушкина, Ж. А.
Гипердиагностика туберкулёза у больных со злокачественными новообразованиями лёгких [Текст] / Ж. А. Лаушкина, П. Н. Филимонов // Туберкулёз и болезни лёгких. — 2014. — N 5. — с. 56-59 : табл. — Библиогр. в конце ст. . — ISSN 2075-1230
Кл.слова (ненормированные):
рак лёгкого — диагностика — задержка диагноза
Доп.точки доступа:
Филимонов, П.Н.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Анализ одногодичной летальности радикально оперированных больных немелкоклеточным рак ом лёгкого старше 70 лет [Текст] / Э. Я. Друкин, В. Г. Прейс, А. Е. Михнин // Вопросы онкологии. — 2014. — Том 60, N 2. — с. 88-93 : табл. — Библиогр. в конце ст. . — ISSN 0507-3758
Кл.слова (ненормированные):
рак лёгкого — хирургическое лечение рак а лёгкого — больные старше 70 лет
Доп.точки доступа:
Друкин, Э.Я.; Прейс, В.Г.; Михнин, А.Е.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Лежнин, В. Л.
Оценка многофакторного влияния техногенного загрязнения на развитие рак а лёгких у населения [Текст] / В. Л. Лежнин, В. С. Казанцев, Е. В. Ползик // Гигиена и санитария. — 2014. — N 3. — с. 26-30 : рис. — Библиогр. в конце ст. . — ISSN 0016-9900
Кл.слова (ненормированные):
техногенное загрязнение окружающей среды — рак лёгкого — многофакторный анализ
Доп.точки доступа:
Казанцев, В.С.; Ползик, Е.В.
Нет сведений об экземплярах (Источник в БД не найден)
Инв. №:
Диагностика и хирургическое лечение рак а лёгкого в условиях специализированного то рак ального отделения для больных с гнойными заболеваниями лёгкого [Текст] / И. В. Дейнега, В. И. Егоров, П. М. Иононов // Вестник хирургии имени И.И. Грекова. — 2014. — Том 173, N 3. — С. 15-18. — Библиогр. в конце ст. . — ISSN 0042-4625
Кл.слова (ненормированные):
рак лёгкого — па рак анкрозное воспаление — абсцесс лёгкого
Доп.точки доступа:
Дейнега, И.В.; Егоров, В.И.; Иононов, П.М.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Аксарин, А. А.
Несостоятельность швов культи бронха в хирургии рак а лёгкого [Текст] / А. А. Аксарин, М. Д. Тер-Ованесов // Хирургия. Журнал имени Н.И. Пирогова. — 2014. — № 9. — с. 33-36 : табл. — Библиогр. в конце ст. . — ISSN 0023-1207
Кл.слова (ненормированные):
рак лёгкого — хирургическое лечение рак а лёгкого — Несостоятельность швов культи бронха
Доп.точки доступа:
Тер-Ованесов, М.Д.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Роль однофотонной эмисионной компьютерной томографии и рентгеновской компьютерной томографии в диагностике метастатического поражения лимфоузлов у больных немелкоклеточным рак ом лёгкого [Текст] / С. В. Канаев, С. Н. Новиков, Д. С. Бейнусов // Вопросы онкологии. — 2014. — Том 60, N 4. — с. 476-481 : табл. — Библиогр. в конце ст. . — ISSN 0507-3758
Кл.слова (ненормированные):
рак лёгкого — метастазы — компьютерная томография и рентгеновская компьютерная томография
Доп.точки доступа:
Канаев, С.В.; Новиков, С.Н.; Бейнусов, Д. С.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Макарова, О. П.
Исследование противовоспалительной активности бронхоальвеолярной лаважной жидкости при рак е лёгкого и воспалительных заболеваний органов дыхания [Текст] / О. П. Макарова, Л. Н. Шишкина, А. П. Огиренко // Туберкулёз и болезни лёгких. — 2014. — N 11. — с. 64-68 : рис. — Библиогр. в конце ст. . — ISSN 2075-1230
Кл.слова (ненормированные):
рак лёгкого — воспалительные заболевания органов дыхания — бронхоальвеолярная лаважная жидкость
Доп.точки доступа:
Шишкина, Л. Н.; Огиренко, А.П.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Оценка эффективности современных методов первичной и уточняющей диагностики рак а лёгкого [Текст] / А. И. Арсеньев, А. А. Барчук, К. А. Костицын // Вопросы онкологии. — 2014. — Том 60, N 6. — с. 695-699. — Библиогр. в конце ст. . — ISSN 0507-3758
Кл.слова (ненормированные):
рак лёгкого — низкодозная компьютерная томография — трансторокальная стереотаксическая трепанбиопсия
Доп.точки доступа:
Арсеньев, А.И.; Барчук, А. А.; Костицын, К.А.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Бурдюков, М. С.
Современные малоинвазивные способы верификации диагноза у больных с опухолями легких [Текст] / М. С. Бурдюков // Вестник рентгенологии и радиологии. — 2015. — N 3. — с. 52-57. — Библиогр. в конце ст. . — ISSN 0042-4676
Кл.слова (ненормированные):
рак лёгкого — эндосонография — тонкоигольная пункция
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Мотус, И. Я.
Бронхиальные свищи после пневмонэктомии при рак е легкого [Текст] / И. Я. Мотус, А. В. Баженов // Хирургия. Журнал имени Н.И. Пирогова. — 2015. — № 8(2). — с. 33-38 : табл. — Библиогр. в конце ст. . — ISSN 0023-1207
Кл.слова (ненормированные):
рак лёгкого — пневмонэктомия — бронхиальные сищи
Доп.точки доступа:
Баженов, А.В.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Метастазы в кожу у больного рак ом лёгкого , первоначально принятого за диссеминированный туберкулёз лёгких [Текст] / С. Н. Новикова, Е. И. Сусликова, Ю. И. Шахова // Туберкулёз и болезни лёгких. — 2015. — N 9. — с. 59-62 : рис. — Библиогр. в конце ст. . — ISSN 2075-1230
Кл.слова (ненормированные):
туберкулёз — рак лёгкого — метастазы в кожу
Доп.точки доступа:
Новикова, С.Н.; Сусликова, Е.И.; Шахова, Ю.И.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Автоматизированная идентификация, интерпретация и классификация очаговых изменений в легких на изображениях, полученных при компьютерной томографии, для проведения скрининга рак а лёгких [Текст] / А. А. Барчук, М. Д. Подольский, С. А. Та рак анов // Вопросы онкологии. — 2015. — Том 61, N 6. — с. 913-919 : табл. — Библиогр. в конце ст. . — ISSN 0507-3758
Кл.слова (ненормированные):
рак лёгкого — лёгочные узлы — иденсификация лёгочных очагов
Доп.точки доступа:
Барчук, А.А.; Подольский, М.Д.; Та рак анов, С.А.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Оценка пригодности архивных цитологических образцов рак а лёгкого для молекулярно-генетических исследований [Текст] / Н. В. Митюшкина, А. Г. Иевлева, А. Н. Полторацкий // Вопросы онкологии. — 2015. — Том 61, N 6. — с. 968-971 : рис. — Библиогр. в конце ст. . — ISSN 0507-3758
Кл.слова (ненормированные):
рак лёгкого — молекулярно-генетические исследования
Доп.точки доступа:
Митюшкина, Н.В.; Иевлева, А.Г.; Полторацкий, А.Н.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Основание использования экспрессионных маркёров для персонализации химиотерапии рак а лёгкого [Текст] / М. М. Цыганов, Е. О. Родионов, С. В. Миллер // Антибиотики и химиотерапия. — 2015. — Том 60, N 9—10. — с. 38-45 : рис. — Библиогр. в конце ст. . — ISSN 0235-2990
Кл.слова (ненормированные):
рак лёгкого — химиотерапия — монорезистентности
Доп.точки доступа:
Цыганов, М.М.; Родионов, Е.О.; Миллер, С.В.
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Рекомендации по ранней диагностике рак а лёгкого для врачей первичного звена [Текст] // Вестник рентгенологии и радиологии. — 2016. — Том 97, N 2. — С. 69-78 . — ISSN 0042-4676
Кл.слова (ненормированные):
рак лёгкого — низкодозная компьютерная томография — скрининг рак а легкого
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Инв. №:
Порханов, Владимир Алексеевич.
Диагностика солитарных очаговых образований легких и стратегия диспансерного наблюдения за пациентами [Текст] / В. А. Порханов, Л. В. Шульженко [и др.] // Казанский мед. ж. — 2016. — Т. 97, № 5. — с. 736-743 : граф. — Библиогр.: с. 742-743 . — ISSN 0368-4814
Кл.слова (ненормированные):
СОЛИТАРНЫЕ ОЧАГОВЫЕ ОБРАЗОВАНИЯ ЛЕГКИХ — ДИАГНОСТИКА — ДИСПАНСЕРИЗАЦИЯ — РАК ЛЁГКОГО — КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ
Доп.точки доступа:
Шульженко, Лариса Владимировна; Поляков, Игорь Станиславович; Болотова, Елена Валентиновна; Смолин, Алексей Алексеевич
Имеются экземпляры в отделах: всего 1 : ЧЗ (Кантемировская, 16) (1)
Свободны: ЧЗ (Кантемировская, 16) (1)
Источник: library.gpmu.org
Студенческий документ № 045450 из МГМСУ им. А. И. Евдокимова
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫС-
ШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«ИВАНОВСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КАФЕДРА ГОСПИТАЛЬНОЙ ТЕРАПИИ
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ПРИ ЗАБОЛЕВАНИЯХ ОРГАНОВ ДЫХАНИЯ
Учебное пособие для студентов, обучающихся по специальности
«лечебное дело»
Составители: Гудухин А.А., Мишина И.Е., Облогина Л.И., Семенов А.В., Михайловская Т.В., Корнилов Л.Я., Алеутская О.Н., Лебедева Е.А., Архипова С.Л.
Зав. кафедрой госпитальной терапии и профессиональных болезней ГБОУ ВПО
«Тверская государственная медицинская академия»
д.м.н., профессор Мазур Евгений Станиславович
Заведующий кафедрой факультетской терапии с военно-полевой терапией ГБОУ ВПО
«Ярославская государственная медицинская академия»
д.м.н., профессор Чижов Петр Александрович
Учебное пособие для аудиторной работы составлено в соответствии с Государственным образовательным стандартом высшего профессионального образования по специальности 060101 — лечебное дело, типовой программы, учебного плана по пульмонологии. Учебное пособие освещает значение изучаемых тем, содержит контрольные вопросы и ситуационные задачи.
Предназначено для самостоятельной подготовки студентов VI курса при изучении модуля «пульмонология» дисциплины «внутренние болезни».
СОДЕРЖАНИЕ
Список сокращений 4 Введение 6 I. Дифференциальный диагноз при синдроме легочного инфильтрата 7 II. Дифференциальный диагноз при синдроме бронхиальной обструкции 46 III. Дифференциальный диагноз при удушье 65 IV. Дифференциальная диагностика диссеминированных процессов в легких 90 V. Дифференциальная диагностика при синдроме плеврального выпота 122 Литература 141
GINA — Global Initiative for Asthma (Глобальная стратегия лечения и профилактики бронхиальной астмы)
GOLD — Global Initiative for Chronic Obstructive Lung Disease (Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких)
MRSA — метициллинрезистентный золотистый стафилококк
MSSA — метициллинчувствительный золотистый стафилококк
АД — артериальное давление
АМП — антимикробный препарат
АП — аспирационная пневмония
АСИТ — аллерген-специфическая иммунотерапия
БАЛ — бронхоальвеолярный лаваж
БОМЖ — без определенного места жительства
ВАП — вентилятороассоциированная пневмония
ВП — внебольничная пневмония
ВИЧ — вирус иммунодефицита человека
ДАД — диастолическое артериальное давление
ДАИ — дозирующий аэрозольный ингалятор
ДВС — диссеминированное внутрисосудистое свертывание
ДЗЛ — диссеминированные заболевания легких
ДЗСТ — диффузные заболевания соединительной ткани
ДН — дыхательная недостаточность
ИБС — ишемическая болезнь сердца
ИВЛ — искусственная вентиляция легких
ИГКС — ингаляционные глюкокортикостероиды
ИТШ — инфекционно-токсический шок
КТ — компьютерная томография
КУМ — кислотоустойчивые микобактерии
ЛФК — лечебная физкультура
МБТ — микобактерии туберкулеза
МКБ — Международная классификация болезней
МОС — максимальная объемная скорость выдоха
МРТ — магнито-резонансная томография
НИВ — неинвазивная интермиттирующая вентиляция легких
НП — нозокомиальная пневмония
ОРВИ — острая респираторная вирусная инфекция
ОРДС — острый респираторный дистресс-синдром
ОРИТ — отделение реанимации и интенсивной терапии
ОФВ1 — объем форсированного выдоха за первую секунду
ПСВ — пиковая скорость выдоха
САД — систолическое артериальное давление
СВЧ — сверхвысокие частоты
СОС — средняя объемная скорость выдоха
СОЭ — скорость оседания эритроцитов
ТЭЛА — тромбоэмболия легочной артерии
УВЧ — ультравысокие частоты
УФ — ультрафиолет
ФЖЕЛ — форсированная жизненная емкость легких
ХОБЛ — хроническая обструктивная болезнь легких
ХПН — хроническая почечная недостаточность
ХСН — хроническая сердечная недостаточность
ЦВД — центральное венозное давление
ЧД — частота дыхания
ЧСС — частота сердечных сокращений
ЭОС — электрическая ось сердца
ЭТА — экзогенный токсический альвеолит ЭхоКГ — эхокардиограмма
ВВЕДЕНИЕ
Многообразие заболеваний органов дыхания, имеющих сходную клиническую или рентгенологическую симптоматику, требует выработки навыка дифференциальной диагностки. Актуальность данного вопроса обусловлена также ростом количества заболеваний органов дыхания с маловыраженным, «атипичным» клиническим течением, трудных для диагностики и требующих применения алгоритмов, отталкивающихся от основного синдрома, выявленного при первичном обследовании больного.
В результате изучения данного учебного пособия студент должен знать:
* основные синдромы поражения системы органов дыхания;
* заболевания, которые могут протекать с этими синдромоми;
* клинические и рентгенологические особенности, а также методы верификации данных заболеваний;
уметь:
* выявить у пациента основной легочный синдром;
* на основании клинических данных заподозрить одно или несколько сходных по проявлениям заболеваний (установить предварительный диагноз);
* составить план дополнительных методов исследований;
* интерпретировать результаты лабораторных и инструментальных методов исследований;
* установить клинический диагноз;
* определить тактику ведения больного; ? назначить лечение.
I. ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ ПРИ СИНДРОМЕ
Легочный инфильтрат — это клинико-рентгенологический синдром, в основе которого лежит проникновение и накопление в ткани легкого клеточных элементов и биологических жидкостей, что ведет к увеличению объема и уплотнению легочной ткани. Накопление только биологических жидкостей (без клеточных элементов) характеризует отек легкого, а не инфильтрацию. Основные группы инфильтратов по морфологии:
* инфекционно-воспалительные (пневмония, туберкулез),
* инфильтраты при опухолях (раковые, лейкозные и т.д.), ? геморрагические (инфаркт легкого).
по размеру и форме:
* лобиты, сегментиты, полисегментиты (затемнения легочной ткани соответствующей формы в пределах доли, одного или нескольких сегментов);
* округлые инфильтраты (однородное затемнение с более или менее четкими контурами на фоне малоизмененной легочной ткани, диаметром от 1 до 5 см);
* очаговые тени (инфильтрат диаметром до 1 см).
Перечень основных заболеваний, при которых возникает синдром легочной инфильтрации:
2. Туберкулез легких (инфильтративный, очаговый, туберкулема)
3. Рак легкого (центральный, периферический) 4. Внебронхиальные доброкачественные опухоли:
4.1. Аденома
4.5. Ксантома
4.7. Гемангиома и др.
5. Инфаркт легкого
6. Эозинофильный инфильтрат
7. Паразитарные заболевания легких (аскаридоз, эхинококкоз)
8. Поражение легких от воздействия физических факторов (бензиновый пневмонит, синдром Мендельсона, радиационные поражения легких)
9. Ателектаз доли легкого, сегмента
10. Заполненные кисты бронхиальные (ретенционные) Клинические проявления синдрома легочного инфильтрата.
Жалобы больных неспецифичны:
* боли в грудной клетке при кашле и глубоком дыхании (если инфильтрат расположен субплеврально).
Физикальные данные:
* отставание пораженной половины грудной клетки в акте дыхания,
* локальное усиление голосового дрожания,
* локальное укорочение, притупление перкуторного звука,
* участок бронхиального дыхания и/или влажных мелкопузырчатых хрипов и/или крепитации.
Клинические проявления синдрома легочной инфильтрации зависят, прежде всего, от размера инфильтрата, а также от его характера и локализации. Описанные выше типичные клинические проявления наблюдаются, в основном, при крупных экссудативных легочных инфильтратах (например, при неспецифической пневмонии). При легочном инфильтрате преимущественно продуктивного характера, например, при опухолях, гранулематозных процессах, а также при воспалительных инфильтратах с нарушением бронхиального дренажа, усиление голосового дрожания, крепитация и хрипы не определяются, выслушивается лишь ослабленное дыхание. В таких случаях на основании клинических данных определить легочный инфильтрат не представляется возможным.
Верификация синдрома осуществляется рентгенологически. Рентгенограмма органов грудной полости должна выполняться как минимум в двух проекциях. Верифицирующим симптомом является затемнение, которое описывается по следующим критериям:
• локализация,
• интенсивность, ? гомогенность, ? контур.
Алгоритм дифференциальной диагностики при легочном инфильтрате
1. Долевые, полисегментарные и сегментарные инфильтраты
1.1 Пневмония — острое локальное инфекционно-воспалительное заболевание легких с вовлечением в патологический процесс респираторных отделов (альвеол, бронхиол), протекающее с инфильтрацией клетками воспаления и внутриальвеолярной экссудацией.
Классификация По этиологии:
* бактериальные (с указанием конкретного возбудителя),
* паразитарные,
* без уточнения возбудителя. Эпидемиологическая:
* аспирационная,
* на фоне иммунодефицита.
По степени тяжести: ? нетяжелые, ? тяжелые.
По локализации: с указанием сегмента или нескольких сегментов.
По характеру течения:
* острое (длительность заболевания менее 1 месяца)
* затяжное (длительность заболевания более 1 месяца). Осложнения:
* парапневмонический плеврит,
* абсцесс и гангрена легких,
* бронхиальная обструкция,
* острая дыхательная недостаточность (дистресс-синдром).
* острое легочное сердце,
* эндокардит,
* менингит, ? энцефалит, ? острый психоз.
Пример формулировки диагноза:
1. Внебольничная пневмония с локализацией в S8-9 правого легкого, нетяжелое течение. ДН I.
2. Внебольничная нижнедолевая левосторонняя пневмония, тяжелое течение, осложненная экссудативным плевритом. ДН II.
Внебольничная пневмония (ВП) — острое заболевание, возникшее во внебольничных условиях (вне стационара), или диагностированное в первые 48 ч от момента госпитализации.
Этиология
Этиология ВП непосредственно связана с нормальной микрофлорой, колонизующей верхние отделы дыхательных путей. Наиболее частые возбудители:
* Streptococcus pneumonie (30-50% случаев заболевания), ? Haemophilus influenzae (до 10%).
Существенную роль в этиологии ВП имеют атипичные микроорганизмы, которые не удается идентифицировать при бактериоскопии или посеве на обычные питательные среды (8-30% случаев заболевания):
* Chlamydophila pneumoniae, Mycoplasma pneumonia (суммарно до 25%), ? Legionella pneumophila.
К редким возбудителям (в 3-5% случаев ВП) относятся:
* Staphylococcus aureus, ? Klebsiella pneumoniae, ? энтеробактерии.
В очень редких случаях ВП может вызывать Pseudomonas aeruginosa (у больных муковисцидозом, при наличии бронхоэктазов).
На практике, ввиду отсутствия результатов микробиологического исследования мокроты в первые дни болезни, вероятный возбудитель, определяющий первичный выбор антибиотика, устанавливается ориентировочно в зависимости от группы пациентов, разделенных с учетом возраста, тяжести заболевания и сопутствующей патологии.
Нозокомиальная (госпитальная, внутрибольничная) пневмония (НП) — заболевание, которое развивается спустя 48 ч и более после госпитализации, при исключении инфекций, которые имелись в инкубационном периоде на момент поступления больного в стационар.
Факторы риска:
* длительность пребывания в стационаре,
* предшествующая антибактериальная терапия, ? наличие фоновых хронических заболеваний, ? специфика лечебного учреждения.
Выделяют раннюю госпитальную пневмонию, возникающую в период от 2 до 5 дня госпитализации, для которой характерны возбудители, в большинстве своем чувствительные к традиционно используемым антимикробным препаратам (S. Pneumoniae, Enterobacteriaceae, H. Influenzae) и имеющую благоприятный прогноз.
Поздняя госпитальная пневмония развивается после 5 дня госпитализации, характеризуется высоким риском наличия полирезистентных возбудителей (P. aeruginosa, Escherichia coli, Klebsiella pneumoniae и Acinetobacter spp.) и менее благоприятным прогнозом.
Выделяют также вентилятороассоциированные пневмонии (ВАП) — пневмонии у лиц, находящихся на искусственной вентиляции легких.
Аспирационные пневмонии (АП) могут быть как вне- так и внутрибольничными. АП осложняют развившуюся у больного аспирацию пищи, рвотных масс, крови, токсических и других агентов в нижние дыхательные пути, сопровождающуюся проникновением вместе с аспиратом патогенной флоры. Аспирация обычно развивается у лиц с расстройствами сознания различной глубины вследствие:
* тяжелого алкогольного опьянения,
* комы различной этиологии,
* отравления снотворными препаратами, ? судорожных состояний.
Аспирация может возникнуть при кардиоспазме, наличии трахеоэзофагеальных свищей.
Вызывают развитие АП анаэробы:
* Peptosstreptococcus и др., а также некоторые аэробы:
* Escherichia coli,
Пневмонии у лиц с иммунодефицитом.
Основными причинами иммунодефицита являются:
* длительное (> 3 недель) использование цитостатиков или системных глюкокортикоидов для лечения опухолей, системных заболеваний, у пациентов после трансплантации органов.
В общем анализе крови иммунодефицит проявляется длительной нейтропенией ( 125 / мин.
* Нарушения сознания.
* Лейкоцитоз > 20,0 Г/л или лейкопения 176,7 мкмоль/л
* SaO2 50 мм рт.ст. при дыхании комнатным воздухом
* Пневмоническая инфильтрация локализуется более чем в одной доле
* Наличие осложнений: полость (полости) распада, плевральный выпот, ИТШ.
* При наличии хотя бы одного критерия внебольничная пневмония расценивается как тяжелая
Диагностический стандарт обследования больного пневмонией
Клинические критерии:
* Острая фебрильная лихорадка, интоксикация,
* Кашель сухой или с мокротой,
* Боль в грудной клетке, связанная с дыханием,
* Усиление голосового дрожания,
* Локальное притупление перкуторного звука,
* Локально выслушиваемое бронхиальное дыхание, участок звучных мелкопузырчатых хрипов и/или крепитации, шум трения плевры.
* лейкоцитоз > 10 Г/л с палочкоядерным сдвигом > 10%, увеличение СОЭ;
* инфильтративное затемнение на обзорной рентгенограмме органов грудной полости;
* выявление микроорганизмов в мокроте при бактериоскопии с окраской мазка по Граму, а также верификация микроорганизма и определение его чувствительности к антибиотикам при бактериологическом исследовании;
* сатурация крови кислородом 38°С), длительностью более 96 часов, непродуктивный кашель, боль в грудной клетке, кровохарканье, дыхательная недостаточность. Грибковые пневмонии развиваются очень быстро и сопровождаются высокой летальностью. Обязательными диагностическими методами наряду с рентгенограммой, являются: КТ в режиме высокого разрешения, микроскопическое исследование респираторных субстратов (мокрота, жидкость БАЛ и пр.) с обязательным посевом на питательные среды. Следует учитывать, что обнаружение грибов в нестерильных в норме биосубстратах (в т.ч. в мокроте) обусловлено колонизацией, которая не требует специфического лечения.
Причины и характер атипичного течения пневмонии.
Наличие тяжелых соматических заболеваний, выраженный иммунодефицит, пожилой возраст и другие факторы могут модифицировать течение пневмоний.
У этой категории больных возможны:
* отсутствие или малая выраженность физикальных признаков легочного воспаления;
* отсутствие лихорадки;
* преобладание внелегочных симптомов (нарушения со стороны центральной нервной системы и др.);
* отсутствие типичных изменений со стороны периферической крови;
* отсутствие типичных рентгенологических изменений, что может быть обусловлено не только вариантом пневмонии, но также локализацией, сроками исследования.
Показания для госпитализации:
1. Тяжелая пневмония.
2. Неэффективность стартовой антибактериальной терапии в амбулаторных условиях в течение 48-72 часов.
3. Социальные показания (невозможность организовать адекватное лечение пневмонии на дому).
Относительные показания для госпитализации:
* возраст старше 60 лет,
* тяжелые сопутствующие заболевания (ХОБЛ, злокачественные новообразования, сахарный диабет, ХПН, ХСН, алкоголизм, наркомания, истощение),
* предпочтения пациента и/или членов его семьи.
Чтобы быстро сориентироваться в тактике ведения конкретного пациента можно использовать английскую шкалу CRB-65, позволяющую прогнозировать летальность и, следовательно, определять показания к госпитализации либо в общетерапевтические отделения, либо в ОРИТ (рис.1).
Рис.1 Шкала прогноза летальности при пневмонии
Режим: на период лихорадки и интоксикации — постельный или полупостельный, с последующим расширением (стационарный, амбулаторный).
Диета: полноценная, обогащенная витаминами, включающая легко усваиваемые продукты, с увеличением объема употребляемой жидкости (1 литр на каждый градус повышения температуры).
Принципы медикаментозной терапии пневмоний
* Раннее начало антибактериальной терапии в соответствии с вероятным возбудителем.
* Улучшение бронхиального дренажа.
* Коррекция микроциркуляторных нарушений.
Установление диагноза пневмонии является абсолютным показанием для назначения антибактериальной терапии. Первая доза антибиотика должна быть дана в первые 4 часа с момента постановки диагноза!
Различают эмпирическую терапию пневмоний (при неизвестной этиологии) и терапию пневмоний установленной этиологии.
Антибактериальная терапия пневмоний известной этиологии
S. pneumonie. Средствами выбора для лечения пневмоний являются аминопенициллины (амоксициллин — внутрь, ампициллин — парентерально), в т.ч. ингибиторзащищенные (амоксициллин/клавуланат) и цефалоспорины III поколения (цефотаксим, цефтриаксон). Макролидные антибиотики являются альтернативой при аллергии на ?-лактамы. Высокой активностью обладают респираторные фторхинолоны (левофлоксацин, моксифлоксацин), ванкомицин и линезолид.
H. influenzae. Средствами выбора являются аминопенициллины (амоксициллин — внутрь, ампициллин — парентерально), в т.ч. ингибиторзащищенные (амоксициллин/клавуланат), цефалоспорины III поколения (цефотаксим, цефтриаксон) фторхинолоны (ципрофлоксацин, офлоксацин, левофлоксацин, моксифлоксацин).
M. pneumonie, C. pneumonie. Наибольшей активностью в отношении «атипичных» возбудителей обладают макролиды, тетрациклины (доксициклин), респираторные фторхинолоны.
S. aureus. Препаратом выбора при пневмониях, вызванных MSSA, является оксациллин, альтернативой могут быть защищенные аминопенициллины, цефалоспорины I-II поколения, линкозамиды. В случае выявления MRSA рекомендуются гликопептидными антибиотиками (ванкомицин) или линезолид, причем последнему следует отдавать предпочтение вследствие фармакокинетических особенностей.
Legionella spp. При лечении легионелезной пневмонии назначаются макролиды. Также высоко эффективны фторхинолоны (ципрофлоксацин, офлоксацин, левофлоксацин, моксифлоксацин).
Enterobacteriaceae. Максимально широким спектром действия обладают цефалоспорины III поколения. Лечение госпитальных пневмоний требует предварительного определения чувствительности к антибиотикам.
P. aeruginosa. В качестве одной из самых распространенных схем терапии псевдомонадных пневмоний рассматривается комбинация цефтазидима и тобрамицина. Высокая частота приобретенной резистентности данного возбудителя к антибиотикам требует предварительной оценки чувствительности в каждом конкретном случае.
Планирование эмпирической терапии основывается на вероятной этиологии заболевания (таблица 1).
Таблица 1.
Эмпирическая антибактериальная терапия внебольничной пневмонии у амбулаторных пациентов
Группа Наиболее частые возбудители Препараты выбора Нетяжелая ВП у пациентов без сопутствующих заболеваний, не принимавших за последние 3 мес АМП ?2 дней S. pneumoniae
M. pneumoniae C. pneumoniae
H. influenzae Амоксициллин внутрь или макролид внутрь1 Нетяжелая ВП у пациентов с сопутствующими заболеваниями и/или принимавшими за последние 3 мес АМП
?2 дней S. pneumoniae
H. influenzae C. pneumoniae
S. aureus Enterobacteriaceae Амоксициллин/клавуланат, амоксициллин/сульбактам внутрь ± макролид внутрь или
Респираторный фторхинолон (левофлоксацин, моксифлоксацин, гемифлоксацин) внутрь Примечание:1 Макролиды являются препаратами выбора при подозрении на «атипичную» этиологию ВП (C. pneumoniae, M. pneumoniae). Следует отдавать предпочтение наиболее изученным при ВП макролидам с улучшенными фармакокинетическими свойствами (азитромицин, кларитромицин) или благоприятным профилем безопасности и минимальной частотой лекарственных взаимодействий (джозамицин, спирамицин).
Таблица 2.
Эмпирическая антибактериальная терапия внебольничной пневмонии у госпитализированных пациентов
Группа Наиболее частые возбудители Рекомендованные режимы терапии Пневмония нетяжелого течения1 S. pneumoniae
H. influenzae C. pneumoniae
S. aureus
Enterobacteriaceae Бензилпенициллин в/в, в,м ± макролид внутрь2
Ампициллин в/в, в/м ± макролид внутрь2
макролид внутрь2
Амоксициллин/сульбактам в/в, в/м ± макролид2
Цефотаксим в/в, в/м ± макролид внутрь2
Цефтриаксон в/в, в/м ± макролид внутрь2
Эртапенем в/в, в/м ± макролид внутрь2 или
Респираторный фторхинолон (левофлоксацин, моксифлоксацин) в/в Пневмония тяжелого течения3 S. pneumoniae Legionella spp.
S. aureus Enterobacteriaceae Амоксициллин/клавуланат в/в + макролид в/в
Цефотаксим в/в+ макролид в/в
Цефтриаксон в/в+ макролид в/в Эртапенем в/в + макролид в/в или
Респираторный фторхинолон (левофлоксацин, моксифлоксацин) в/в
+ цефотаксим, цефтриаксон в/в Примечание:
1 Предпочтительна ступенчатая терапия. При стабильном состоянии пациента допускается сразу назначение препаратов внутрь.
2 Следует отдавать предпочтение наиболее изученным при ВП макролидам с улучшенными фармакокинетическими свойствами (азитромицин, кларитромицин) и/или благоприятным профилем безопасности и минимальной частотой лекарственных взаимодействий (джозамицин, спирамицин).
3 При наличии факторов риска P. aeruginosa — инфекции (бронхоэктазы, прием системных глюкокортикоидов, терапия антибиотиками широкого спектра действия более 7 дней в течение последнего месяца, истощение) препаратами выбора являются цефтазидим, цефепим, цефоперазон/сульбактам, тикарциллин/клавуланат, пиперациллин/тазо-бактам, карбапенемы (меропенем, имипенем), ципрофлоксацин. Все вышеуказанные препараты можно применять в монотерапии или комбинации с аминогликозидами II-III поколения. При подозрении на аспирацию целесообразно использовать амоксициллин/клавуланат, цефоперазон/сульбактам, тикарциллин/кла-вуланат, пиперациллин/тазо-бактам, карбапенемы (меропенем, имипенем).
Первоначальная оценка эффективности терапии пневмонии должна производиться в первые 48-72 часа. Основными критериями эффективности являются:
* нормализация температуры тела или ее снижение 65 лет, терапия ?-лактамами в течение предшествующих 3 месяцев, иммунодефицитные заболевания/состояния).
Алгоритм действий при медленно разрешающейся пневмонии
Если клинического улучшения не отмечается, и у пациента отсутствуют факторы риска медленного разрешения ВП, то показано проведение дифференциальной диагностики с такими заболеваниями, как:
* локальная бронхиальная обструкция (опухоль);
* ТЭЛА; * застойная сердечная недостаточность; ? медикаментозная лихорадка и др.
* солевые растворы (физиологический, Рингера и т.д.) 1000-3000 мл, ? глюкоза 5% — 400-800 мл/сут, ? гемодез 400 мл/сут.
Растворы вводятся под контролем ЦВД и диуреза.
Кислородотерапия — через маску, катетеры, ИВЛ в зависимости от степени дыхательной недостаточности.
НПВС (аспирин, ибупрофен, диклофенак и др.) внутрь или парентерально.
Улучшение бронхиального дренажа
* атровент, беродуал через небулайзер 4 раза в сутки,
* мукорегуляторы (амброксол, ацетилцистеин внутрь или ингаляционно)
Коррекция микроциркуляторных нарушений ? гепарин 15000 ед/сут, ? реополиглюкин 400 мл/сут.
Иммунозаместительная терапия
* габриглобин (Gabreglobine) 1 доза — 2,5 г, курс лечения 2,5-10 г 1 раз/сут в течение 3-10 дней.
В общий комплекс лечебных мероприятий обязательно включают лечебную гимнастику. Дыхательные упражнения не только улучшают вентиляцию легких и кровообращение, но и являются средством профилактики осложнений (гипостаз, ателектаз, плевральные спайки и др.). При неосложненном течении пневмонии программа восстановительного лечения может начинаться и заканчиваться в условиях стационара. При тяжелом течении заболевания пациенты после стационарного лечения могут быть направлены в специализированные санатории и реабилитационные отделения. Применение комплексного восстановительного лечения приводит в подавляющем большинстве случаев к выздоровлению больного и восстановлению трудоспособности.
Физиотерапия при пневмонии направлена на устранение воспаления, достижение более быстрого рассасывания воспалительного очага, улучшение функции внешнего дыхания, лимфо- и кровообращения бронхолегочной системы, восстановление нарушенного иммунного статуса, оказание гипосенсибилизирующего действия.
Противопоказания: выраженная интоксикация, температура тела выше 38°, сердечная недостаточность II-III стадии, легочное кровотечение и кровохарканье, тромбоэмболии, инфаркт-пневмония, пневмоторакс, подозрение на новообразование.
В первые дни заболевания назначают воздействие электрическим полем УВЧ на грудную клетку в непрерывном (мощностью 40-100 Вт) или импульсном (4,5-6 Вт) режимах. Электрическое поле УВЧ обладает противовоспалительным, улучшающим кровообращение, болеутоляющим, улучшающим функцию нервной системы, десенсибилизирующим действием. УВЧ не следует назначать при деструктивной пневмонии. Рекомендуются также ингаляции фитонцидов, бронхолитиков, щелочных растворов, отваров трав с отхаркивающим действием, эритемное ультрафиолетовое облучение грудной клетки (обычно отдельными полями) соответственно пораженной доле легкого, по одному полю ежедневно. Хороший эффект на стадии инфильтрации дает применение гальванизации грудной клетки на фоне антибиотикотерапии в течение 2040 мин, которую проводят при капельном внутривенном введении после того, как израсходовано 1/2-2/3 объема раствора, а при внутримышечном — через 11,5 ч после инъекции. Это повышает концентрацию препарата в воспалительном очаге.
В периоде разрешения воспалительного очага назначают СВЧ-терапию на область очага поражения или нижних долей легких. В отличие от УВЧ электрическое поле СВЧ действует не на весь организм, а локально, на воспалительный участок. По такому же принципу проводят индуктотермию (лечение переменным магнитным полем высокой частоты), применяя слаботепловые и тепловые дозы. Индуктотермия оказывает седативное, спазмолитическое, болеутоляющее действие, понижается тонус мышц тканей, расширяются кровеносные сосуды, раскрываются недействующие капилляры, увеличивается кровоток, повышаются активность и интенсивность фагоцитоза и неспецифического иммунитета, улучшаются показатели функции симпатоадреналовой системы.
В этот же период болезни проводят магнитотерапию с помощью низкочастотного (50 Гц) магнитного поля в непрерывном или прерывистом режимах, что благоприятно влияет на функции сердечно-сосудистой системы, обусловливая преимущество этого метода при лечении больных с сопутствующей сердечно-сосудистой патологией. Противопоказаниями для магнитотерапии является общее тяжелое состояние больного, температура тела свыше 38оС, выраженная гипотензия, гипертоническая болезнь III стадии, кровотечения или склонность к ним, системные заболевания крови, кахексия, рецидивирующий тромбофлебит, дефекты кожи в области воздействия
Для улучшения рассасывания воспалительного очага и устранения бронхоспазма, болей, затрудненного отхождения мокроты используют электрофорез кальция, магния, гепарина, эуфиллина, экстракта алоэ, аскорбиновой кислоты, лизоцима.
В периоде разрешения воспалительного очага используют ингаляции с отхаркивающими, муколитическими, общеукрепляющими препаратами, а также теплолечение — аппликации озокерита, парафина, иловых и торфяных грязей.
На 2-3-й неделе можно назначить климатотерапевтические процедуры (дневное пребывание на веранде, воздушные ванны).
Все методы сочетают с занятиями ЛФК, массажем. Лечебная физкультура показана на 2-3-й день с момента нормализации температуры тела. Используют упражнения, способствующие увеличению дыхательной подвижности грудной стенки, растяжению плевральных спаек, укрепляющие дыхательные мышцы и мускулатуру брюшного пресса.
При лечении затянувшихся пневмоний большее значение приобретают методы закаливания (водные обтирания, обливания, души), климатотерапия (в условиях санатория или отделения реабилитации), общее УФоблучение, аэрозольтерапия отхаркивающими, муколитическими и общеукрепляющими препаратами.
Диспансеризация.
Диспансерное наблюдение осуществляется в течение 6 месяцев с визитами к участковому терапевту через 1, 3 и 6 месяцев после выписки. Общий анализ крови, мокроты, флюорограмма, спирограмма выполняются дважды, через 1 и 6 месяцев, биохимический анализ крови — 1 раз через 6 месяцев. При необходимости проводятся консультации ЛОР-врача, стоматолога и пульмонолога. Оздоровительные мероприятия: витаминотерапия, ЛФК, сауна, санация очагов инфекции, профилактика ОРВИ и гриппа, отказ от курения, направление в профильные санатории.
1.2 Инфильтративный туберкулез органов дыхания характеризуется развитием в легких воспалительных изменений, преимущественно экссудативного характера с казеозным некрозом и наличием или отсутствием деструкции легочной ткани. Данная клиническая форма является наиболее частым проявлением вторичного туберкулеза и регистрируется у 65-75% впервые выявленных больных туберкулезом органов дыхания. Различают следующие клиникорентгенологические варианты туберкулезного инфильтрата:
* бронхолобулярный (захватывает 2-3 легочных дольки);
* округлый;
* облаковидный (сегментарный, полисегментарный);
* перисциссурит (облаковидный инфильтрат по ходу главной или добавочной междолевой борозды);
* лобит. В связи с преобладанием экссудативной тканевой реакции дифференциальной диагностики с пневмонией обычно требуют 3 из перечисленных клинико-рентгенологических вариантов инфильтративного туберкулеза: облаковидный инфильтрат, перисциссурит и туберкулезный лобит.
В анамнезе могут быть выявлены провоцирующие факторы: контакт с больным туберкулезом (экзогенная суперинфекция), сахарный диабет, ВИЧинфекция, психоэмоциональные травмы, гиперинсоляция, естественная гормональная перестройка, лечение гормональными препаратами и другие состояния и заболевания, снижающие приобретенный в первичном периоде иммунитет. Определенное дифференциально-диагностическое значение может иметь безуспешность терапии антибиотиками широкого спектра действия. Клиническая картина в этих случаях во многом сходна с таковой при пневмонии: острое начало, фебрильная лихорадка, интоксикация, продуктивный кашель, боли в груди при дыхании. Иногда первой манифестацией облаковидного инфильтрата может быть кровохарканье или легочное кровотечение. Наиболее выражены интоксикационный и респираторный синдромы при лобитах. Пальпаторно может определяться болезненность и ригидность мышц плечевого пояса на стороне поражения (симптом Воробьева-Поттенджера). При перкуссии легких можно выявить укорочение перкуторного звука в зонах «тревоги» (над- и подключичные пространства, надлопаточная, межлопаточная и подмышечная области). Дыхание над зоной поражения ослабленное бронхиальное, на высоте вдоха после покашливания можно выслушать мелкопузырчатые влажные хрипы, над полостью распада дыхание бронхиальное и определяются средне- и крупнопузырчатые влажные хрипы. В общем анализе крови лейкоцитоз (до 1618 Г/л), со сдвигом лейкоцитарной формулы влево, лимфопения, моноцитоз, увеличение СОЭ до 20-23 мм/ч. В биохимическом анализе крови снижается содержание альбуминов и повышается содержание ?- и ?-глобулинов. При выраженной интоксикации в моче появляются белок, гиалиновые цилиндры (токсическая почка).
Рентгенодиагностика.
Облаковидный инфильтрат — затемнение неправильной формы с нечеткими, постепенно исчезающими в здоровой легочной ткани контурами. Располагается обычно в за ключицей, занимает 1-2 сегмента, склонен к распаду, тогда в наиболее плотных участках, соответствующих казеозу, обнаруживаются просветления. При появлении в полости грануляционного слоя ее контур отграничивается более плотной кольцевидной тенью (формирующаяся каверна).
Перисциссурит — затемнение, чаще располагающееся в верхней доле и прилегающее к малой междолевой борозде. На прямой рентгенограмме видна тень треугольной формы, вершиной обращенная к корню легкого (треугольник Сержана). Нижняя граница тени четкая, верхняя — размытая, постепенно переходящая в здоровую легочную ткань. Перисциссурит реже, чем облаковидный инфильтрат, подвергается распаду.
Лобит — обширное затемнение всей или большей части доли, малой или средней интенсивности, негомогенное, с четкой границей по междолевой борозде. При деструкции появляются просветления различных размеров.
Для всех трех вариантов в окружающей инфильтрат легочной ткани характерно наличие очаговых теней, как плотных, так и мягких за счет лимфогенного и бронхогенного обсеменения.
Реакция Манту чаще гиперэргическая. Для верификации диагноза необходимо исследование мокроты на МБТ. При облаковидном инфильтрате, лобите в связи с выраженной тенденцией к деструкции бактериовыделение обычно массивное. Микобактерии туберкулеза можно обнаружить у многих больных уже методом прямой бактериоскопии после окраски мазка мокроты по ЦилюНельсену (необходимо исследовать не менее 3-х образцов мокроты). При необходимости используются люминесцентная микроскопия и/или посев на питательные среды. Кроме того, могут выявляться свежие эластические волокна, указывающие на формирование полости распада, или обызвествленные эластические волокна, кристаллы холестерина и соли кальция, характерные для обострения процесса в зоне старых туберкулезных очагов.
При отсутствии бактериовыделения в диагностически сложных случаях необходимо использовать фибробронхоскопию с браш- и пункционной биопсией, чрезбронхиальной биопсией патологического образования, современные иммунологические методы (Диаскинтест и др.), а также молекулярнобиологические методы обнаружения МБТ (ПЦР).
1.3 Казеозная пневмония — остропрогрессирующая форма легочного туберкулеза, характеризующаяся острым началом, выраженным интоксикационным синдромом, обширными поражениями и тяжелым прогрессирующим течением. Различают лобарную казеозную пневмонию, которая развивается как самостоятельная клиническая форма туберкулеза у ранее здорового человека, и лобулярную казеозную пневмонию как осложнение других форм туберкулеза органов дыхания (подострого диссеминированного, инфильтративного, фибрознокавернозного). Патоморфологически для казеозной пневмонии характерно резкое преобладание казеозно-некротических изменений над другими специфическими изменениями в легочной ткани и формирование секвестрирующих полостей распада (единичных гигантских или множественных). В 100% случаев поражаются терминальные бронхиолы, появляются очаги бронхогенной диссеминации.
Развивается казеозная пневмония чаще у мужчин молодого и среднего возраста, одиноких, злоупотребляющих алкоголем, живущих в плохих материально-бытовых условиях (лица БОМЖ, мигранты). Факторами риска являются также ВИЧ-инфекция, белковое голодание, стрессы, длительное лечение глюкокортикостероидами, цитостатиками, контакт с бактериовыделителем.
Также как и при неспецифической пневмонии, клиническая картина лобарной казеозной пневмонии яркая. Начало острое, фебрильная лихорадка, озноб, слабость вплоть до адинамии, анорексия, быстрая потеря массы тела (до 10-20 кг и более), поты. Выражены и респираторные симптомы: одышка, боли в груди при дыхании, кашель, который первые 2-3 недели может быть сухим, но при расплавлении казеоза и его отторжении кашель становится продуктивным с отхождением большого количества мокроты, приобретающей гнойный характер. Могут быть кровохарканье и легочные кровотечения.
Больные, как правило, поступают в терапевтические, пульмонологические стационары в тяжелом состоянии с диагнозом пневмонии. При объективном обследовании отмечается истощение пациента, бледность кожных покровов, цианоз слизистой губ, кончика носа, тахипноэ с участием вспомогательной мускулатуры. Пораженная половина грудной клетки отстает при дыхании, может быть несколько уменьшена в объеме вследствие гиповентиляции, сопутствующей казеозу. При перкуссии определяется притупление легочного звука над пораженным участком, при аускультации — ослабленное бронхиальное дыхание, хрипы первые 2-3 недели могут не выслушиваться, но с развитием распада легочной ткани и формированием полостей дыхание становится бронхиальным и выслушиваются многочисленные звонкие средне- и крупнопузырчатые влажные хрипы. У пациентов могут определяться тахикардия, акцент II тона над легочной артерией.
Подозрение на казеозную пневмонию должно возникать при быстром ухудшении состояния пациента, значительном снижении у него массы тела, отсутствии эффекта от антибиотикотерапии, наличии эпидемических, социальных, медико-биологических факторов риска по туберкулезу в анамнезе.
При проведении дополнительного обследования в клиническом анализе крови, как правило, отмечаются анемия, лейкоцитоз/лейкопения, нейтрофилез, абсолютная и относительная лимфопения, высокие цифры СОЭ (40-60 мм и выше), токсигенная зернистость нейтрофилов. Значительные изменения и в биохимических показателях: гипопротеинемия, диспротеинемия с уменьшением содержания альбуминов. В общем анализе мочи протеин-, лейкоцит- и эритроцитурия, гиалиновые цилиндры. Кожные туберкулиновые пробы отрицательные (вторичная отрицательная анергия).
При исследовании мокроты на возбудитель туберкулеза первые 2-3 недели МБТ в материале могут не обнаруживаться методом прямой микроскопии с окраской по Цилю-Нельсену, но с образованием полостей в легких у больных отмечается обильное бактериовыделение, определяемое бактериоскопически и бактериологически.
При рентгенологическом исследовании лобарная казеозная пневмония характеризуется затемнением всей или большей части доли легкого. Тень интенсивная, вначале гомогенная без четкой демаркации по междолевой борозде. При прогрессировании процесса на фоне затемнения появляются участки просветления неправильной формы с нечеткими контурами. На стороне поражения и в противоположном легком визуализируются множественные, крупные, неправильной формы очаги бронхогенного обсеменения.
Течение казеозной пневмонии осложняется развитием спонтанного пневмоторакса, легочного кровотечения, дыхательной недостаточности смешанного типа, чаще с преобладанием рестриктивного компонента.
Прогноз при казеозной пневмонии часто неблагоприятный. Летальность составляет 50-60%. Больные погибают от легочно-сердечной недостаточности, инфекционно-токсического шока, профузного легочного кровотечения.
1.4 Центральный рак легкого характеризуется поражением главного, долевого, промежуточного и сегментарных бронхов. В зависимости от характера роста выделяют три анатомические формы:
1. Эндобронхиальный рак. Опухоль растет в просвет бронха, вызывает сужение его просвета и нарушение вентиляции.
2. Перибронхиальный рак. Рост опухоли происходит кнаружи от стенки бронха. Нарушение вентиляции возникает за счет сдавливания бронхиальной стенки извне, или отсутствует.
3. Смешанная форма. Опухоль развивается как со стороны слизистой бронха, так и кнаружи от его стенки.
Первичные (локальные) симптомы наблюдаются у больных центральным раком легкого. К первой группе симптомов относятся кашель, боль в грудной клетке, кровохаркание, одышка и повышение температуры тела. В начале заболевания кашель сухой, интенсивный, позднее сопровождается выделением слизистой или слизисто-гнойной мокроты. Кровохаркание встречается в 30-50% случаев в виде прожилок крови или густого окрашивания мокроты кровью. Иногда мокрота имеет цвет малинового желе. Причинами кровохаркания могут быть: распад опухоли, изъязвление слизистой бронхов и деструктивные изменения в ателектазе. Аррозия бронхиальных сосудов или ветвей легочной артерии может привести к массивному кровотечению. Боль в грудной клетке — частый симптом рака легкого, возникающий вследствие ателектаза, смещения средостения и раздражения париетальной плевры. Характер и интенсивность болевых ощущений бывает различной: покалывание в грудной клетке, остро возникающая боль, иррадиирующая в область сердца, плечо, лопатку, мышцы живота. Одышка развивается у 30-60% больных раком легкого в связи с ателектазом и смещением средостения, нарушением кровообращения, плевритом. Примерно у 30% больных центральным раком начало болезни острое или подострое вследствие развития обструктивного пневмонита: повышение температуры тела до высоких цифр, озноб и проливной пот, усиление кашля, одышки, увеличение количества мокроты.
Симптомы местно-распространенного рака наблюдаются у больных с метастатическим поражением лимфатических узлов средостения или при непосредственной инвазии опухоли в органы и ткани грудной полости. Все клинические признаки данной группы — поздние и свидетельствуют о неблагоприятном прогнозе заболевания.
Синдром верхней полой вены обусловлен нарушением оттока венозной крови от головного мозга и верхней половины тела. Больные жалуются на головокружение, головные боли, одышку, сонливость, обморочные состояния. Характерными признаками синдрома являются цианоз и отек лица, шеи, верхних конечностей, грудной клетки, набухание яремных вен, появление подкожных венозных коллатералей на грудной стенке.
Дисфагия обусловлена метастазами в лимфатических узлах заднего средостения или непосредственным распространением опухоли на пищевод.
Осиплость голоса встречается у больных раком левого легкого и свидетельствует о вовлечении в опухолевый процесс возвратного гортанного нерва.
Симптомы диссеминации опухоли: снижение массы тела, неврологическая симптоматика, боли в костях.
Паранеопластические синдромы: неопластическая гиперкальциемия, гипертрофическая остеоартропатия.
Физикальные данные скудные. При аускультации на стороне поражения может отмечаться ослабление везикулярного дыхания, обусловленное ателектазом.
Рентгенологическая диагностика. У больных с преимущественно эндобронхиальной формой рака тень опухоли часто не выявляется, а рентгенологические изменения обусловлены нарушением вентиляции. Вначале, когда нет полного стеноза бронха, возникает локальная эмфизема, обусловленная задержкой воздуха в отделах легкого дистальнее карциномы. Когда опухоль полностью перекрывает просвет бронха, формируется ателектаз: участок интенсивного гомогенного затемнения с четкими контурами в соответствующем легочном поле. Сегментарные и долевые ателектазы обычно имеют треугольную форму с основанием, обращенным к периферии. У больных с ателектазом всего легкого выявляется массивное затемнение гемиторакса со смещением средостения в сторону поражения. При перибронхиальной форме рака на рентгенограмме выявляется затемнение с нечеткими контурами в проекции опухолевого узла. Нарушения бронхиальной проходимости могут оказаться незначительными или полностью отсутствовать. Наиболее труден для первичной диагностики вариант перибронхиального роста, когда опухоль стелется вдоль бронхов, непосредственно не визуализируется и не сопровождается гиповентиляцией. В подобных случаях рентгенологически определяются тяжистые тени, расходящиеся от корня по направлению к периферическим отделам легкого.
Развитие обструктивного пневмонита в ателектазе рентгенологически проявляется участками просветления, которые соответствуют полостям деструкции. Нередко при рентгенографии выявляется плевральный выпот, который может быть вызван воспалением в ателектазе, сдавливанием крупных сосудистых стволов или же диссеминацией опухоли по листкам плевры и перикарду.
Нередко пневмонит на рентгенограммах может скрывать центральную обструкцию бронхов. В этом случае эффективно использование компьютерной томографии, которая решает следующие задачи:
* уточнить наличие и солитарность образования, выявить возможные метастазы;
* изучить размеры, структуру, плотность и контуры опухоли;
* определить взаимоотношение опухолевых масс с морфологическими структурами корня легкого и средостения;
* уточнить возможное происхождение опухоли;
* изучить изменения легочной ткани;
* выявить поражение лимфатических узлов средостения.
Верифицирующим методом диагностики центрального рака является бронхоскопия, которая дает информацию об уровне поражения бронхиального дерева и состоянии слизистой бронхов. Эндоскопическими признаками рака являются:
* визуальное обнаружение опухоли,
* ригидное сужение стенки бронха,
* уплощение карины или шпоры устья бронха,
* кровоточивость слизистой и
* так называемое «мертвое» устье, когда бронх не участвует в дыхании.
Из наиболее измененного участка слизистой оболочки берется биопсия, материал подвергается цитологическому и гистологическому исследованию, уточняющему гистологический вариант опухоли.
1.5 Обтурационный ателектаз (уплотнение легочной ткани невоспалительной природы) — это спадение легкого или его части, наблюдаемое при прекращении доступа воздуха в альвеолы. Помимо злокачественных опухолей легких причинами обтурационного ателектаза могут стать: туберкулез (в результате сдавления бронха увеличенными лимфатическими узлами или вследствие прорыва в бронх казеозных масс с закупоркой просвета бронха),
склеротический бронхит, инородные тела, послеоперационный период (вследствие закупорки бронха слизью при нарушении дренажной функции бронхов на фоне поверхностного дыхания).
Клиника: жалобы на инспираторную одышку и кашель, сухой и свистящий вначале, а затем надсадный и мучительный. Данные физикального обследования зависят от величины спавшегося участка легкого. При значительной величине ателектаза пораженная сторона может быть уменьшена в размерах, отстает при дыхании, межреберные промежутки втянуты и сужены, цианоз кожных покровов. Голосовое дрожание ослаблено или не определяется. Над зоной ателектаза определяется тупой перкуторный звук, смещение границ относительной сердечной тупости в пораженную сторону вследствие смещения сердца и средостения. Дыхание резко ослаблено или не проводится.
Рентгенологически — гомогенное затемнение соответствующее всей доле, отдельным сегментам или долькам, суженные межреберья, смещение средостения в пораженную сторону, более высокое стояние диафрагмы по отношению к здоровому легкому, смещение сердца на вдохе в сторону ателектаза, а на выдохе — в здоровую (симптом Гольцкнехта-Якобсона). При компьютерной томографии, ателектаз характеризуется четкими вогнутыми контурами, имеет форму пораженной структурной единицы легкого, выявляется сужение или полная обтурация бронха.
1.6 Инфаркт легкого является следствием тромбоэмболии легочной артерии и возникает в 10-30% случаев ТЭЛА. Предрасполагающими факторами венозного тромбоза и ТЭЛА являются вынужденная гиподинамия больных, сердечная недостаточность, перенесенный или имеющийся тромбофлебит нижних конечностей, хирургические вмешательства, переломы и травмы нижних конечностей с длительной иммобилизацией, злокачественные новообразования, пожилой возраст, беременность, ожирение, прием эстрогенов.
Клиника: одышка, боли в грудной клетке, повышение температуры тела, кашель, кровохарканье (наблюдается у 30% больных), бледность кожных покровов с пепельным оттенком (выраженный цианоз имеет место при массивной ТЭЛА), набухание шейных вен, патологическая пульсация в эпигастральной области, тахикардия, артериальная гипотензия, над зоной инфаркта могут выслушиваться сухие и мелкопузырчатые хрипы. Во втором межреберье слева от грудины выслушивается акцент II тона и систолический шум. Над мечевидным отростком или в четвертом межреберье у левого края грудины отмечается ритм галопа.
На ЭКГ отклонение ЭОС вправо, SI-QIII, подъем ST, уплощение или инверсия зубца Т в отведениях III, aVF, V1-V2. ЭхоКГ: повышение давления в легочной артерии, дилатация правого желудочка. Скрининг — определение Д-димера. При рентгенологическом обследовании определяется затемнение чаще субплеврально, клиновидной формы, верхушкой обращенное к корню легкого с нечеткими контурами, однородной структуры, умеренной интенсивности, высокое стояние купола диафрагмы на стороне поражения. Выбухание конуса легочной артерии, расширение тени сердца вправо, корень легкого расширен, деформирован.
Верифицирует диагноз пульмосцинтиграфия: дефекты наполнения изотопа («холодные зоны») и ангиопульмонография: расширение легочной артерии, культя сосуда, отсутствие контрастирования сосудов дистальнее места обтурации.
1.7 Эозинофильный инфильтрат (эозинофильная пневмония, синдром Леффлера) — полиэтиологическое аллергическое заболевание, характеризующееся развитием главным образом воспалительно-аллергической реакцией легочной ткани в виде «летучих» инфильтратов. Встречается в любом возрасте одинаково часто у мужчин и у женщин. Аллергены: лекарства (аспирин, пенициллины, сульфаниламиды, барбитураты, витамины и др.), пыльца растений, грибы рода аспергиллюс, пищевые продукты, глисты. В отдельных случаях потенциальный аллерген обнаружить не удается. В анамнезе у больных или у родственников — аллергические заболевания. В дебюте могут иметь место катаральные явления со стороны верхних дыхательных путей. В дальнейшем — общее недомогание, потливость, одышка, боли в груди, субфебрильная или фебрильная лихорадка, кашель сухой или со скудной мокротой лимонно-желтого цвета. Возможны другие проявления аллергии: крапивница, отек Квинке, «летучие» артриты, узловатая эритема. Физикально: может определяться локальное укорочение перкуторного звука, сухие или влажные мелкопузырчатые хрипы.
В общем анализе крови эозинофилия до 30-50%, в мокроте также могут определяться эозинофилы. При рентгенологическом исследовании эозинофильный инфильтрат по форме приближается к неправильной округлой или овальной (облаковидный), гомогенный, контуры нечеткие, средней интенсивности. Характерна летучесть: может бесследно исчезнуть в течение 1 недели или сменить локализацию. Эффективна терапия глюкокортикостероидами.
2. Округлые инфильтраты
2.1 Периферический рак легкого представляет из себя опухоль, развивающуюся из дистального участка сегментарного или более мелкого бронха. Выделяют следующие клинико-анатомические формы:
1. Шаровидная — наиболее частая разновидность периферического рака. Опухоль имеет вид узла, овальной или округлой формы без капсулы. Структура новообразования бывает однородной, но нередко в толще узла определяются участки распада и кровоизлияний.
2. Пневмониеподобная (или диффузная) форма характерна для бронхиолоальвеолярной аденокарциномы. Опухоль развивается из пневмоцитов и макроскопически выглядит как участок инфильтрации легочной паренхимы, часто с очагами распада. Опухолевый процесс распространяется по доле легкого из одного или нескольких первичных опухолевых очагов в легочной паренхиме, затем происходит слияние их в единый опухолевый конгломерат — инфильтрат.
3. Полостной рак.
Особой формой является периферический рак верхней доли легкого с синдромом Пенкоста — опухоль инфильтрирует прилежащие органы и нервные стволы. Клиника: боли в верхней части плеча, плечевом поясе (по локтевой стороне) вследствие прорастания шейно-плечевого сплетения. Боли в межлопаточном пространстве и на передней поверхности грудной клетки вследствие прорастания межреберных нервов и задних отрезков II-IV ребер. Слабость мышц кисти, парестезии, расстройства чувствительности участков кисти и предплечья, иннервируемых n. Medianus (CVII — Th1-2). Синдром Горнера: птоз, миоз, энофтальм (вследствие повреждения нервов шестого симпатического ганглия. Осиплость голоса встречается у больных раком левого легкого и свидетельствует о вовлечении в опухолевый процесс возвратного гортанного нерва.
Шаровидная форма периферического рака длительно протекает бессимптомно и обычно выявляется при профилактическом ФГ обследовании. Симптомы опухоли проявляются тогда, когда она прорастает плевру, сдавливает достаточно крупный бронх с формированием ателектаза или начинает метастазировать. Физикальные данные также малоинформативны, учитывая малые размеры узла.
При рентгенологическом исследовании выявляется негомогенное затемнение неправильной округлой формы, средней интенсивности, с волнистым или неровным контуром; по периферии затемнения могут быть выявлены короткие линейные тени, уходящие в окружающую легочную ткань («усики»). Часто видна «дорожка» к корню легкого или к плевре, что свидетельствует о лимфогенном и периваскулярном распространении карциномы.
При пневмониеподобной форме периферического рака вначале бывает сухой кашель, затем появляется мокрота — скудная, вязкая, переходящая в последующем в жидкую, обильную, пенистую. С присоединением инфекции клиническое течение опухоли приобретает сходство с рецидивирующей пневмонией, сопровождающейся повышением температуры, болями в груди, кашлем с обильным количеством мокроты, одышкой и выраженной интоксикацией.
При полостной форме периферического рака в отличие от абсцедирующей пневмонии полость обычно расположена эксцентрично и не содержит жидкости. В центральных отделах полостной карциномы обычно находится некротическая ткань.
Рентгенологическое обследование дополняется томографическим, которое решает те же вопросы, что и при центральном раке легкого.
Для верификации диагноза используется бронхоскопия с аспирацией содержимого приводящего бронха и последующим его цитологическим исследованием или трансторакальная биопсия под рентгенологическим контролем.
2.2 Туберкулома — клиническая форма вторичного (редко первичного) туберкулеза, при которой в легочной ткани формируется инкапсулированное казеозно-некротическое объемное образование диаметром более 10 мм. Формированию туберкулемы предшествует инфильтративная (чаще) или очаговая формы туберкулеза. Это так называемые истинные туберкулемы. При относительно напряженном клеточном иммунитете происходит рассасывание экссудативного компонента специфического воспаления, а казеозно-некротическое ядро окружается двухслойной капсулой. Могут быть ложные туберкулемы (псевдотуберкулемы), которые образуются из туберкулезных каверн при облитерации дренирующего бронха и заполнения полости грануляциями и казеозными массами.
Классификация.
* мелкие (до 2 см), ? средние (2-4 см),
* крупные (более 4 см). По количеству:
* единичные,
* множественные; По течению:
* прогрессирующие (с развитием перифокальной инфильтрации, распада, появления в окружающей ткани очагов бронхогенного отсева),
* стабильные (отсутствие перифокальной реакции и признаков распада в туберкулеме),
* регрессирующие (уменьшение размеров туберкулемы, уплотнение, фрагментация, инкрустация казеозных масс солями кальция).
Клиническая картина при туберкулеме достаточно скудная и зависит от типа ее течения. Туберкулемы со стабильным или регрессирующим течением протекают бессимптомно и выявляются при профилактических флюорографических обследованиях населения. При прогрессировании туберкулемы появляются симптомы интоксикации, кашель (сухой или с небольшим количеством мокроты), возможно кровохарканье.
Укорочение перкуторного звука можно обнаружить при крупных размерах туберкулемы, расположенных субплеврально. При прогрессирующей туберкулеме с наличием распада и перифокального воспаления могут выслушиваться непостоянные и немногочисленные влажные хрипы.
Изменения в клиническом и биохимическом анализах крови неспецифичны и появляются только в периоде прогрессирования процесса. Туберкулиновые реакции нормергические, но иногда могут быть гиперергическими. Функция внешнего дыхания не нарушена.
На обзорной рентгенограмме органов грудной клетки определяется фокус затемнения округлой формы, средний интенсивности с четкими контурами (синдром округлой тени) с локализацией в I, II или VI сегментах. Конгломератная туберкулема может иметь неправильную форму и полициклический наружный контур. При прогрессировании туберкулемы контуры вследствие перифокального воспаления становятся нечеткими, размытыми. В фазе распада появляется эксцентрично расположенная полость щелевидной или серповидной формы, «дорожка» к корню легкого за счет дренирующего бронха, очаги обсеменения в окружающей легочной ткани. Важной особенностью рентгенологической картины туберкулемы в отличие от других заболеваний, сопровождающихся синдромом округлой тени, является наличие в окружающей легочной ткани немногочисленных полиморфных очагов и пневмофиброза.
Бактериовыделение обычно скудное и возникает в фазе распада туберкулемы. Микобактерии туберкулеза чаще обнаруживаются только методом посева мокроты на питательные среды. Диагностический материал для верификация диагноза может быть получен с помощью фибробронхоскопии с чрезбронхиальной биопсией патологического образования, трансторакальной биопсии или пробной торакотомии с гистологическим и микробиологическим исследованием материала.
2.3 Инфильтративный туберкулез (лобулярный и округлый инфильтраты).
При этих клинических формах преобладает продуктивная реакция, а зона перифокального воспаления относительно невелика. Течение процесса малосимптомное. У больных может наблюдаться повышенная утомляемость, снижение работоспособности и аппетита, раздражительность, эпизодические повышения температуры тела. Стетоакустические изменения могут отсутствовать. Учитывая малую выраженность симптомов, они не обращаются за медицинской помощью, и заболевание выявляется только при периодических флюорографических обследованиях.
Бронхолобулярный инфильтрат: ограниченное затемнение полигональной формы чаще в кортикальной зоне I, II, IV сегментов до 3 см в диаметре, низкой или средней интенсивности, с нечеткими контурами, вытянуто по направлению к корню.
Округлый инфильтрат: ограниченное затемнение средней интенсивности, округлой формы без четких контуров, негомогенное. Часто локализуется в подключичной зоне (классический инфильтрат Ассманна-Редекера). При распаде в центре фокуса появляется просветление без четкого внутреннего и наружного контуров, к корню легкого отходит «дорожка» дренирующего бронха (симптом «теннисной ракетки»), в окружающей легочной ткани определяются свежие очаги бронхогенного обсеменения.
Реакция Манту обычно нормэргическая. В общем анализе мокроты определяются КУМ, могут выявляться свежие эластические волокна, указывающие на формирование полости распада, или обызвествленные эластические волокна и соли кальция, характерные для обострения старых туберкулезных очагов.
Если отсутствуют достаточные данные для установления диагноза туберкулеза, проводят бронхоскопию с биопсией бронха или легкого.
2.4 Эхинококкоз лёгкого характеризуется развитием кисты. Лёгкие как мишень паразита встречаются в 20-30% случаях эхиноккоза. Долгое время заболевание протекает бессимптомно. В этот период кисты выявляются при профилактических флюорографических обследованиях и могут достигать 5-8-10 см в диаметре. Затем появляются слабо выраженные признаки интоксикации: утомляемость, слабость, иногда тошнота. По мере роста кисты и сдавлении ею окружающих тканей, возникает боль в груди, кашель (вначале сухой, затем с мокротой), кровохарканье, одышка. При больших кистах возможна деформация грудной клетки, выбухание межреберных промежутков. Эхинококковая киста может осложняется перифокальным воспалением лёгочной ткани, сухим или экссудативным плевритом. Возможно нагноение кисты, прорыв её в бронх или в плевральную полость. Прорыв кисты в бронх сопровождается приступообразным кашлем с большим количеством светлой мокроты, содержащей примесь крови, чувством нехватки воздуха, цианозом. В случае прорыва кисты в плевральную полость появляются острая боль в груди, озноб, повышение температуры тела, иногда развивается анафилактический шок. В плевральной полости определяется жидкость. У больных эхинококкозом легких периодически может появляться крапивница. При перкуссии определяется притупление перкуторного звука при больших размерах кисты и формировании ателектазов, аускультативные данные разнообразны и неспецифичны.
В общем анализе крови можно выявить эозинофилию, лимфоцитоз, повышение СОЭ. Рентгенологически эхинококковая киста — это округлое затемнение с четкими контурами, интенсивное, гомогенное. Характерно изменение формы затемнения при глубоком вдохе (симптом Неменова). Иногда наблюдается также узкое чашеобразное просветление над уплотнением. После откашливания остается округлой формы, наполненное воздухом пространство.
Диагноз основывается на данных эпидемиологического анамнеза, клиникорентгенологических признаках, положительных результатах аллергологической пробы (реакция Касони), обнаружении сколексов эхинококка в мокроте (при прорыве кисты в бронх) или в плевральной жидкости (при прорыве кисты в плевральную полость). Используют серологические методы диагностики на обнаружение антител к эхинококку классов IgG.
3. Очаговые инфильтраты
3.1 Очаговая пневмония (см. раздел 1.1).
3.2 Очаговый туберкулез легких характеризуется наличием немногочисленных очагов, преимущественно продуктивного характера, в ограниченном участке одного или обоих легких и занимающих 1-2 сегмента, и малосимптомным клиническим течением. Диагностируется у 6-15% впервые выявленных больных туберкулезом.
Различают свежий (мягко-очаговый) и хронический (фиброзно-очаговый) варианты течения.
При свежем очаговом туберкулезе в интактной легочной ткани, обычно в I, II или VI сегментах, формируется внутридольковая казеозная бронхопневмония с экссудативным компонентом (очаг Абрикосова). Процесс ограниченный и клинически может протекать бессимптомно. При выраженном экссудативном компоненте воспаления могут быть маловыраженные симптомы интоксикации (утомляемость, снижение работоспособности, непостоянный субфебрилитет, ухудшение аппетита, раздражительность, у молодых женщин нарушение менструального цикла и др.) и «грудные» (кашель с незначительным количеством слизистой мокроты). При физикальном исследовании изменения могут отсутствовать или выявляется укорочение перкуторного звука в проекции I-II сегментов, при аускультации — ослабленное дыхание над зоной поражения и редко немногочисленные мелкопузырчатые хрипы на высоте вдоха после покашливания. При рентгенологическом исследовании в I, II, VI сегментах определяются единичные или немногочисленные тени размерами до 10 мм, малой интенсивности, без четких контуров с тенденцией к слиянию.
Хронический очаговый туберкулез патоморфологически характеризуется наличием в легочной ткани в пределах 1-2 сегментов на фоне ограниченного перибронхиального и периваскулярного пневмосклероза инкапсулированных, частично фиброзированных очагов с сохранением в них элементов активного специфического воспаления (очаги Ашоффа-Пуля). Туберкулезный процесс приобретает хроническое волнообразное течение с периодами ремиссии и обострения. Для ремиссии характерно отсутствие клинических симптомов, при обострении процесса появляются симптомы интоксикации, кашель со скудным количеством слизистой мокроты, редко наблюдается кровохарканье. При физикальном обследовании вследствие развития соединительной ткани можно обнаружить при топографической перкуссии сужение поля Кренига и высоты стояния верхушки на стороне поражения, при сравнительной перкуссии — укорочение звука локально, аускультативно — жесткое дыхание. Рентгенологически хронический очаговый туберкулез характеризуется наличием в пределах 12 сегментов (чаще в I, II, VI) немногочисленных очаговых теней размерами 3-6 мм, средней и высокой интенсивности, с четкими контурами, без тенденции к слиянию. При обострении процесса контуры очагов становятся нечеткими, а в окружающей ткани могут появляться свежие очаговые тени.
В общем анализе крови могут быть выявлены лимфоцитоз, сдвиг влево и повышенная СОЭ. Туберкулиновые реакции чаще нормэргические. Для верификации очагового туберкулеза применяются компьютерную томографию и различные методы обнаружения микобактерий туберкулеза (бактериоскопический, бактериологический, ПЦР). Материал для исследования может быть получен с помощью бронхоскопии с аспирационной биопсией или бронхоальвеолярным лаважем.
Помимо периферического рака и туберкулезного процесса причиной появления округлого затемнения или очага в легких, особенно у лиц молодого возраста, могут быть 3.3 доброкачественные опухоли (аденома, невринома, гемангиома, гамартома остеохондрома и др.) и 3.4 ретенционные (заполненные) кисты легких. Доброкачественные опухоли и кисты характеризуются бессимптомным течением, не дают роста, не метастазируют и выявляются, в основном, при профилактическом флюорографическом обследовании. Среди опухолей исключение составляет аденома. Это единственная доброкачественная опухоль, которая может характеризоваться появлением новых участков поражения, т.е. метастазированием. Рентгенологически выявляется округлое или овальное затемнение различной локализации, контур затемнения четкий, гладкий, реже бугристый, окружающий легочный фон не изменен, структура тени гомогенная. Несмотря на относительную безобидность доброкачественных опухолей и ретенционных кист, учитывая возможные альтернативы, для дифференциальной диагностики необходимо использовать все имеющиеся возможности, включая КТ, МРТ, бронхоскопию, трансторакальную биопсию и пробную торакотомию, которая является не только методом диагностики, но и способом лечения.
Синдром легочного инфильтрата труден для дифференциальной диагностики, поскольку сопровождает многие заболевания. Поэтому можно следовать рекомендациям профессора Л.И. Дворецкого: «Для интерниста оправдано положение — любой легочный инфильтрат требует исключения туберкулеза, особенно при наличии факторов риска и отсутствия эффекта антибиотикотерапии». А также совету академика Л.Д. Линденбратена — «лечить, как пневмонию и обследовать, как рак».
Тестовые задания по теме.
Выберите один или несколько правильных ответов.
1. СИНДРОМ ЛЕГОЧНОГО ИНФИЛЬТРАТА — ЭТО
1) рентгенологический синдром, характеризующийся затемнением легочной ткани различного размера и формы
2) клинико-рентгенологический синдром, характеризующийся признаками уплотнения легочной ткани: при перкуссии легких — укорочением перкуторного тона, при рентгенологическом исследовании — инфильтративным затемнением различной величины и формы
3) синдром при котором выявляется укорочение прекуторного звука или ослабление дыхания в зоне уплотнения легочной ткани
2. КАКОВА ВОЗМОЖНАЯ ПРИРОДА ИНФИЛЬТРАТОВ
4) геморрагическая
3. ПНЕВМОНИЯ — ЭТО
1) острое или хроническое инфекционное заболевание преимущественно бактериальной этиологии, характеризующееся очаговым поражением респираторных отделов легких, наличием внутриальвеолярной экссудации, выявляемой при физикальном и/или рентгенологическом исследовании, выраженными в различной степени лихорадочной реакцией и интоксикацией
2) острое инфекционное заболевание преимущественно бактериальной этиологии, характеризующееся поражением респираторных отделов легких, наличием внутриальвеолярной экссудации, выявляемой при физикальном и/или рентгенологическом исследовании, выраженными в различной степени лихорадочной реакцией и интоксикацией
3) инфекционное заболевание, при котором поражается респираторный отдел и бронхиальное дерево выявляемой при физикальном и/или рентгенологическом исследовании, выраженными в различной степени лихорадочной реакцией и интоксикацией
4. КЛИНИЧЕСКИМИ КРИТЕРИЯМИ ПНЕВМОНИИ ТЯЖЕЛОГО ТЕЧЕНИЯ ЯВЛЯЮТСЯ 1) общее тяжелое состояние больного
2) признаки сердечно-сосудистой недостаточности
3) частота дыхательных движений > 30 в 1 мин
4) наличие осложнений
5. РАЗВЕРНУТЫЙ ДИАГНОЗ У БОЛЬНОГО С ПНЕВМОНИЕЙ ДОЛЖЕН ОТРАЖАТЬ
1) этиологию, локализацию процесса, степень тяжести, сопутствующие заболевания
2) этиологию, локализацию процесса, степень тяжести, характер течения, осложнения, степень дыхательной недостаточности
3) этиологию, локализацию процесса, степень тяжести, характер течения, осложнения
4) этиологию, локализацию процесса, степень тяжести, характер течения, степень дыхательной недостаточности
6. САМЫМИ ЧАСТЫМИ ВОЗБУДИТЕЛЯМИ ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ ЯВЛЯ-
1) Chlamidia pneumonie, Legionella, Staphylococcus aureus pneumonie 2) Klebsiella pneumonie; Pseudomonas aeruginosa; Staphylococcus spp.
3) Streptococcus pneumoniae, Haemophilus influenzae, Micoplasma pneumonie
4) Streptococcus pneumoniae, Chlamidia pneumonie, Legionella
7. ОБЪЕКТИВНЫМИ КРИТЕРИЯМИ ДИАГНОСТИКИ ПНЕВМОНИИ ЯВЛЯЮТСЯ
1) инфильтрация легочной ткани, выявляемая при рентгенографии грудной клетки в 2-х проекциях, микробиологическое исследование мокроты
2) наличие лихорадки, интоксикации
3) усиление голосового дрожания, локальное притупление перкуторного тона, наличие влажных мелкопузырчатых хрипов или крепитации
4) боли за грудиной, не связанные с дыханием
8. КАКАЯ ПНЕВМОНИЯ НАЗЫВАЕТСЯ ГОСПИТАЛЬНОЙ
1) пневмония, развившаяся в первые 48-72 часа от момента госпитализации
2) пневмония, развившаяся в течение первых четырех суток от момента госпитализации
3) пневмония, развившаяся не ранее чем через 48-72 часа от момента госпитализации
4) пневмония, которая была диагностирована в стационаре
9. К ЛЕГОЧНЫМ ОСЛОЖНЕНИЯМ ПНЕВМОНИИ ОТНОСЯТСЯ
1) парапневмонический плеврит, эмпиема плевры
2) абсцесс и гангрена легких
3) бронхиальная обструкция
4) острая дыхательная недостаточность (дистресс-синдром)
10. КАКОЙ ИЗ ПЕРЕЧИСЛЕННЫХ КРИТЕРИЕВ УКАЗЫВАЕТ НА ТЯЖЕЛОЕ ТЕЧЕНИЕ ПНЕВМОНИИ:
1) лейкоцитоз (> 20 Г/л) или лейкопения ( 55%).
Целью длительной О2-терапии является повышение РаО2 до уровня не менее 8,0 kPa (60 mm рт.ст.) в покое на уровне моря, и/или SaO2 не менее 90%, т.е. показателей, обеспечивающих нормальную оксигенацию жизненно важных органов.
Буллэктомия является самой старой хирургической процедурой по поводу буллезной эмфиземы. Удаление большой буллы, которая не принимает участия в газообмене, приводит к расправлению окружающей легочной паренхимы. Такая операция уменьшает одышку и улучшает функцию легких.
Операция уменьшения объема легкого является операцией, при которой удаляется часть легкого для уменьшения гиперинфляции и достижения более эффективной насосной работы респираторных мышц. При этом повышается эластическая тяга легких, уменьшая выраженность бронхиальной обструкции.
Трансплантация легкого у тщательно отобранных пациентов с очень тяжелым течением ХОБЛ улучшает качество жизни и функциональные показатели. Критерии отбора:
* ОФВ1 6,7 kPa (50 mm рт.ст.),
* признаки вторичной легочной гипертензии.
Обострение ХОБЛ определяется как событие в течении заболевания, характеризующееся острым изменением имеющихся у больного одышки, кашля и/или отделения мокроты по сравнению с обычным уровнем, которое выходит за рамки ежедневных колебаний, что является основанием для изменения плановой терапии по поводу ХОБЛ.
Наиболее частыми причинами обострения являются инфекция трахеобронхиального дерева и загрязнение воздуха, однако причины примерно одной трети случаев обострений установить не удается. Критерии обострения:
* усиление одышки,
* снижение толерантности к физическим нагрузкам,
* увеличение количества мокроты, ? изменение характера мокроты на гнойный, ? повышение температуры тела.
Измерение функциональных показателей в период обострения затруднено и может быть неточным, поэтому спирометрия не рекомендуются для рутинного применения.
Показано выполнение пульсоксиметрии и анализа газов артериальной крови. Если при дыхании комнатным воздухом РаО2 8 кПа, или 60 мм рт.ст.), и/или тяжелый/ухудшающийся респираторный ацидоз (pH 5 мг/л)
Выбор антибиотика зависит от тяжести обострения и наличия факторов риска неблагоприятного исхода, к которым относятся:
* наличие сопутствующих заболеваний,
* тяжелая форма ХОБЛ,
* частые обострения (>3 в год),
* применение антибактериальных препаратов в последние 3 месяца.
Характер обострения Антибиотики первого ряда Альтернативные антибиотики Легкое обострение без факторов риска неблагоприятного исхода • ?-лактамы (ампициллин, амоксициллин),
• тетрациклин • ?-лактам/ингибитор ?лактамаз (амоксиклав),
• макролиды (азитромицин, кларитромицин, рокситромицин),
• цефалоспорины 2-го или 3-го поколений Умеренное обострение с фактором(ами) риска неблагоприятного исхода • ?-лактам/ингибитор ?лактамаз (амоксиклав, ампициллин/сульбактам),
• макролиды (азитромицин, кларитромицин, рокситромицин),
• цефалоспорины 2-го или 3-го поколений • фторхинолоны (левофлоксацин, моксифлоксацин) Тяжелое обострение с факторами риска неблагоприятного исхода (высока вероятность инфекции P.
Aeruginosa) • фторхинолоны (ципрофлоксацин, левофлоксацин — высокие дозы)
• ?-лактам с активностью против P. aeruginosa (цефалоспорины 4-го поколения, карбапенемы) 5. Респираторная поддержка.
Неинвазивная интермиттирующая вентиляция (НИВ) с помощью приборов, создающих либо отрицательное, либо положительное давление через носовую или лицевую маску.
Показания.
* Частота дыхательных движений > 25 в минуту.
* Одышка с использованием вспомогательных дыхательных мышц и парадоксальным движением живота.
* Ацидоз (pH ? 7,35) и/или гиперкапния (PaCO2 >6 кПа, или 45 мм рт.ст.) Противопоказания (может присутствовать любой из них).
* Остановка дыхания.
* Сердечно-сосудистая нестабильность (гипотензия, аритмии, инфаркт миокарда).
* Изменения ментального статуса; неспособность пациента к сотрудничеству с медицинским персоналом.
* Высокий риск аспирации.
* Вязкий или обильный бронхиальный секрет.
* Недавняя лицевая или гастроэзофагеальная хирургическая операция.
* Некорригируемая назофарингеальная патология.
* Ожоги.
Искусственная вентиляция легких.
* Непереносимость НИВ или неудача НИВ или наличие противопоказаний к НИВ.
* Тяжелая одышка с использованием вспомогательных дыхательных мышц и парадоксальным движением живота.
* Частота дыхательных движений > 35 в минуту.
* Тяжелый ацидоз (pH 8 кПа, или 60 мм рт.ст.).
* Сонливость, нарушенный ментальный статус.
* Сердечно-сосудистые осложнения (гипотензия, шок).
* Другие осложнения (метаболические аномалии, сепсис, пневмония, тромбоэмболия легочных артерий, баротравма, массивный плевральный выпот).
1.2. Туберкулез бронхов.
К бронхиальной обструкции приводит скопление творожистых масс в просвете бронхов.
Клиническая картина туберкулезной инфекции в этом случае дополняется экспираторной одышкой и сухими свистящими хрипами в легких при аускультации.
Компьютерная томография помогает выявить локальное сужение бронхов. Бронхоскопия с биопсией верифицирует диагноз.
1.3. Муковисцидоз — системное наследственное заболевание, характеризующееся поражением желёз внешней секреции, тяжёлыми нарушениями функций органов дыхания и желудочно-кишечного тракта.
Причиной патологических изменений при муковисцидозе является мутация гена трансмембранного регулятора муковисцидоза. Этот белок регулирует транспорт электролитов (главным образом хлора) через мембрану клеток, выстилающих выводные протоки экзокринных желез. Мутация приводит к нарушению структуры и функции синтезируемого белка, в результате чего секрет, выделяемый этими железами, становится чрезмерно густым и вязким. Повышенная вязкость бронхиального секрета приводит к развитию мукостаза и сужению просвета мелких бронхов и бронхиол, что способствует развитию эмфиземы, а при полной закупорке бронхов — формированию ателектазов. Формы муковисцидоза:
* смешанная (легочно-кишечная, 75-80%); ? бронхолегочная (15-20%); ? кишечная (5%).
Начинается заболевание в детском возрасте, для него характерны кашель с отделением вязкой мокроты, частые бронхиты, пневмонии, снижение аппетита, ограничение двигательной активности.
Объективно: кожные покровы бледные с землистым оттенком, цианоз различной степени выраженности, одышка в покое, бочкообразная форма грудной клетки, уменьшение массы тела. Могут иметь место деформация грудины по типу «клиновидной» и симптом «барабанных палочек». При перкуссии — коробочный оттенок перкуторного звука. При аускультации — ослабленное везикулярное дыхание, влажные мелко- и среднепузырчатые хрипы.
Кишечные проявления муковисцидоза обусловлены недостаточностью ферментативной активности желудочно-кишечного тракта, прежде всего — поджелудочной железы. Расщепление и всасывание питательных веществ снижено, в кишечнике преобладают гнилостные процессы, сопровождающиеся накоплением газов. Характерны: очень частый стул (суточный объём каловых масс значительно превышает возрастную норму), метеоризм, схваткообразные боли в животе, сухость во рту (что обусловлено высокой вязкостью слюны).
Возможно также снижение репродуктивной функции у мужчин в связи с недоразвитием или отсутствием семявыносящих протоков.
Для постановки диагноза заболевания необходимо наличие четырёх основных критериев:
1) хронический бронхолёгочный процесс,
2) кишечный синдром,
3) случаи муковисцидоза в семье,
4) положительные результаты потового теста (диагностически достоверным критерием муковисцидоза является содержание ионов хлора выше 60 ммоль/л и натрия — выше 70 ммоль/л).
2. Хронические заболевания с пароксизмальным характером диспноэ
2.1. Бронхиальная астма (см. раздел «Дифференциальный диагноз при синдроме бронхиальной обструкции»).
2.2. Биссиноз (профессиональная бронхиальная астма).
Развивается при длительном контакте с пылью (аллергенами) растительного или животного происхождения (хлопковая, льняная, древесная, шерстяная и др.).
Первые признаки заболевания появляются через 10-15 лет работы в контакте с пылью.
Основные проявления — приступообразная одышка, чувство стеснения в груди, приступообразный кашель, свистящие хрипы. Возможен субфебрилитет.
Обычно указанные симптомы наиболее выражены по понедельникам («симптом понедельника»), а к концу недели они уменьшаются или исчезают. Со временем появляются кашель с отделением вязкой мокроты, общая слабость, быстрая утомляемость.
В отличие от бронхиальной астмы развёрнутых приступов удушья при биссинозе не бывает.
Объем дополнительных методов исследования сходен с таковым при бронхиальной астме.
Основное значение в диагностике придается выявлению и документированию профессиональной вредности.
2.3. Трахеобронхиальная дискинезия (см. раздел «Дифференциальный диагноз при удушье»).
2.4. Загрудинный зоб — увеличение в размерах эктопически расположенной щитовидной железы, приводящее к сдавлению трахеи.
Может сопровождаться приступами удушья с появлением в легких свистящих хрипов.
Со стороны легких и сердца характерных изменений нет.
В ряде случаев выявляются клинические признаки гипертиреоза.
В мокроте непостоянно определяются эозинофилы.
Решающую роль в диагностике играет УЗИ и изотопные методы исследования щитовидной железы, позволяющие уточнить ее расположение и функциональную активность.
2.5. Синдром Чарджа-Стросса (см. раздел «Дифференциальный диагноз при удушье»).
2.6. Бронхолегочный аспергиллез (см. раздел «Дифференциальный диагноз при удушье»).
2.7. Гельминтозы.
Легочная форма описторхоза или аскаридоза характеризуется лихорадкой, кашлем, приступами удушья с определением в легких обилия сухих хрипов.
Отмечаются также диспептические явления, боли в правом подреберье, гепатомегалия.
В крови — эозинофилия.
Обнаружение яиц описторхиса или аскарид в кале подтверждает диагноз.
2.8. Центральный рак легких, карциноидная опухоль, опухоль средостения (см. раздел «Дифференциальный диагноз при удушье»).
3. Остропротекающая патология.
3.1. Анафилактический шок.
Характерно резкое снижение АД, удушье, боли в животе, тошнота, тахикардия. Может развиться крапивница.
В диагностике основное значение имеет аллергологический анамнез и непосредственная связь состояния с действием аллергена.
3.2. Отек Квинке (см. раздел «Дифференциальный диагноз при удушье»).
3.3. Синдром Мендельсона (см. раздел «Дифференциальный диагноз при удушье»).
3.4. Бронхиолит.
В анамнезе — связь заболевания с ОРВИ, лекарственной терапией, ингаляцией токсических аэрозолей.
В клинике преобладают прогрессирующая одышка, непродуктивный кашель, сухие свистящие хрипы в нижних отделах. Клиническая картина часто носит «застывший» характер. На поздних стадиях заболевания больные превращаются в «синих пыхтельщиков».
Рентгенологические изменения обнаруживаются в 50% случаев в виде гипервоздушности или слабовыраженной очагово-сетчатой диссеминации.
Компьютерная томография высокого разрешения позволяет выявить изменения в легких в 90% случаев: бронхоэктазы и мозаичное снижение прозрачности на выдохе.
При констриктивном бронхиолите наблюдается обструктивный тип нарушений функции внешнего дыхания: снижение скоростных потоковых показателей, повышение статических легочных объемов. Обструкция носит необратимый характер.
При пролиферативном бронхиолите иногда имеют место умеренные признаки рестрикции.
При анализе газового состава крови выявляют гипоксемию и гипокапнию.
3.5. Тромбоэмболия легочной артерии (ТЭЛА) — это полное или частичное перекрытие основного ствола или ветвей легочной артерии тромбом или эмболом из венозной системы большого круга кровообращения или правых отделов сердца.
Анамнестические данные:
• вынужденная гиподинамия больных
• перенесенный или имеющийся тромбофлебит нижних конечностей
• хирургические вмешательства
• переломы и травмы нижних конечностей с длительной иммобилизацией
• беременность
• острое начало болезни!
Клиническая классификация:
* массивная — поражено более 50 % объёма сосудистого русла лёгких (эмболия лёгочного ствола и/или главных лёгочных артерий); заболевание проявляется шоком и/или системной гипотензией;
* субмассивная — поражено 30-50 % объёма сосудистого русла лёгких (эмболия нескольких долевых или многих сегментарных лёгочных артерий); проявляется симптомами правожелудочковой недостаточности;
* немассивная — поражено менее 30 % объёма сосудистого русла лёгких (эмболия мелких дистальных лёгочных артерий); проявления отсутствуют либо минимальны (инфаркт лёгкого).
Клиника:
* внезапно возникающая одышка вплоть до удушья,
* боли в грудной клетке,
* артериальная гипотензия,
* бледность кожных покровов с пепельным оттенком (выраженный цианоз имеет место при массивной ТЭЛА),
* набуханием шейных вен,
* патологическая пульсация в эпигастральной области,
* во втором межреберье слева от грудины выслушивается акцент II тона и систолический шум,
* над мечевидным отростком или в четвертом межреберье у левого края грудины отмечается ритм галопа.
Скрининг: определение D-димера (до 0,5 пг/мл в норме).
ЭКГ: отклонение ЭОС вправо, SI-QIII, подъем ST, уплощение или инверсия зубца Т в отведениях III, aVF, V1-V2.
ЭхоКГ: повышение давления в легочной артерии, дилатация правого желудочка.
Верифицируют диагноз: ангиопульмонография — расширение легочной артерии, культя сосуда, отсутствие контрастирования сосудов дистальнее места обтурации; пульмосцинтиграфия — дефекты наполнения изотопа («холодные зоны»).
3.6. Инородные тела трахеи и бронхов (см. раздел «Дифференциальный диагноз при удушье»).
3.7. Отравление фосфорорганическими соединениями (см. раздел «Дифференциальный диагноз при удушье»).
3.8. Передозировка ?-блокаторов (см. раздел «Дифференциальный диагноз при удушье»).
3.9. Острая левожелудочковая недостаточность (см. раздел «Дифференциальный диагноз при удушье»).
Тестовые задания по теме.
Выберите один или несколько правильных ответов.
1. СИНДРОМ БРОНХИАЛЬНОЙ ОБСТРУКЦИИ — ЭТО
1) состояние, при котором наблюдается обратимое или необратимое сужение бронхов
2) состояние, характеризующееся приступообразным, реже — медленнопрогрессирующим развитием экспираторного или смешанного диспноэ с проявлениями гипоксии или гиперкапнии и снижением параметров бронхиальной проходимости
3) состояние, характеризующееся приступообразным, реже — медленнопрогрессирующим развитием экспираторного или смешанного диспноэ, полностью поддающимися лечению бронхолитиками.
4) состояние, приводящее к гипоскии или гиперкапнии на фоне снижения ЖЕЛ, ОФВ1 и других показателей ФВД.
2. К МЕХАНИЗМАМ ВОЗНИКНОВЕНИЯ БРОНХИАЛЬНОЙ ОБСТРУКЦИИ ОТНОСИТ-
СЯ ВСЁ, КРОМЕ
1) усиления слизеобразования
2) отёка стенки бронхов 3) альвеолярного отёка 4) бронхоспазма.
3. ДОСТОВЕРНЫМ ПРИЗНАКОМ ОБРАТИМОСТИ БРОНХИАЛЬНОЙ ОБСТРУКЦИИ
ЯВЛЯЕТСЯ
1) увеличение ОФВ1 после приёма В2-агонистов > чем на 15 %
2) уменьшение ОФВ1 после приёма В2-агонистов > чем на 15%
3) увеличение ОФВ1 после приёма ингаляционных кортикостероидов > чем на 15%
4) уменьшение ОФВ1 после приёма ингаляционных кортикостероидов > чем на 15%.
4. КАКИЕ МЕХАНИЗМЫ БРОНХИАЛЬНОЙ ОБСТРУКЦИИ ОТНОСЯТ К ОБРАТИМЫМ:
а) ГИПЕРСЕКРЕЦИЯ СЛИЗИ, б) БРОНХОСПАЗМ, в) ОТЕК СЛИЗИСТОЙ ОБОЛОЧКИ
БРОНХОВ, г) СКЛЕРОЗ СТЕНКИ БРОНХОВ, д) ЭКСПИРАТОРНЫЙ КОЛЛАПС БРОНХОВ
1) все варианты
4) а,б,в 5. КАКИЕ МЕХАНИЗМЫ БРОНХИАЛЬНОЙ ОБСТРУКЦИИ ОТНОСЯТ К НЕОБРАТИМЫМ: а) ГИПЕРСЕКРЕЦИЯ СЛИЗИ, б) БРОНХОСПАЗМ, в) ОТЕК СЛИЗИСТОЙ ОБОЛОЧКИ БРОНХОВ, г) СКЛЕРОЗ СТЕНКИ БРОНХОВ, д) ЭКСПИРАТОРНЫЙ КОЛЛАПС
БРОНХОВ 1) все варианты
2) а,б,г
6. КАКОВА НАИБОЛЕЕ ХАРАКТЕРНАЯ ЖАЛОБА ПРИ СИНДРОМЕ БРОНХИАЛЬНОЙ
1) инспираотрная одышка 2) экспираторная одышка 3) боли в грудной клетке.
4) снижение толерантности к физическим нагрузкам
7. КАКИЕ ЗАБОЛЕВАНИЯ ПРОТЕКАЮТ С БРОНХООБСТРУКТИВНЫМ СИНДРОМОМ
1) ретростернальный зоб
2) трахео-бронхиальная дискинезия
3) узелковый полиартериит
4) ТЭЛА 8. ВЫСОКИЕ ПОКАЗАТЕЛИ СОДЕРЖАНИЯ ЭРИТРОЦИТОВ И ГЕМОГЛОБИНА В КРО-
ВИ У БОЛЬНОГО С ХОБЛ СВИДЕТЕЛЬСТВУЮТ
1) об обострении заболевания
2) о вторичном эритроцитозе
3) о декомпенсации дыхательной недостаточности 4) о благоприятном течении заболевания.
9. ИНДЕКС ТИФФНО ПРИ БРОНХИАЛЬНОЙ ОБСТРУКЦИИ
2) повышается
3) не изменяется
4) проба не показательна.
10. ОТРАВЛЕНИЕ КАКИМИ ВЕЩЕСТВАМИ МОЖЕТ ПРИВЕСТИ К БРОНХООБСТРУКТИВНОМУ СИНДРОМУ
1) хлорорганическими
2) фосфорорганическими 3) метиловым спиртом 4) этиловым спиртом.
Ситуационная задача № 2.
Больной Н., 55 лет, обратился к участковому терапевту с жалобами на кашель по утрам с отделением вязкой зеленой мокроты, одышку при небольшой физической нагрузке, утомляемость.
Настоящее ухудшение около двух недель, связывает с перенесенной вирусной инфекцией. Кашель со слизистой мокротой отмечает около 10 лет. В течение последних 2 лет стал отмечать одышку. Иногда, когда чувствует себя хуже, по совету знакомых использует сальбутамол (по одной дозе утром и вечером), с кратковременным эффектом. Отмечает, что за последний год похудел примерно на 5 килограммов.
Работает плотником. Курит 20-30 сигарет в сутки более 35 лет. Аллергические реакции на пенициллиновые антибиотики и новокаин в виде крапивницы, отека Квинке. Гепатит, туберкулез, малярию, тифы, венерические заболевания отрицает. Кровь не переливали. Травм, операций не было. У матери бронхиальная астма, отец умер от рака желудка.
Общее состояние удовлетворительное. Акроцианоз. Пальпируемые лимфатические узлы не увеличены, безболезненные. Рост 170 см, вес 86 кг. Мышечный тонус сохранен, болезненности в мышцах нет. Отеков нет. Грудная клетка бочкообразная. Тип дыхания брюшной. Дыхательные движения грудной клетки симметричны. ЧД 21 в минуту. Пальпация грудной клетки безболезненна, эластичность снижена. При сравнительной перкуссии определяется коробочный оттенок звука над всей поверхностью легких. Подвижность нижнего легочного края справа и слева по задней подмышечной линии 3 см. При аускультации на фоне ослабленного дыхания выслушиваются диффузные сухие свистящие и жужжащие хрипы. Пульс одинаковый на обеих руках, 110 в 1 мин, ритмичный, удовлетворительного наполнения, ненапряжен. АД 110/65 мм рт.ст. Тоны сердца приглушены. Акцент II тона на легочной артерии. Слизистая ротоглотки не гиперемирована. Живот при пальпации мягкий, безболезненный. Печень и селезенка не пальпируются. Симптом Пастернацкого отрицательный. Щитовидная железа не пальпируется.
Вопросы:
1. Поставьте предварительный диагноз.
2. С какими заболеваниями следует проводить дифференциальную диагностику?
3. Составьте план дополнительного обследования.
4. Оцените результаты дополнительных методов обследования.
5. Сформулируйте клинический диагноз.
6. Определите тактику ведения и назначьте лечение.
Приложения к ситуационной задаче № 2
Анализ крови общий.
Эритроциты — 4,2 Т/л, Hb — 175 г/л, лейкоциты — 13,2 Г/л, эозинофилы — 1%, нейтрофилы: палочкоядерные — 6%, сегментоядерные -58%, лимфоциты — 25%, моноциты — 10%, СОЭ — 28 мм/ч.
Анализ мочи общий.
Соломенно-желтая, реакция кислая, уд. вес 1018, белок — следы, лейкоциты 3-5-8 в п/зрения, эритроцитов нет.
Анализ мокроты общий.
Желто-зеленая, лейкоциты — сплошь в поле зрения, эритроциты — 1-3 в поле зрения, альвеолярные макрофаги до 10 в поле зрения и скопления, эпителий плоский в умеренном количестве, АК, ВК отсутствуют.
Спирометрия: Индекс Тиффно 65%, ОФВ1 52% от должного. Проба с сальбутамолом: прирост ОФВ1 — 9%. Суточная вариабельность ПСВ — 12%.
Пульсоксиметрия: SрO2 — 88%.
ЭКГ ЧСС 100 в минуту, RIII>RII>RI, зубец Р высокий, заостренный; высокий зубец R в V1-2, глубокий зубец S в V5-6, единичные предсердные экстрасистолы.
Легочные поля повышенной прозрачности, корни структурны, расширены, легочный рисунок усилен, в нижних легочных полях деформирован
III. ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ ПРИ УДУШЬЕ
Удушье — крайняя степень выраженности одышки, сопровождающейся обычно мучительным чувством недостатка воздуха.
По механизму возникновения выделяют:
1. Удушье, обусловленное нарушением проходимости верхних дыхательных путей.
2. Удушье, обусловленное бронхиальной обструкцией.
3. Удушье при отеке легких.
4. Удушье при быстром уменьшении респираторной части легкого.
5. Удушье при заболеваниях диафрагмы.
6. Удушье при нарушении нервной регуляции ритма дыхания.
Механизмами развития удушья при нарушении проходимости верхних дыхательных путей являются непосредственное воздействие аллергенов, вирусных и бактериальных токсинов, сдавление извне и обтурация инородным телом. Скопление воспалительного экссудата, отек, фибринозные наложения, нарушение эластичности и тонуса мембранозной части трахеи уменьшают просвет дыхательных путей, вплоть до обструкции.
Механизмами развития удушья при бронхиальной обструкции являются бронхоспазм, отек слизистой оболочки бронхиол, гиперсекреция слизи и повышение ее вязкости.
Развитие удушья при отеке легких обусловлено декомпенсацией левожелудочковой недостаточности, при которой повышается венозное и капиллярное давление в системе малого круга кровообращения. В результате этого увеличивается внутригрудной объем крови и повышается легочный венозный и капиллярный объем, что в свою очередь уменьшает жизненную емкость легких. Дополнительным фактором, способствующим возникновению удушья, является повышение уровня стояния диафрагмы, что приводит к уменьшению остаточного объема легких. Это приводит к выраженному нарушению газообмена между альвеолами и капиллярами. При развитии некардиогенного отека легких имеют значение гипергидратация, повышение капиллярной проницаемости в альвеолах под влиянием токсинов и метаболических расстройств.
Возникновение удушья в результате уменьшения респираторной части легкого обусловлено сочетанием ряда факторов: выключением большого объема легочной ткани из газообмена (при субтотальной пневмонии); несоответствием между вентиляцией и перфузией из-за гиперсекреции и бронхоспазма, шунтированием крови в легких.
В основе удушья при нарушении нервной регуляции ритма дыхания лежит дискоординация автоматизма дыхательного центра и собственного ритма работы дыхательных мышц (при органических поражениях ЦНС), а также нейральной активации (реакции восприятия удушья), как результата стимуляции периферических рецепторов при гипервентиляционном синдроме.
Диагностический поиск.
Несмотря на то, что причиной удушья может быть огромное число заболеваний, более двух третей всех случаев, как правило, связаны с заболеваниями респираторной или сердечно-сосудистой систем.
Обязательные вопросы Комментарий Сердечно-сосудистые или бронхо-легочные заболевания в анамнезе? Факторы, провоцирующие удушье? Физическая нагрузка, контакт с аллергенами, другие. Боль в грудной клетке или ощущение перебоев в сердце? Инфаркт миокарда, эмболия легочной артерии, аритмия, спонтанный пневмоторакс. Наличие кашля, мокроты? Инфекция нижних дыхательный путей (пневмония, бронхит). Перенесённая вирусная инфекция в ближайший месяц? Миокардит. Побочное действие лекарственных веществ, интоксикации? Салицилаты, большие дозы теофиллина, метанол, этиленгликоль вызывают гиперпноэ. Факторы риска развития тромбоза глубоких вен голени и, как следствие, эмболии легочной артерии? Недавнее хирургическое вмешательство на органах живота или таза, злокачественные новообразования, длительная неподвижность, предшествующие тромбофлебит глубоких вен или эмболия легочной артерии, недавние роды, ожирение, применение оральных контрацептивов с высоким содержанием эстрогенов. Условия возникновения и скорость нарастания одышки? Внезапно развившаяся одышка в покое подозрительна на эмболию легочной артерии или спонтанный пневмоторакс.
Тяжёлая одышка, развившаяся за 1-2 часа, характерна для острой сердечной недостаточности или приступа бронхиальной астмы. Физикальное обследование.
Методика Комментарий Оценка гемодинамики Определение уровня артериального давления, частоты сердечных сокращений, кардиомонитор (при наличии боли, аритмии). Определение частоты дыхательных движений Возможности произнести фразу из нескольких слов без перерыва (речь сохранена при лёгкой степени и затруднена при тяжёлой степени дыхательной недостаточности). Измерение температуры тела Лихорадка может свидетельствовать об инфекции. Осмотр шеи Набухание шейных вен отражает повышение центрального венозного давления. Цианоз Не является надёжным признаком, т.к. он появляется на поздних стадиях тяжёлой гипоксемии. При наличии — «холодный» цианоз характерен для сердечной недостаточности, «теплый» — для дыхательной. Аускультация сердца Повреждение клапанов или разрыв межжелудочковой перегородки. Перкуссия легких • укорочение перкуторного звука, • коробочный перкуторный звук. Аускультация лёгких • сухие свистящие хрипы на выдохе (бронхоспазм),
• сухие свистящие хрипы на вдохе (стридор, например, за счёт инородного тела в верхних дыхательных путях),
• влажные хрипы в задненижних отделах грудной клетки («сердечный» характер одышки),
• ослабление или отсутствие дыхательных шумов (плевральный выпот, пневмоторакс). Обследование нижних конечностей Симптомы, позволяющие предположить тромбоз глубоких вен:
• увеличение окружности поражённой конечности по меньшей мере на 1 см по сравнению со здоровой,
• боль в икроножных мышцах при тыльном сгибании стопы (симптом Хоманса),
• при передне-заднем сдавлении икроножных мышц (симптом Мозеса).
В качестве инструментальных методов исследования применяют:
• рентгенографическое исследование грудной клетки,
• ЭКГ, • газы артериальной крови.
Нередко для верификации диагноза применяются специальные методы:
• легочные тесты (исследование ФВД),
• исследование газового состава крови во время нагрузки,
• бронхопровокационные тесты,
Перечень заболеваний, протекающим с симптомом удушья.
1. Удушье, обусловленное нарушением проходимости верхних дыхательных путей:
1.1 аллергический отек гортани;
1.2 заглоточный абсцесс;
1.3 дифтерийный круп;
1.4 крупозный стенозирующий ларингит;
1.5 ларингоспазм;
1.7 инороднее тело трахеи;
1.8 опухоли трахеи;
1.9 трахеобронхиальная дискинезия.
2. Удушье, обусловленное бронхиальной обструкцией
2.1 бронхиальная астма;
2.2 бронхолегочный аспергиллез;
2.3 карциноидные опухоли;
2.4 синдром Чарджа — Стросса;
2.5 доброкачественная аденома бронха;
2.7 сдавление крупных бронхов извне;
2.8 синдром Мендельсона;
2.9 отравление фосфорорганическими соединениями;
2.10 передозировка ?-адреноблокаторов.
3. Удушье при отеке легких
3.1 кардиогенный отек легких; 3.2 нефрогенный отек легких;
3.3 токсический отек легких.
4. Удушье при быстром уменьшении респираторной части легкого
4.1 пневмония;
4.2 спонтанный пневмоторакс;
4.3 экссудативный плеврит;
4.4 тромбоэмболия легочной артерии;
4.5 ОРДС (острый респираторный дистресс синдром).
5. Удушье при заболеваниях диафрагмы
5.1 фибрилляция диафрагмы; 5.2 синдром Эрба-Гольдфлама.
6. Удушье при нарушении нервной регуляции ритма дыхания
6.1 органические поражения центральной и периферической нервной системы;
6.2 гипервентиляционный синдром.
Алгоритм дифференциальной диагностики.
1. Удушье, обусловленное нарушением проходимости верхних дыхательных путей (на уровне гортани и трахеи), клинически характеризуется стридорозным дыханием с затруднением на вдохе.
При стенозе на уровне гортани стридор часто сочетается с афонией. Больной при вдохе откидывает голову назад. При вдохе слышен всегда резкий «скрипучий» звук.
При стенозе на уровне трахеи афонии обычно нет. Больной при вдохе поднимает плечи и опускает подбородок. «Скрипучий» звук на вдохе может отсутствовать.
1.1. Аллергический отек гортани (частный случай отека Квинке).
В анамнезе нередко выявляют различные аллергические заболевания и реакции.
Характерно быстрое (иногда за несколько минут) развитие удушья. Наблюдается стридор, охриплость голоса, лающий кашель, цианоз лица. Нередко параллельно развивается отек Квинке в области губ, щек, шеи. Возможно возникновение крапивницы.
Если присоединяется бронхоспастический синдром, то одышка становится смешанной, в легких появляются сухие свистящие хрипы. В общем анализе крови выявляется эозинофилия.
1.2. Заглоточный абсцесс развивается на фоне ангины, паратонзиллита. В предшествующие дни — клиника тяжелой ангины.
Характерны: высокая температура тела, боли в горле с иррадиацией в уши, глухой голос с носовым оттенком, стридорозное дыхание, которое постепенно переходит в удушье.
Определяется припухлость на шее в области перифаренгиального пространства. Увеличены и болезненны регионарные лимфоузлы. Необходима консультация оториноларинголога и экстренная ларингоскопия.
1.3. Дифтерия гортани обычно развивается при распространении пленок с миндалин и из носоглотки, изолированная дифтерия гортани встречается редко.
Клиника катаральной (дисфонической) стадии характеризуется грубым «лающим» кашлем и нарастающей осиплостью голоса. В стенотической стадии голос становится афоничным, кашель — беззвучным. Больной бледный, беспокойный, шумное (стридорозное) дыхание с удлиненным вдохом и втяжением уступчивых мест грудной клетки. В асфиксической стадии дыхание становится частым, поверхностным, затем аритмичным. Нарастает цианоз, пульс становится нитевидным, артериальное давление падает. Нарушается сознание, появляются судороги, может наступить смерть от асфиксии.
Помимо симптомов поражения гортани наблюдаются лихорадка, интоксикация. При осмотре зева могут выявляться отек и цианотичная гиперемия миндалин, небных дужек, язычка, грязно-серые налеты на слизистой. Подчелюстные лимфатические узлы увеличены и болезненны при пальпации.
Обязательным исследованием является бактериологическое исследование мазков из носа, зева, а также пленок из гортани.
1.4. Крупозный стенозирующий ларингит наблюдается при некоторых вирусных заболеваниях.
На фоне симптоматики острой респираторной вирусной инфекции возникают боли в верхней части грудины, осиплость голоса, стенотическое дыхание, переходящее в удушье. Отмечаются диффузный цианоз, психомоторное возбуждение больного.
1.5. Ларингоспазм — спазм мускулатуры гортани с закрытием голосовой щели и удушьем.
Может возникать при ларингите, вдыхании раздражающих веществ, случайном попадании пищи или воды в дыхательные пути, при раздражении возвратного нерва (опухолью, аневризмой). При истерии развитие ларингоспазма обычно связано с психотравмирующей ситуацией.
Характерны: инспираторное удушье, побледнение кожи, цианоз, судорожные движения конечностей.
1.6. Коклюш характеризуется приступами «конвульсивного», «удушливого» кашля, прерываемого так называемыми репризами — судорожными вдохами на фоне спазма голосовой щели, что сопровождается свистящим или скрипучим звуком. Во время приступа кашля лицо краснеет, затем синеет, вены шеи набухают, выступают слезы, голова вытягивается вперед, язык высовывается до предела изо рта, кончик его загнут кверху. Приступ заканчивается отхождением вязкой, стекловидной мокроты и нередко рвотой. При тяжелом течении коклюша возникают носовые кровотечения, кровоизлияния в склеру, апноэ, судороги, непроизвольное мочеиспускание и дефекация.
В крови выявляется лейкоцитоз, лимфоцитоз.
Для обнаружения возбудителя делают посевы на специальные среды с использованием мазков из зева.
1.7. Инороднее тело трахеи может вызвать внезапное тяжелое удушье, иногда со смертельным исходом.
Чаще в трахею попадают кусочки пищи, зубных протезов. Возможна закупорка трахеи бронхолитом при туберкулезе лимфатического узла с прорывом в трахею. Способствующими факторами являются быстрая еда, разговор во время еды, смех, алкогольное опьянение.
Внезапно развивается приступ резкого судорожного кашля, цианоз лица, слезо- и слюнотечение. Инспираторная одышка при реактивном воспалении слизистой трахеи переходит в удушье, возможна асфиксия.
1.8. Опухоли трахеи могут быть доброкачественными (папиллома, фиброма, аденома, невринома и др.) и злокачественными.
Чаще всего наблюдается аденоиднокистозный, реже ? эпидермоидный рак.
Клинические симптомы возникают при сужении просвета на 50 и более процентов. Характерны:
* инспираторная одышка, усиливающаяся при физической нагрузке,
* приступы инспираторного удушья, прекращающиеся после отхождения мокроты,
* сухой кашель, усиливающейся при перемене положения тела и при пальпации трахеи,
* кровохарканье,
* изменение тембра голоса.
От появления первых признаков до развития выраженного трахеального синдрома при доброкачественных опухолях проходит около 2 лет, при злокачественных — около года.
Проводится рентгенография трахеи, КТ, фибротрахеоскопия с биопсией.
1.9. Трахеобронхиальная дискинезия — экспираторный стеноз (коллапс) трахеи и бронхов; функциональное нарушение, характеризующееся пролабированием на выходе мембранозной стенки трахеи и бронхов с экспираторным сужением их просветов. Трахеобронхиальная дискинезия обычно манифестирует при форсированном дыхании и кашле, слабо проявляясь при спокойном дыхании.
В основе заболевания лежит нарушение эластичности и тонуса мембранозной части трахеи, которое может быть первичным (после острой респираторной вирусной инфекции, туберкулеза, если бактериальные и вирусные токсины вызвали повреждение эластических, мышечных, интрамуральных нервных волокон в стенках трахеи и крупных бронхов) и вторичным (у больных хроническими неспецифическими заболеваниями легких с бронхиальной обструкцией и эмфиземой легких).
В зависимости от выраженности экспираторного сужения трахеи и главных бронхов во время форсированного дыхания и кашля различают две степени дискинезии:
I степень — сужение на 2/3 просвета и более, без смыкания трахеобронхиальных стенок.
II степень — полный экспираторный коллапс трахеи и бронхов со смыканием их стенок при форсированном выдохе.
Обычно возраст больных старше 30 лет.
Характерным клиническим симптомом трахеобронхиальной дискинезии является своеобразный лающий битональный кашель с дребезжащим, трубным оттенком, нередко приступообразный, иногда сопровождаемый рвотой, головокружением.
Ведущим методом диагностики является бронхоскопия, при которой дискинезия проявляется увеличением подвижности и значительным пролабированием на выдохе мембранозной стенки трахеи и бронхов. При дискинезии II степени обнаруживается смыкание задней мембранозной и переднебоковых трахеобронхиальных стенок. Вследствие расширения мембранозной части просветы трахеи и бронхов обычно имеют уплощенную форму или форму полулуния.
2. Удушье, обусловленное бронхиальной обструкцией наиболее часто встречается при бронхиальной астме и характеризуется выраженной экспираторной одышкой.
2.1. Бронхиальная астма — это хроническое воспалительное заболевание дыхательных путей, в котором принимают участие многие клетки и клеточные элементы. Хроническое воспаление обусловливает развитие бронхиальной гиперреактивности, которая приводит к повторяющимся эпизодам свистящих хрипов, одышки, чувства заложенности в груди и кашля, особенно по ночам или ранним утром. Эти эпизоды обычно связаны с распространенной, но изменяющейся по своей выраженности обструкцией дыхательных путей в легких, которая часто бывает обратимой либо спонтанно, либо под действием лечения (GINA, 2007).
Механизмы бронхиальной обструкции при бронхиальной астме:
* бронхоспазм (является главным механизмом сужения дыхательных путей, практически полностью обратимо под действием бронхолитиков);
* отек слизистой оболочки бронхов (может играть особенно важную роль при обострениях);
* гиперсекреция слизи (может приводить к окклюзии просвета бронхов — «слизистые пробки»).
* ремоделирование стенки бронхов (может иметь большое значение при тяжелой бронхиальной астме, не обратимо под действием существующих препаратов);
Классификация бронхиальной астмы
По этиопатогенезу (МКБ Х, 1992)
1. Преимущественно аллергическая
1.1. Аллергический бронхит
1.2. Аллергический ринит с астмой
1.3. Атопическая астма
1.4. Экзогенная аллергическая астма
1.5. Сенная лихорадка с астмой
2. Неаллергическая астма
2.1. Идиосинкразическая (аспириновая) астма
2.2. Эндогенная неаллергическая астма
3. Смешанная астма
4. Неуточненная астма
4.1. Астматический бронхит
4.2. Поздно возникшая астма
5. Астматический статус
По фазе течения: обострение и ремиссия.
По клиническим признакам перед началом лечения*.
Степень тяжести Критерии Интермиттирующая бронхиальная астма ?
? ? Симптомы реже 1 раза в неделю
Короткие обострения
Ночные симптомы не чаще 2 раз в месяц ? ОФВ1 или ПСВ?80% от должных значений ? Вариабельность показателей ПСВ или ОФВ1 ? 20% Легкая персистирующая бронхи- ? Симптомы чаще 1 раза в неделю, но реже 1 раза в день альная астма ? Обострения могут влиять на физическую активность и сон ? Ночные симптомы чаще 2 раз в месяц ? ОФВ1 или ПСВ ? 80% от должных значений ? Вариабельность показателей ПСВ или ОФВ1 20-30% Персистирующая бронхиальная астма средней тяжести ?
Обострения могут влиять на физическую активность и сон
Ночные симптомы чаще 1 раза в неделю ? ОФВ1 или ПСВ от 60 до 80% от должных значений ? Вариабельность показателей ПСВ или ОФВ1 ? 30% Тяжелая персистирующая бронхиальная астма ?
Частые ночные симптомы
Ограничесние физической активности ? ОФВ1 или ПСВ ? 60% от должных значений ? Вариабельность показателей ПСВ или ОФВ1 ? 30% * Классификация тяжести бронхиальной астмы осуществляется по наихудшему признаку.
Диагностика бронхиальной астмы.
Жалобы: * эпизоды одышки, удушья, свистящего дыхания, заложенности в грудной клетке;
* кашель, сухой или с отделением вязкой, иногда стекловидной мокроты;
* появление симптомов после эпизодов контакта с аллергеном, неспецифическими ирритантами (дымом, газами, резкими запахами), после физической нагрузки;
* сезонная вариабельность симптомов;
* наличие в семейном анамнезе случаев бронхиальной астмы или атопии;
* сочетание симптомов бронхиальной астмы с ринитом;
* ухудшение в ночные часы;
* уменьшение в ответ на соответствующую терапию бронхиальной астмы.
Если у врача возникает подозрение на наличие у пациента бронхиальной астмы, он должен задать ряд обязательных вопросов (GINA, 2007):
1) Бывают ли у пациента эпизоды свистящих хрипов, в том числе повторяющиеся?
2) Беспокоит ли пациента кашель по ночам?
3) Отмечаются ли у пациента свистящие хрипы или кашель после физической нагрузки?
4) Бывают ли у пациента эпизоды свистящих хрипов, заложенности в грудной клетке или кашля после контакта с аэроаллергенами или полютантами?
5) Отмечает ли пациент, что простуда у него «спускается в грудную клетку» или продолжается более 10 дней?
6) Уменьшается ли выраженность симптомов после применения соответствующих противоастматических препаратов?
Физикальные данные:
В связи с вариабельностью обструкции характерные симптомы болезни не обязательно выявляются при физикальном обследовании вне обострения бронхиальной астмы. При обострении заболевания у пациента наблюдаются следующие симптомы: ? экспираторная одышка,
* раздутие крыльев носа при вдохе,
* постоянный или прерывающийся кашель,
* включение вспомогательной дыхательной мускулатуры, ? сухие хрипы при аускультации.
Несмотря на то, что сухие хрипы являются наиболее характерными симптомами БА, они могут отсутствовать даже при выраженном обострении. Тем не менее, в этом состоянии у пациентов имеются другие признаки, отражающие тяжесть обострения: цианоз, сонливость, затруднения при разговоре, тахикардия, эмфизема.
Помимо клинических данных, важную роль в диагностике бронхиальной астмы играет исследование функции легких (ФЖЕЛ, ОФВ1 и ПСВ) и в особенности подтверждение обратимости и вариабельности их нарушений.
Обратимость — быстрое увеличение ОФВ1 (на 12 и > %) или ПСВ (на 15 и > %), выявляемое через 15-20 минут после ингаляции бронхолитика быстрого действия — например, 200-400 мкг сальбутамола или более медленное улучшение функции легких, развивающееся через несколько дней или недель после назначения адекватной поддерживающей терапии, например ингаляционными глюкокортикостероидами.
Вариабельность — колебания выраженности симптомов и показателей функции легких в течение определенного промежутка времени. Чаще всего исследуют суточные колебания ПСВ, которые у пациентов с бронхиальной астмой обычно более 20%.
Каждому больному бронхиальной астмой показана ежедневная пикфлоуметрия. Мониторирование астмы с помощью пикфлоуметра дает следующие возможности:
* определить обратимость и вариабельность бронхиальной обструкции;
* оценить степень тяжести заболевания на этапе первичной диагностики;
* идентифицировать профессиональную астму; ? прогнозировать обострения астмы; ? оценить эффективность лечения.
У пациентов с жалобами на характерные симптомы бронхиальной астмы, но с нормальными показателями функции легких возможно использование провокационных тестов с ингаляцией метахолина или гистамина. Результаты теста обычно приводятся в виде провокационной концентрации (или дозы) агента, вызывающего заданное снижение ОФВ1 (как правило, на 20%).
В общем анализе крови может выявляться эозинофилия.
В анализе мокроты — эозинофилы, кристаллы Шарко-Лейдена, спирали Куршмана.
В обязательный комплекс дополнительных методов исследования включены иммунологические методы, позволяющие выявить повышение общего и специфических IgE. А также консультация аллерголога с проведением (в период ремиссии) кожных аллергических проб.
Таким образом, диагностика бронхиальной астмы строится на основании анализа симптомов и анамнеза, а также исследовании функции внешнего дыхания и данных аллергологического обследования. Наиболее важными спирометрическими функциональными тестами являются выявление ответа на ингаляции ?2-агонистов, изменение вариабельности бронхиальной проходимости с помощью мониторирования ПСВ. Важным критерием в диагностике является определение аллергологического статуса, хотя отсутствие признаков атопии при наличии остальных симптомов не исключает диагноз астмы.
Лечение бронхиальной астмы
Базисная терапия БА основана на ступенчатом подходе и предусматривает обязательное проведение комплекса элиминационных мероприятий и аллергенспецифической иммунотерапии (АСИТ).
Элиминационные мероприятия и АСИТ.
Элиминационные мероприятия (исключение контакта с установленным или предполагаемым аллергеном) предполагают соблюдение гипоаллергенного быта, диеты, а также исключение использования лекарственных препаратов, наиболее часто ухудшающих самочувствие больных БА.
АСИТ используется при лечении пациентов с доказанной ролью IgЕ в механизме заболевания при невозможности избежать контакта с аллергеном. Данные метод заключается во введении в организм пациента водно-солевого экстракта того аллергена, к которому у больного выявлена повышенная чувствительность. Аллерген может быть использован в виде подкожных введений или применен местно (ингаляционно, перорально, интраназально, сублингвально). При этом формируется снижение тканевой чувствительности к аллергену, снижение неспецифической тканевой гиперреактивности, клинически эффективная АСИТ сопровождается угнетением признаков аллергического воспаления. АСИТ проводится аллергологом-иммунологом в условиях аллергологического кабинета или стационара.
Медикаментозная терапия
Фармакотерапия Ступени 1 2 3 4 5 Средства для купирования симптомов ?2-агонист короткого действия по потребности (но не больше 6-8 доз в сутки) Препараты базисной (контролирующей) терапии* Нет Выберите один Выберите один Добавьте один или более Добавьте один или оба Низкие дозы
ИГКС Низкие дозы
ИГКС + ДДБА** Средние или высокие дозы ИГКС +
ДДБА ** Минимальная возможная доза перорального ГКС Антилейкотриеновый препарат Средние или
высокие дозы ИГКС Антилейкотриеновый препарат Антитела к IgE Низкие дозы ИГКС + антилейкотриеновый препарат Теофиллин замедленного высвобождения Низкие дозы ИГКС + теофиллин замедленного высвобождения *Предпочтительное применение препаратов показано в светло-серых ячейках
** ДДБА — ?2-агонист длительного действия
Эквивалентные дозы ИГКС
Препарат Низкая суточная доза, мкг Средняя суточная доза, мкг Высокая суточная доза, мкг Беклометазона дипропионат 200 ? 500 >500 ? 1000 >1000 ? 2000 Будесонид* 200 ? 400 >400 ? 800 >800 ? 1600 Флутиказон 100 ? 250 >250 ? 500 >500 ? 1000 Циклесонид* 80 ? 160 >160 ? 320 >320 ? 1280 Мометазон* 200 ? 400 >400 ? 800 >800 ? 1200 *Препарат можно применять 1 раз в сутки при нетяжелой бронхиальной астме.
После назначения того или иного объема терапии первичная оценка эффективности проводится через 2 недели. При отсутствии эффекта, прежде всего необходимо убедиться в правильности использования ингаляторов пациентом.
Если удается добиться положительной динамики в течении заболевания, то через 1-2 месяца необходимо оценить уровень контроля бронхиальной астмы.
Характеристики Контролируемая бронхиальная астма (всё нижеперечисленное) Частично контролируемая бронхиальная
астма (любое проявление
в течение любой неде-
ли) Неконтролируемая бронхиальная астма Дневные симптомы Отсутствуют (или ?2 эпизодов в неделю) >2 эпизодов в неделю Наличие трех или более признаков частично контролируемой бронхиальной астмы* Ограничения активности Отсутствуют Любые Ночные симптомы/ пробуждения Отсутствуют Любые Потребность в ?2агонистах короткого действия Отсутствуют (или ?2 эпизодов в неделю) >2 эпизодов в неделю Функция легких
(ПСВ или ОФВ1) Нормальная 95%
6) 90-95%
2) постепенное начало инспираторной одышки;
3) длительность заболевания > 3 мес;
4) двусторонние крепитирующие хрипы в нижних отделах легких.
Наличие четырех «больших» диагностических признаков и трех «малых» позволяет установить диагноз ИФА без гистологического подтверждения. Дополнительным признаком ИФА является ухудшение состояния на фоне антибактериальной терапии и положительный клинический эффект при лечении глюкокортикостероидами.
Основные направления терапии при ИФА:
1. Базисная терапия (глюкокортикостероиды, иммуносупрессанты — азатиоприн, антифибротические препараты — пеницилламин).
2. Эфферентная терапия (плазмаферез).
3. Длительная кислородотерапия.
4. Трансплантация легких.
Диспансерное наблюдение больных ИФА должно осуществляться в специализированных пульмонологических учреждениях.
1.2. Экзогенный аллергический альвеолит (ЭАА) — патологический процесс, представляющий собой аллергическую реакцию преимущественно респираторного отдела легких на различные аллергены.
* бактериальные (актиномицеты, Micropolispora faeni и др.);
* грибковые (Aspergillus fumigatus, Penicillium casei, Cryptostroma corticale, плесневые грибы);
* белковые антигены животного происхождения (экскременты кур, голубей, попугаев, свиней, клещи);
* антигены растительного происхождения (опилки дуба, кедра, коры льна, красного дерева, солома, экстракты кофейных зерен, хлопок, лен);
* медикаментозные антигены (противомикробные, противовоспалительные, противопаразитарные препараты, ферменты, лекарства белкового происхождения, контрастные вещества)
Производства, работа на которых может представлять риск развития ЭАА: сельское хозяйство; пищевая промышленность; текстильная и швейная промышленность; химическая и фармацевтическая промышленность; деревообрабатывающая промышленность.
Классификация ЭАА:
1) острая форма; 2) подострая форма; 3) хроническая форма.
При каждой форме ЭАА преобладают различные морфологические процессы (при острой форме — интерстициальный отек; при подострой — инфильтрация альвеол и межальвеолярных перегородок лимфоцитами, эпителиодными и плазматическими клетками; при хроническом течении — интерстициальный фиброз).
При острой форме ЭАА, которая встречается наиболее часто, симптомы болезни возникают через 4-6 часов после экспозиции аллергена. Характерными признаками являются: лихорадка с ознобом, одышка, сухой кашель, тошнота, миалгии, боль в груди, артралгии. У части больных могут возникать приступы затрудненного дыхания и явления вазомоторного ринита. При аускультации определяются влажные мелко- и среднепузырчатые хрипы над всей поверхностью легких, развивается тахикардия. При наличии бронхоспазма выслушиваются сухие свистящие хрипы. Характерным является синдром элиминации с нормализацией клинических, функциональных и рентгенологических изменений после прекращения воздействия аллергена и рецидив болезни после возобновления контакта с ним. При продолжающемся контакте с причинным агентом заболевание прогрессирует.
Подострая форма ЭАА характеризуется постепенным развитием симптомов, что затрудняет выявление связи между клиническими проявлениями болезни и воздействием агента. Характерны: одышка, кашель с небольшим количеством мокроты, субфебрильная температура, снижение аппетита, похудание.
Повторные контакты вызывают обострение патологического процесса.
Развитие хронического ЭАА обусловлено длительным (нередко многолетним) контактом с небольшими дозами аллергена. При этом, как правило, отсутствуют острые эпизоды болезни, характерны прогрессирующая одышка, цианоз, похудание. Ведущим является синдром хронического бронхита с первично хроническим течением, нарастанием обструкции.
Лабораторная и инструментальная диагностика.
Общий анализ крови: лейкоцитоз, сдвиг лейкоцитарной формулы, увеличение СОЭ (острая форма ЭАА); эозинофилия (только при ЭАА, вызванных аспергиллами).
Биохиимческий анализ крови: гипергаммаглобулинемия (у больных с хронической формой ЭАА).
Иммунологическое исследование: специфические преципитирующие антитела класса IgG (уточняют связь заболевания с профессией).
Возможно также использование провокационного ингаляционного теста: после вдыхания аэрозоля с предположительным антигеном оцениваются температура, частота дыхания, аускультативная картина, величина ЖЕЛ.
Рентгенологическая картина при ЭАА: двусторонняя инфильтрация с нечеткими контурами в нижних и средних отделах легких или мелкоочаговая диссеминация, при переходе в хроническую форму формируется «сотовое легкое». ФВД: рестриктивный тип нарушений вентиляционной функции, сочетающийся с необратимым или частично обратимым нарушением бронхиальной проходимости.
Анализ БАЛ: увеличение общего числа клеток и процентного содержания лимфоцитов (от 20 до 90% общего состава), повышенные уровни IgA, IgG, IgM. Для гистологической верификации ЭАА проводят биопсию легких.
Диагностические критерии ЭАА:
* начало или ухудшение заболевания через несколько часов после контакта с аллергеном;
* подтверждение контакта с аллергеном;
* характерные изменения на рентгенограммах и КТ легких;
* лимфоцитоз БАЛ;
* характерные морфологические изменения;
* появление клинических, лабораторных и функциональных признаков после контакта с аллергеном.
* крепитация;
Основные принципы лечения:
1) прекращение контакта с аллергеном;
2) назначение ингаляционных или системных глюкокортикостериодов; 3) эфферентная терапия (плазмаферез); 4) бронхолитическая терапия.
При ЭАА абсолютно противопоказано назначение антибактериальных препаратов. Если заболевание связано с профессией, то больные трудоспособного возраста нуждаются в рациональном трудоустройстве. При снижении квалификации они подлежат направлению на МСЭК для решения вопросов экспертизы стойкой нетрудоспособности.
1.3 Экзогенный токсический альвеолит (ЭТА) — патологический процесс, возникающий вследствие воздействия на легочную паренхиму веществ, обладающих цитотоксическими свойствами.
К веществам, обладающим пневмотропным токсическим действием, относят следующие группы:
1) лекарственные препараты
• цитостатики (метотрексат, азатиоприн, циклофосфамид, флударабин);
• антибиотики (блеомицин, митомицин, фуразолидон, цефалоспорин), сульфаниламиды;
• противосудорожные препараты (карбамазепин, дифенил);
• антиаритмики (амиодарон);
• мочегонные (гидрохлортиазид); • противодиабетические (хлорпропамид); • цитокины, моноклональные антитела.
2) токсические вещества производственной сферы:
• раздражающие газы (сероводород, хлор, аммиак);
• металлы (кадмий, ртуть, никель, кобальт, марганец, бериллий, цирконий);
• органические растворители (бензин, нефть, керосин, бензол, толуол, ацетон, этиленгликоль);
• гербициды, инсектициды; • пластмассы (полиуретан).
Классификация ЭТА по клиническому течению:
1) Острое течение.
2) Подострое течение.
3) Хроническое течение.
Острая форма ЭТА может протекать по следующим типам:
* ингаляционная лихорадка (металлическая дымная лихорадка, полимерная дымная лихорадка, токсический синдром от органической пыли);
* токсический отек легких; ? респираторный дистресс-синдром; ? альвеолит.
ЭТА возникает при первом контакте с высокими концентрациями токсических веществ. При этом поражаются сразу несколько лиц, находившихся в зоне повышенного содержания вредных факторов. Клиническая картина ЭТА зависит от агрессивности токсического агента, его концентрации, времени экспозиции и индивидуальной реакции организма.
Для ЭТА характерны:
* симптомы ларингофарингита (боль в горле, осиплость голоса, свистящее стридорозное дыхание),
* токсический бронхит (непродуктивный кашель, одышка, боли и чувство тяжести в грудной клетке),
* ринит (слезотечение, чихание, носовое кровотечение),
* лихорадка, артралгии, аллергическая сыпь на коже, похудание,
* аускультативно выслушиваются сухие и влажные мелкопузырчатые хрипы, крепитация.
В тяжелых случаях развиваются плевральные выпоты, респираторный дистресс-синдром, токсический отек легких.
При бериллиозе могут наблюдаться внелегочные поражения: лимфаденопатия, поражение кожи и слюнных желез, печени.
У пациентов с «кобальтовым легким» отмечается прогрессирование пневмофиброза и развитие «сотового легкого».
Воздействие органических растворителей отличается преобладанием токсических изменений центральной нервной системы (токсическая энцефалопатия), развитием ирритационного дерматита.
Рентгенологические изменения: равномерное снижение прозрачности легочной ткани, мелко- и крупноячеистая деформация рисунка, двусторонние мелкоочаговые тени преимущественно в нижних отделах легких, уменьшение объема нижних долей.
Исследование ФВД выявляет рестриктивный тип нарушений вентиляционной функции. При развитии облитерирующего бронхиолита возможно развитие обструктивного синдрома.
Специфическая диагностика бериллиоза включает кожную пробу Куртиса (в случае положительной пробы накожная аппликация 0,5-1% раствора хлорида бериллия вызывает появление эритемы).
В сложных случаях диагностики показано проведение биопсии.
Диагностические критерии ЭТА.
* начало или ухудшение через несколько часов после контакта с токсическими веществами;
* подтверждение контакта с токсическими веществами санитарногигиеническими исследованиями;
* характерные изменения на рентгенограммах и КТ;
* лимфоцитоз и/или нейтрофилез БАЛ;
* характерные морфологические изменения;
* появление клинических признаков после повторных контактов с этиологическим фактором;
* высокое содержание токсических веществ в биологических средах;
* положительные пробы на гиперчувствительность к металлам (кожные, серологические);
* повышенный уровень сывороточного гликопротеина KL-6.
* рестриктивные тип нарушения ФВД;
* легочная гипертензия;
* артериальная гипоксемия в покое и при нагрузке.
Патогенетическая терапия при ЭТА включает глюкокортикоидные и антиоксидантные препараты, экстракорпоральные методы лечения (плазмаферез, гемосорбция).
2.1. Саркоидоз — системное воспалительное заболевание неизвестной природы, характеризующимся образованием в различных органах и тканях неказеифицирующихся саркоидных гранулем.
Саркоидозом чаще болеют женщины.
Морфологическим проявлением саркоидоза является неказеифицирующаяся эпителиоидноклеточная гранулема. Это компактное скопление мононуклеарных фагоцитов — макрофагов и эпителиоидных клеток. Гранулемы при саркоидозе обычно более мелкого размера, чем при туберкулезе, и для них не характерно слияние.
Саркоидоз может протекать бессимптомно (13%) и выявляться при периодических флюорографических осмотрах. Заболевание может иметь острое (2025%), первично-хроническое (65-70%) и рецидивирующее течение.
Варианты острого начала саркоидоза: Синдром Лефгрена — лихорадка, полиартралгия, узловатая эритема, двусторонее увеличение лимфатических узлов корней легких рентгенологически. Синдром Хеерфордта-Вальденстрема: лихорадка, увеит (чаще передний), паротит, парез лицевого нерва (паралич Белла), рентгенологически — двусторонее увеличение внутригрудных лимфатических узлов.
В клинике первично-хронического саркоидоза симптомы появляются при нарушении функции пораженного органа вследствие структурных изменений. На начальных этапах развития заболевания она скудная. Легочные симптомы:
* одышка; ? сухой кашель; ? торакалгия.
Наиболее частые внелегочные симптомы:
* слабость (утренняя усталось, интермиттирующая усталость, вечерняя слабость, хроническая усталость);
* суставной синдром (боль и отек может быть в голеностопных суставах, суставах кистей рук и стоп, реже в позвоночнике);
* снижение остроты зрения и/или затуманивание зрения (признаки саркоидного увеита);
* кардиалгия, сердцебиения или перебои в работе сердца, признаки сердечной недостаточности;
* неврологические нарушения (патогномоничным для саркоидоза считается паралич Белла — односторонний паралич лицевого нерва, который принято считать признаком благоприятного прогноза);
* узловатая эритема (Erythema nodosum) (пальпируемые возвышающиеся над кожей болезненные синевато-багровые узловатые двусторонние высыпания на коже голеней, размером от одного до нескольких сантиметров в диаметре, плотные, полушаровидной формы, при рассасывании оставляют временную пигментацию);
* лимфаденопатия безболезненные, подвижные увеличенные периферические лимфатические узлы (чаще шейные и паховые).
Изменения лабораторных показателей при саркоидозе неспецифичны. Диагностическое значение имеет повышение активности АПФ в крови более 150% от нормы (для лиц старше 20 лет нормальными считаются значения от 18 до 67 единиц в 1 литре (u/l).
Гиперкальциемия и гиперкальцийурия (в норме в сыворотке крови общий Ca 2,0-2,5 ммоль/л, ионизированный Ca 1,05-1,30 ммоль/л; Ca в моче — 2,5-7,5 ммоль/сут).
Проба Манту с 2 ТЕ ППД-Л при активном саркоидозе дает отрицательный результат в 80-85% случаев и имеет высокую чувствительность для диагностики саркоидоза.
На КТ и рентгенограмме для саркоидоза ВГЛУ характерно увеличение лимфатических узлов всех групп центрального средостения и корней легких, перибронхиальных и трахеобронхиальных, полицикличностью их контуров. Лимфатические узлы имеют шаровидную или овоидную форму, однородную структуру, гладкие четкие контуры, без перифокальной инфильтрации и склероза. При значительном увеличении лимфоузлов, обусловливающих внешнюю компрессию бронхов, в легких могут возникать гиповентиляция соответствующего сегмента или доли, рецидивирующие воспаления и ателектаз. Наиболее характерным признаком саркоидоза легких является полиморфная мелкоочаговая диссеминация, очаги располагаются вдоль бронхососудистых пучков, междолевых щелей, костальной плевры, в междольковых перегородках, вызывая неравномерное («четкообразное») утолщение интерстициальных структур легких. Хроническое рецидивирующее течение саркоидоза характеризуется появлением полиморфизма очаговых изменений, в виде увеличения размеров очагов, деформации их контуров и слияния в мелкие зоны консолидации. В таких инфильтратах возможно формирование полостей. Четвертая стадия саркоидоза характеризуется формированием обширных участков пневмосклероза в виде зон уплотнения легочной ткани в верхних долях (пневмоцирроз), дистрофическими изменения с развитием буллезной эмфиземы в кортикальных и наддиафрагмальных отделах легких.
По рентгенологическим данным саркоидоз органов грудной клетки разделяют на 5 стадий:
Стадия Рентгенологическая картина Частота Стадия 0 Нет изменений на рентгенограмме органов грудной клетки 5% Стадия I Увеличение внутригрудных лимфатических узлов (ВГЛУ); изменений в легочной ткани нет 50% Стадия II Увеличение внутригрудных лимфатических узлов и изменения легочной ткани 30% Стадия III Изменения легочной ткани без увеличения внутригрудных лимфатических узлов 15% Стадия IV Необратимый фиброз легких 20% Характерно клиническое несоответствие между относительно удовлетворительным состоянием больного и распространенностью патологического процесса в лимфоузлах и легочной ткани на рентгенограммах.
При УЗИ паренхиматозных органов обычно выявляют множественные гипоэхогенные узлы в печени, селезенке, а также увеличение лимфатических узлов в гепатодуоденальной связке, в воротах печени и селезенки, в перипанкреатической клетчатке.
При спирометрии у большинства больных с прогрессирующим саркоидозом развиваются рестриктивные нарушения, однако эндобронхиально расположенные гранулемы могут приводить к развитию необратимой бронхиальной обструкции.
Гистологическое исследование является верифицирующим методом диагностики. Эндоскопическое ультразвуковое исследование с выполнением чрезпищеводной тонкоигольной аспирационной биопсии лимфатических узлов средостения становится наиболее перспективным методом дифференциальной диагностики медиастинальной лимфаденопатии.
Внелегочные проявления саркоидоза:
* саркоидоз кожи (узлы, бляшки, макулопапулезные изменения, ознобленная волчанка, рубцовый саркоидоз).
* Поражение глаз (передний и задний увеит).
* Саркоидоз периферических лимфатических узлов (задние и передние шейные лимфатические узлы, надключичные, локтевые, подмышечные и паховые).
* Спленомегалия, гиперспленизм.
* Саркоидоз костного мозга.
* Поражение почек (мочевой синдром, нефротический синдром).
* Поражение суставов (голеностопных, коленных и локтевых).
* Саркоидоз костей (бессимптомный кистоидный остеит малых костей рук и ног; кистоподобные образования нижней челюсти; деструктивные изменения позвонков). На рентгенограммах и КТ кистозные или литические изменения. На МРТ инфильтрация мелких и крупных костей, признаки остеонекроза.
* Саркоидоз мышц (гранулематозный миозит и миопатия). На МРТ инфильтрация мягких тканей, объемные образования различной локализации, миопатия и узловые образования в мышцах.
* Саркоидоз ЛОР-органов (носа, гортани, миндалин, уха, ротовой полости).
* Саркоидоз сердца: различают фульминантные (внезапная сердечная смерть, инфарктоподобный вариант, кардиогенный шок), быстропрогрессирующие (с нарастанием хронической сердечной недостаточности в течение 1-2 лет) и медленно прогрессирующие (хронические, с рецидивами и улучшениями) варианты кардиосаркоидоза. На Эхо-КГ обнаруживаются единичные очаги в миокарде, чаще в межжелудочковой перегородке размером 3-5 мм.
* Нейросаркоидоз (поражение черепных нервов, поражение оболочек головного мозга, нарушения функции гипоталамуса, поражения ткани головного мозга, ткани спинного мозга, судорожный синдром, периферическая нейропатия, миопатия). На МРТ головного мозга выявляется гидроцефалия, одиночная или множественные гранулемы. Возможны тромбозы сосудов с микроинсультами.
* Саркоидоз желудочно-кишечного тракта (гранулематозный гастрит, паротит).
В настоящее время используются следующие подходы к лечению саркоидоза. Поскольку частота спонтанных ремиссий высока, у больных с бессимптомным течением, с первой стадией саркоидоза и стабильном состоянием лечение не показано. У больных с прогрессирующим течением болезни по данным рентгенологического и функционального исследования дыхания, при выраженных симптомах или внелегочных проявлениях препаратами первой линии являются оральные кортикостероиды. Часто применяемым экстракорпоральным методом удаления циркулирующих иммунных комплексов является плазмаферез. При терминальных стадиях саркоидоза следует иметь в виду пересадку легких.
В своем течении саркоидоз может иметь следующие варианты течения: спонтанная регрессия; регрессия на фоне лечения; стабилизация состояния (спонтанная или после терапии); прогрессирование; волнообразное течение; рецидив.
Саркоидная реакция — состояние, гистологически тождественное саркоидозу, но более скудно проявляющееся и ограниченное областью пораженного органа или регионарными лимфатическими узлами. По крайней мере, 54 различных заболевания могут вызывать саркоидную реакцию: пневмокониозы, рак желудка, щитовидной железы, поджелудочной железы, кожи, лимфогранулематоз и др.
2.2 Гистиоцитоз Х легких (ГХЛ) (легочный лангергансоклеточный гистиоцитоз) — заболевание ретикулогистиоцитарной системы неизвестной этиологии, характеризующееся первичной пролиферацией атипичных гистиоцитов (клеток Х) и образованием в легких и других тканях гистиоцитарных гранулем (инфильтратов).
Этиология неизвестна. Все описанные случаи ГХЛ спорадические. Встречается только среди представителей белой расы. Абсолютное большинство заболевших ГХЛ являются курильщиками (более 90%). Клональный характер пролиферации клеток Лангерганса в очагах поражения дал основание предполагать опухолевую природу заболевания, однако возможность спонтанных ремиссий при ГХЛ делают это предположение маловероятным.
Гранулемы, формирующиеся при ГХЛ, содержат преимущественно атипичные гистиоциты — крупные овоидные клетки с эозинофильной цитоплазмой и ядром неправильной формы; а также эозинофилы, плазматические клетки. Заболевание относится к системным, гранулемы могут обнаруживаться во всех органах и тканях, наиболее частая локализация — легкие и кости.
Клинические проявления ГХЛ варьируют от минимальных со спонтанным излечением до генерализованных быстро прогрессирующих, приводящих к полиорганной недостаточности. В большинстве случаев у взрослых болезнь протекает бессимптомно (первично хроническое течение). Первым проявлением ГХЛ может быть спонтанный пневмоторакс (у 60% больных), медленно прогрессирующая одышка, непостоянный сухой кашель. Для хронической формы ГХЛ характерна триада признаков: деструктивный остеолизис (поражение ребер, нижней челюсти, голеней, позвонков, костей свода черепа), несахарный диабет и экзофтальм, связанный с гистиоцитарной инфильтрацией орбиты. Наличие лихорадки, анемии, гепатоспленомегалии является предиктором неблагоприятного прогноза. Аускультация выявляет ослабленное дыхание, сухие хрипы, крепитацию.
Лабораторные изменения неспецифичны. Злокачественное течение сопровождается повышением активности АПФ в сыворотке крови. Важным в диагностике является обнаружение клеток Лангерганса и лимфоцитоз в БАЛ. На рентгенограмме для ГХЛ характерно наличие двусторонней мелкоочаговой диссеминации на фоне усиленного легочного рисунка, рецидивирующие пневмотораксы, раннее формирование тонкостенных кистозно-буллезных образований и «сотового легкого». На ранних стадиях ГХЛ при ФВД регистрируется рестриктивный синдром, но по мере прогрессирования болезни присоединятся обструктивные нарушения. Выявление гранулем при гистологическом исследовании позволяет верифицировать диагноз.
Патогенетически обоснованным направлением терапии является назначение глюкокортикостероидов, цитостатиков. Рецидивирующий спонтанный пневмоторакс может быть показанием для торакотомии.
2.3 Диссеминированный туберкулез (ДТ) характеризуется появлением в легких, а также в других органах множественных очагов специфического воспаления. Выделяют 3 варианта диссеминированного туберкулеза в зависимости от распространенности процесса:
* генерализованный,
* с преимущественным поражением легких (до 90% всех случаев), ? с преимущественным поражением других органов.
Основным источником, из которого МБТ распространяются по организму, являются остаточные посттуберкулезные изменения первичного периода, преимущественно во внутригрудных лимфатических узлах. Рассеивание может происходить гематогенным, лимфогенным, лимфогематогенным путями. По течению выделяют острый, подострый и хронический варианты диссеминированого туберкулеза легких.
Острый диссеминированный туберкулез в современной клинической классификации туберкулеза, а также в МКБ-10, выделен в самостоятельную клиническую форму — милиарный туберкулез. Это тяжелая остропрогрессирующая форма туберкулеза, при отсутствии своевременной диагностики и специфического лечения которой наступает летальный исход (дыхательная недостаточность, инфекционно-токсический шок, поражение жизненно важных органов). В патогенезе милиарного туберкулеза имеют значение наличие свежего или реактивация старого туберкулезного очага, значительное снижение защитных сил организма вплоть до ареактивности (ВИЧ-инфекция IVВ-V стадиии при уровне СД4 менее 200 клеток/мкл; лечение ГКС, ингибиторами ФНО-альфа и другими иммуносупрессорами, психические и физические травмы, беременность, ранний послеродовый период и др.), общая и местная гиперсенсибилизация организма, способствующая повышению проницаемости сосудистой стенки и гемато-энцефалического барьера, вследствие авитаминоза, массивной экзогенной суперинфекции, гиперинсоляции и т.д. При наличии подобных условий микобактерии туберкулеза (МБТ) из очага поступают в кровь, возникает массивная микобактериемия и полиорганное рассеивание инфекции (легкие, печень, почки, селезенка, лимфатические узлы, мозговые оболочки и др.).
Патоморфологически милиарный туберкулез характеризуется почти одномоментным появлением в интерстиции легких по ходу капилляров множества мономорфных продуктивных очагов 1-2 мм в диаметре с относительно четкими очертаниями, не склонных к слиянию и деструкции. При своевременном и адекватном лечении очаги могут полностью подвергнуться обратному развитию (рассасыванию).
Клинические формы:
— острейший туберкулезный сепсис (тифобациллез Ландузи); — латентный милиарный туберкулез.
Тифоидный вариант обычно имеет острое начало и сопровождается выраженными симптомами интоксикации: фебрильная лихорадка любого типа (прогностически неблагоприятна волнообразная и инвертированная), диспепсические расстройства, резкая слабость, отсутствие аппетита, поты, редко ознобы. Пациенты могут поступать в инфекционные отделения с диагнозами: «сепсис», «лихорадка неясного генеза» и др. Легочный вариант развивается более постепенно. На фоне умеренно выраженного синдрома интоксикации доминируют респираторные симптомы: сухой, реже со скудной слизистой мокротой кашель, одышка, боли в груди при дыхании. Такие больные направляются в терапевтические отделения с диагнозами: «пневмония, «бронхит», «плеврит». При милиарном туберкулезе высока вероятность поражения ЦНС, поэтому при появлении у больного головной боли, гиперестезий, вегетативно-сосудистых реакций (пятна Труссо и др.) необходимо проведение пункции даже при отсутствии менингеальных симптомов. Состояние средней тяжести или тяжелое. Кожа бледная, акроцианоз. При перкуссии легких определяется коробочный звук, при аускультации ослабленное или жесткое дыхание (вследствие развития компенсаторной эмфиземы). Могут выслушиваться крепитирующие или немногочисленные влажные мелкопузырчатые хрипы в межлопаточном пространстве. Со стороны других систем наиболее характерны тахикардия, увеличение печени, селезенки. При коинфекции «туберкулез и ВИЧ» часто увеличиваются периферические лимфатические узлы (шейные, подмышечные, паховые), поражаются также мезентериальные лимфатические узлы, брюшина, кишечник с клиническими проявлениями абдоминального синдрома. В клиническом анализе крови характерны анемия, лейкоцитоз/лейкопения, эозинопения, лимфопения, высокие цифры СОЭ. В клиническом анализе мочи — безболезненная гематурия. Туберкулиновая проба Манту с 2 ТЕ ППД-Л и Диаскинтест отрицательные (вторичная отрицательная анергия). Микобактерии туберкулеза в мокроте обычно не обнаруживаются. Рентгенологическое исследование: учитывая малые размеры очагов, наиболее информативна КТ. Первые 7-10 дней болезни можно отметить лишь диффузное снижение прозрачности легких, нечеткость (смазанность) легочного рисунка, который в дальнейшем становится сетчатым, мелкопетлистым (отек и уплотнение межацинозных, междольковых перегородок). И только на 2-3-4 неделях болезни могут визуализироваться на всем протяжении легких с обеих сторон множественные однотипные очаговые тени 1-2 мм в диаметре, малой или средней интенсивности без склонности к слиянию и распаду. У пациентов с ВИЧ-инфекцией характерно увеличение внутригрудных лимфатических узлов.
Острейший туберкулезный сепсис (тифобациллез Ландузи). Данный вариант милиарного туберкулеза развивается на фоне вторичного иммунодефицита и патоморфологически характеризуется образованием в органах множества мелких очагов специфического некроза (казеоза), иногда без клеточных элементов (без эпителиоидных клеток, клеток Лангханса). Развивается остро, протекает стремительно с выраженными респираторными и интоксикационными симптомами (фебрильная лихорадка, ознобы, поты, адинамия, анорексия, одышка, кашель с мокротой). В клинике могут быть также 2 синдрома: абдоминальный (желтушность кожных покровов, увеличение печени и селезенки, асцит, значительное повышение в крови содержания билирубина, АСТ, АЛТ) и гематологический (увеличение печени, селезенки, периферических лимфатических узлов, в клиническом анализе крови агранулоцитоз, панцитопения, лейкемоидные реакции). Рентгенологически при острейшем туберкулезном сепсисе в легких с обеих стороны множественные очаги 3-5 мм, неправильной формы с преимущественной локализацией в средних и нижних отделах.
«Латентный» милиарный туберкулез чаще развивается у пожилых (женщины 70 лет и старше). Клинически отмечаются нерегулярная лихорадка, персистирующая в течение нескольких недель и анемия. Диагностика обычно посмертная, если не выполнено лучевое обследование органов дыхания.
Учитывая объективные трудности диагностики милиарного туберкулеза (клиническое многообразие, внелегочные локализации, отсутствие МБТ в мокроте, сложности интерпретации рентгенологической картины), практически следует использовать рекомендации экспертов Всемирной Организации Здравоохранения по туберкулезу: при лихорадке у больного более 7-10 дней и неустановленной ее этиологии необходимо в план дифференциальной диагностики включать милиарный туберкулез, а при невозможности его исключения назначать пробную противотуберкулезную терапию без применения антибиотиков широкого спектра действия (аминогликозидов, фторхинолонов, рифампицина, капреомицина). В случае милиарного туберкулеза температура тела начнет снижаться в течение первой же недели лечения (Д.Крофтон с соавт., 1996).
Подострый диссеминированный туберкулез легких развивается при менее значительных нарушениях иммунитета и меньшей массивности микобактериемии, чем при милиарном туберкулезе. Распространение инфекции из очагов послепервичного периода может происходить гематогенно, лимфогенно, лимфогематогенно. Провоцирующие факторы: неполноценное питание, психические травмы, гиперинсоляция, ВИЧ-инфекция (при уровне СД4 500-300 клеток/мкл) и др. В интерстиции, преимущественно в верхних и средних отделах легких, возникают очаги средних и крупных размеров (5-10 мм) с различной степенью сочетания экссудативной и продуктивной специфических реакций. Вследствие экссудации очаги склонны к слиянию с развитием лобулярной специфической пневмонии. При прогрессировании процесса образуются полости распада и характерные для подострого диссеминированного туберкулеза тонкостенные («штампованные») каверны без перифокальной реакции. Гематогенная диссеминация часто не ограничивается только легкими, в процесс вовлекаются плевра, верхние и нижние дыхательные пути, глотка, почки, половые органы и т.д. При лимфогенном рассеивании МБТ очаги преимущественно продуктивного характера образуются в средних и нижних отделах легких на фоне лимфангита. При инволюции подострого диссеминированного туберкулеза очаги могут рассасываться, инкапсулироваться, фиброзироваться. В окружающей ткани развивается пневмосклероз, эмфизема. Подострый диссеминированный туберкулез развивается постепенно, в течение нескольких недель. Несмотря на значительную протяженность поражения легких, самочувствие больного может быть хорошим, а общее состояние удовлетворительным и болезнь иногда выявляется при плановом флюорографическом обследовании. Но чаще появляются утомляемость, снижение работоспособности и аппетита, психоэмоциональная лабильность, потливость, повышение температуры тела, малопродуктивный кашель, одышка при физической нагрузке, кровохарканье, боль в груди при дыхании. Иногда первой манифестацией болезни может явиться внелегочное поражение: увеличение периферических лимфатических узлов (при сочетании с ВИЧ-инфекцией), боли при глотании, осиплость голоса, боли в пояснице и дизурические расстройства и другие. Состояние больных обычно удовлетворительное, дефицит массы тела отсутствует, кожные покровы обычного цвета. При перкуссии легких можно обнаружить укорочение звука в верхних отделах легких над зоной слияния очагов, при аускультации — незвучные мелко- или среднепузырчатые влажные хрипы. При прогрессировании процесса интоксикационный и респираторный синдромы усиливаются. Клинические «маски» подострого диссеминированного туберкулеза: ОРВИ, бронхит, пневмония, вегетативная сосудистая дистония, ларингит, пиелонефрит и другие. В клиническом анализе крови могут быть умеренно выраженные воспалительные изменения, лимфопения, моноцитоз. В клиническом анализе мочи (в случае специфического процесса в почках) — протеин-, лейкоцит- и эритроцитурия. Проба Манту с 2 ТЕ ППД-Л и Диаскинтест положительные, иногда гиперергические. В мокроте при возникновении в легких деструкции обнаруживаются эластические волокна, микобактерии туберкулеза (микроскопически и культурально). Рентгенологически в верхних и средних отделах обоих легких на фоне мелкосетчатого легочного рисунка множество очагов средних и крупных размеров, неправильной формы, с нечеткими контурами малой и средней интенсивности, с тенденцией к слиянию. При деструкции определяются одиночные, но чаще множественные тонкостенные кольцевидные тени различных размеров, создающими иногда картину «сотового» легкого. При лимфогенной диссеминации очаги асимметрично локализуются в средних и нижних отделах легких на фоне петлистой деформации легочного рисунка (лимфангит). Очаги средних размеров, с нечеткими контурами, без выраженной тенденции к слиянию и деструкции. Нередко на томограммах в средостении обнаруживаются обызвествленные лимфатические узлы. При фибробронхоскопии — явления диффузного катарального бронхита, при туберкулезе бронхов — бугорки, инфильтраты, язвы, иногда рубцы. Таким образом, для подострого диссеминированного туберкулеза характерна диссоциация между яркой рентгенологической картиной и скудными клиническими и физикальными проявлениями. При несвоевременной диагностике, неполноценном лечении подострый диссеминированный туберкулез приобретает хроническое течение.
Хронический диссеминированный туберкулез легких чаще наблюдается у лиц, уже состоящих на учете в противотуберкулезном диспансере, но иногда диагностируется и у впервые выявленных больных. Хронический диссеминированный туберкулез характеризуется длительным волнообразным течением. Периоды ремиссий сменяются периодами обострений с появлением в легких свежих очагов гематогенного или бронхогенного обсеменения. В период очередного обострения при гематогенной диссеминации очаги могут появиться в гортани, почках, костях и суставах, кишечнике и других органах. Клиническая картина хронического диссеминированного туберкулеза зависит от давности и фазы процесса. При обострении у больного усиливаются слабость, утомляемость, потливость, повышается температура тела, усиливается также кашель, увеличивается количество мокроты слизисто-гнойного характера, нарастает одышка, возможны кровохарканье и легочное кровотечение. В период ремиссии симптомы интоксикации уменьшаются, но одышка и продуктивный кашель становятся постоянными проявлениями болезни. Хроническое течение туберкулеза сопровождается выраженными личностными изменениями. Больные раздражительны, конфликтны, иногда агрессивны, безразличны к себе и окружающим, очень ранимы. Они быстро утомляются и истощаются. У больных может быть депрессия, возникают мысли о безнадежности своего состояния, нежелание считаться с рекомендациями врачей и лечиться. При объективном обследовании у больных отмечаются дефицит массы тела, снижение тургора тканей и эластичности кожи, акроцианоз при физической нагрузке или в покое. Перкуторная картина в легких «пестрая» — укорочение звука над зоной слияния свежих очагов и фиброза, тимпанит над поверхностно расположенными крупными кавернами, коробочный звук в нижних отделах легких вследствие эмфиземы. При аускультации могут выслушиваться рассеянные сухие, мелко- и среднепузырчатые влажные хрипы. Каверны могут быть «немыми», то есть перкуторно и аускультативно не выявляться. Рентгенологическая картина: легочный рисунок диффузно усилен, обогащен и деформирован, на этом фоне субтотально или тотально определяются полиморфные по величине, интенсивности, форме и четкости контуров множественные очаговые тени, полости распада в виде тонкостенных кольцевидных теней. Корни легких подтянуты вверх вследствие фиброза и уменьшения в объеме верхних отделов легких (симптом «падающего дождя» или «плакучей ивы»). Тень сердца имеет срединное расположение и измененную конфигурацию («капельное сердце», «дымовая труба»). В нижних отделах легочный рисунок обеднен, прозрачность легочных полей повышена вследствие эмфиземы. Показатели клинического анализа крови зависят от фазы процесса и отражают активность туберкулеза. Проба Манту с 2 ТЕ ППД-Л и Диаскинтест слабоположительны и диагностического значения не имеют. В мокроте больных обычно методами световой микроскопии, люминесцентной микроскопии и бактериологически обнаруживаются микобактерии туберкулеза, часто с множественной или широкой лекарственной устойчивостью. В процессе течения заболевания развиваются такие осложнением, как легочносердечная недостаточность, кровохарканье и легочное кровотечение, спонтанный пневмоторакс, эмпиема плевры, казеозная лобулярная пневмония, редко в настоящее время амилоидоз внутренних органов, которые могут привести к летальному исходу. Прогрессирование хронического диссеминированного туберкулеза легких приводит к формированию фибрознокавернозного туберкулеза.
2.4 Пневмокониозы (pneumon — «легкое», konia — «пыль») — это профессиональное заболевание легких, возникающее в результате воздействия промышленной пыли, проявляющееся хроническим диффузным пневмонитом с развитием фиброза легких.
Дифференциально-диагностическое значение имеют профессиональный маршрут больного, условия труда (химический состав пыли, ее концентрация в воздухе рабочей зоны, дисперсность, длительность экспозиции и т.д.), архивные данные профилактических осмотров.
По фиброгенным свойствам различат три класса опасности пылевых частиц:
1. Высокофиброгенные (двуокись кремния, асбест).
2. Средне- или умереннофиброгенные (тальк, стекловолокно, цемент, глина). Пневмокониозы от воздействия высоко- и умеренно фибриногенной пыли имеют склонность к прогрессированию и часто осложняются туберкулезом легких.
3. Слабофиброгенные (каменный уголь, магнезит). Эти пыли вызывают силикатозы (асбестоз, талькоз, коалиноз), карбокониозы (антракоз, графитоз), пневмокониозы шлифовальщиков и наждачников. Для них характерны умеренно выраженный фиброз, доброкачественное и малопрогрессирующее течение. Патоморфологически различают две формы пневмокониоза: узелковую и диффузно-склеротическую. Для узелковой формы характерно наличие периваскулярно и перибронхиально расположенных узелков различной формы в легочной ткани. При диффузно-склеротической форме ткань легкого уплотнена, неравномерной воздушности за счет разрастания грубых тяжей соединительной ткани, чередующихся с участками эмфиземы.
К наиболее частым пневмокониозам относится силикоз, развивающийся от воздействия пыли с содержанием свободной двуокиси кремния более 10%. В дифференциальной диагностике следует учитывать профессиональный анамнез. Для силикоза характерно длительное бессимптомное течение (иногда 15-20 лет). Кашель, выделение мокроты и одышка появляются часто в связи с сопутствующим бронхитом. Обращает на себя внимание относительно удовлетворительное общее состояние больного при массивных изменениях в легких. Распространенные мелкоочаговые тени в легких имеют четкие очертания, мономорфны, располагаются симметрично с обеих сторон, преимущественно в нижних и средних отделах на фоне грубых фиброзных изменений окружающей легочной ткани. Могут выявляться перинодулярная эмфизема, плевральные спайки, утолщения междолевой плевры. Корни как правило расширены, отмечается полицикличность их контура за счет плотных увеличенных лимфоузлов. Отдельные лимфатические узлы могут обызвествляться по типу «яичной скорлупы». Множественные узелковые тени на фоне деформированного по сетчатому и мелкоячеистому типу легочного рисунка составляют картину «снежной бури».
Для пневмокониозов характерны как рестриктивные, так и обструктивные нарушения ФВД. В БАЛ может выявляться нейтрофилез, лимфоцитоз. Контакт с асбестом подтверждает обнаружение в мокроте и БАЛ асбестовых телец, представляющих собой фагоцитированные волокна асбеста. Верификация диагноза осуществляется гистологически.
В лечении патогенетически обоснованным является применение антиоксидантной терапии, препаратов, улучшающих микроциркуляцию, снижающих давление в легочной артерии и оксигенотерапия.
3. Диссеминации опухолевой природы.
3.1. Бронхиолоальвеорлярный рак (БАР) — один из пяти основных подтипов аденокарциномы легкого (немелкоклеточный рак легкого), развивающийся из эпителиальных элементов дистальных бронхиол.
Группы риска БАР:
— имеющие хронические обструктивные заболевания легких;
— имеющие предшествующие онкологические заболевания верхних дыхательных путей и легких;
— имеющие в семейном анамнезе онкологическую патологию; — курильщики старше 40 лет.
Макроскопически выделяют пневмониеподобную, узловую (локальную), диссеминированную (мультинодальную) и смешанные формы БАР. Особенностью микроструктры опухоли является отсутствие собственной стромы — опухолевые клетки выстилают внутренние поверхности легочных альвеол. По гистологическому строению различат слизеобразующий (светлоклеточный) и без слизеобразования (темноклеточный) рак.
Классическая картина БАР отличается выделением большого количества слизистой пенистой мокроты (бронхорея). Периферическая локализация опухоли в верхней доле при узловой форме БАР характеризуется длительным бессимптомным течением. Наличие параканкрозного плеврального выпота чаще всего свидетельствует о плевральных метастазах. Наиболее частая локализация отделанных метастазов БАР — надпочечники, печени, кости, головной мозг.
На рентгенограмме и КТ вследствие развития лимфангита в прилегающей легочной ткани формируется своеобразная лучистость контуров опухолевого узла. Аденокарциномы отличаются длинными толстыми лучами, отходящими от очага к плевре и корню легкого. Для БАР характерно нарушение ФВД по смешанному типу. Опухолевые (аденоматозные) клетки могут быть обнаружены в мокроте, БАЛ. С целью верификации должна быть выполнена видеоторакоскопия с биопсией, при необходимости трансторакальная пункция, фибробронхоскопия. Терапия БАР зависит от стадии (хирургическая, химиотерапия или лучевая терапия).
3.2. Метастатическое поражение легких.
Метастазирование опухолей в легкие может осуществляться гематогенным, лимфогенным, бронхогенным или смешанным путем. Источником метастазирования чаще служат первичные злокачественные опухоли молочной железы, желудка, щитовидной железы, почки, толстого кишечника, поджелудочной железы, предстательной железы, яичка и яичников. Метастатическое поражение легких встречается у пациентов пожилого возраста, в анамнезе у них могут быть указания на перенесенную операцию по поводу опухоли.
Наиболее часто метастазы локализуются в нижних и средних отделах легких, поскольку эти зоны кровоснабжаются наиболее интенсивно. Гематогенные метастазы отличает бессимптомность, более выраженная клиническая картина наблюдается при лимфогенном пути распространения (прогрессирующая одышка, упорный непродуктивный мучительный кашель, интенсивные боли в грудной клетке). Параканкрозный выпот в плевральную полость имеет тенденцию к быстрому накоплению несмотря на частые пункции («неисчерпаемый»), часто носит серозно-геморрагический характер, может содержать атипичные клетки (АК). Состояние больных быстро ухудшается.
При рентгенологическом исследовании выявляют густую мелкоочаговую диссеминацию на всем протяжении легочных полей. Очаги имеют четкие и ровные контуры, без тенденции к слиянию и распаду крупные и мономорфные («штампованные», «монетовидные»), окружающая легочная ткань не изменена, без признаков воспаления и очагов отсева. В центральных отделах легких равномерное утолщение междольковых перегородок может определяться как линии Керли. Характерно нарастание изменений на рентгенограмме легких при оценке в динамике. На КТ метастазы имеют неправильную форму, бугристые контуры. Для верификации диагноза используют ФБС, цитологическое исследование БАЛ, видеоторакоскоскопию, чрезбронхиальную и открытую биопсию легкого. В большинстве случаев методом выбора при лечении метастатического поражения легких является химиотерапия.
3.3. Лимфангиолеймиоматоз легких (ЛАМ) — редкое заболевание, характеризующееся опухолеподобным разрастанием гладкомышечных волокон в интерстициальной ткани легких с последующей мелкокистозной трансформацией легочной паренхимы.
Болезнь поражает только женщин детородного возраста (около 30 лет). Этиология неизвестна, предполагается важная роль эндокринных нарушений в возникновения ЛАМ. Основой патологического процесса является пролиферация гладкомышечных клеток в интерстиции, стенках бронхов и сосудов, лимфатических узлах, а также других органах (матка, почки, абдоминальные лимфатические узлы, кишечник). В 70% случаев у больных ЛАМ выявляются лейомиомы (фибромиомы) матки, односторонние ангиомиолипомы почек.
Различают две морфологические формы ЛАМ: очаговую и диффузную. Симптомы ЛАМ мало специфичны: усиливающаяся одышка, кровохарканье, рецидивирующий пневмоторакс. По мере прогрессирования заболевания возможны хилезный плевральный выпот, хилезный асцит (хилоперитонеум), хилоперикардит, хилурия.
Рентгенологически ЛАМ характеризуется появлением множественных булл (эмфизематозных вздутий диаметром до 2см) на фоне усиления легочного рисунка («кистозно-буллезное легкое»), нередко синдром плеврального выпота. Характерен обструктивный тип нарушений ФВД. Верификация диагноза производится при биопсии. Лечение симптоматическое. Прогноз неблагоприятный.
3.4. Эпителиодная гемангиоэндотелиома легких (ЭГЛ) — многофокусное образование с низкой степенью злокачественности, поражающее легкие, реже печень, кости, мягкие ткани.
ЭГЛ возникает преимущественно у женщин в возрасте от 12 до 60 лет. Макроскопически в материале биопсии выявляются серо-белого цвета очаги хрящевой плотности размерами от 0,1 до 2-3 см в диаметре без капсулы. В большинстве случаев ЭГЛ протекает бессимптомно, а изменения легочной ткани обнаруживаются при профилактических осмотрах. На рентгенограммах и КТ определяются множественные узелки разной величины и интенсивности с четкими контурами. Диагноз устанавливается только гистологически.
4. Болезни накопления
4.1. Альвеолярный протеиноз (АП) — редкое заболевание неизвестной этиологии, характеризующееся прогрессирующей одышкой вследствие накопления в альвеолах и мелких дыхательных путях внеклеточно расположенного белковолипоидного вещества, дающего положительную PAS-реакцию (пурпурное окрашивание при применении реактива Шиффа).
Первичный АП встречается преимущественно у мужчин 20-50 лет. Вторичный протеиноз является осложнением других (прежде всего гематологических) заболеваниях. Ключевым звеном патогенеза АП является дисбаланс обмена фосфолипидов, в результате чего в альвеолярном пространстве накапливается сурфактантоподобное вещество.
В течение длительного времени заболевание протекает бессимптомно. По мере прогрессирования нарастает одышка, появляется сухой кашель, субфебрильная температура, боли в груди, похудание, быстрая утомляемость, изредка кровохарканье.
На рентгенограмме определяется мелкоочаговая диссеминация, имеющая тенденцию к слиянию, преимущественно в средних и нижних долях, часто базальные инфильтраты. Корреляция между клиническими и рентгенологическими данными отсутствует. Со временем формируется рестриктивный тип нарушения ФВД. БАЛ представляет собой маслянистую непрозрачную жидкость, молочно белого цвета, которая образует белый осадок при отстаивании. В БАЛ патогномонично многократное увеличение белка, большое количество PASположительный эозинофильных бесклеточных телец. При биопсии легочной ткани в альвеолах также выявляется материал, дающий положительную PASреакцию.
При АП противопоказано назначение антибактериальных, глюкокортикоидных препаратов, иммуносупрессантов в связи с их неэффективностью. Единственным эффективным методом терапии больных является лечебный бронхоальвеолярный лаваж. Течение болезни доброкачественное.
4.2. Амилоидоз легочный — системное заболевание, характеризующееся внеклеточным отложением фибрилл амилоида (нерастворимых депозитов белка) в паренхиме легких, стенках сосудов, слизистой оболочке дыхательных путей, плевре, лимфатических узлах средостения.
Мужчины болеют чаще, чем женщины, в большинстве случаев заболевание развивается после 40 лет.
Классификация амилоидоза:
1) первичный (врожденная ферментопатия, наследуемая аутосомнодоминатным путем);
2) вторичный (развивается на фоне хронических заболеваний — остеомиелита, туберкулеза, бронхоэктатической болезни, опухолей, сифилиса, малярии,
ДЗСТ); 3) идиопатический; 4) сенильный.
В основе патогенеза амилоидоза — гиперсинтез иммуноглобулинов Вклетками. Для солитарной формы амилоидоза характерно образование одного или нескольких очаговых (псевдоопухолевых) отложений амилоида в паренхиме легких. Диффузный амилоидоз характеризуется отложением амилоида в межальвеолярных перегородках, вокруг капилляров.
Клинические варианты амилоидоза:
• трахеобронхиальный амилоидоз (жалобы на надсадный сухой кашель, затрудненное свистящее дыхание, охриплость голоса, кровохарканье; при нарушении бронхиальной проходимости — рецидивирующие воспалительные процессы и ателектазы в соответствующей части легкого);
• узловой паренхиматозный амилоидоз (характерны локальные симптомы, системные проявления, как правило, отсутствуют);
• диффузный амилоидоз легких (протекает тяжело, свойственна прогрессирующая рефрактерная к лечению одышка, кашель, рецидивирующее кровохарканье);
• орофарингеальный амилоидоз с макроглоссией;
• амилоидоз лимфатических узлов ворот легкого и(или) средостения (может сопровождаться синдромом верхней полой вены);
• амилоидоз плевры и сосудов легких (встречается редко).
У больных амилоидозом в биохимическом анализе крови определяются гипергаммаглобулинемия, гиперхолестеринемия, гиперфибриногенемия, повышение уровня щелочной фосфатазы. На рентгенограмме при амилоидозе обнаруживаются множественные очаги с четкими контурами на фоне усиления и деформации легочного рисунка. Нарушение ФВД зависит от формы амилоидоза: при трахеобронхиальном амилоидозе выявляется обструктивный тип нарушений, при диффузном амилоидозе — рестриктивный. Диагноз может быть верифицирован только при гистологическом исследовании биопсийного материла (легкого, трахеи, бронхов). Амилоид дает положительную окраску Конго красным.
При лечении вторичного амилоидоза показана активная терапия основного заболевания. В терапии первичного амилоидоза противопоказано использование глюкокортикостероидов и цитостатиков, так как возникающее угнетение иммунной системы способствует амилоидогенезу. Прогноз при диффузной и узловой паренхиматозной формах амилоидоза неблагоприятен.
4.3. Идиопатический гемосидероз легких (ИГЛ) — редкое заболевание, характеризующееся эпизодическим кровохарканьем вследствие рецидивирующих внутриальвеолярных кровоизлияний, вторичной железодефицитной анемией и волнообразным течением, приводящим к распространенному пневмофиброзу и дыхательной недостаточности.
Болезнь чаще встречается в детском возрасте (обычно до 10 лет), среди взрослых чаще болеют мужчины 20-40 лет. В последние годы наиболее распространена гипотеза об иммуноаллергической природе заболевания. При первичном ИГЛ реакция антиген-антитело приводит к некрозу эндотелия и нарушению структуры альвеолярно-капиллярной мембраны, что обусловливает микрокровоизлияния и импрегнацию паренхимы легких солями железа. В результате накапливаются альвеолярные макрофаги, содержащие гемосидерин. Вторичный гемосидероз легких — синдром других заболеваний, сопровождающихся повторными кровоизлияниями в альвеолы (левожелудочковая недостаточность, тромбоцитопеническая пурпура, системные васкулиты).
В клинической картине ИГЛ чередуются периоды ремиссии и кризы. Кризы характеризуются резкой слабостью, лихорадкой, кровохарканьем, головокружением, болями в грудной клетке. Выраженность одышки тем больше, чем значительнее площадь кровоизлияния в легочную паренхиму. Присоединение инфаркт-пневмонии, рецидивирующего пневмоторакса, легочного кровотечения может привести к летальному исходу. В гемограмме определяется микроцитарная гипохромная анемия, снижение сывороточного железа, повышение билирубина. Рентгенологическая картина характеризуется появлением двусторонних множественных мелкоочаговых теней или крупных инфильтратов, сливающихся между собой. Характерная особенность при ИГЛ — внезапное возникновение рентгенологических изменений и быстрая обратная динамика. При спирометрии в большинстве случаев определяется обструктивный синдром. Диагноз должен быть подтвержден гистологически — при биопсии в альвеолах выявляется большое количество гемосидерофагов.
В лечении ИГЛ в настоящее время применяются глюкокортикостероиды, цитостатики, десферал (дефероксамин), плазмаферез.
5. Системные васкулиты с поражением легких.
5.1. Гранулематоз Вегенера (ГВ) — гранулематозное воспаление респираторного тракта и некротизирующий васкулит, поражающий мелкие и средние сосуды, обычно сочетающийся с некротизирующим гломерулонефритом.
ГВ обычно дебютирует в возрасте 35-45 лет. Центральным звеном патогенеза является синтез антинейтрофильных цитоплазматических аутоантител (АНЦА) к протеиназе-3 (90% больных). АНЦА активируют выработку эпителиальными клетками провоспалительных цитокинов, а также напрямую повреждают клетки эндотелия. Морфологическим субстратом ГВ является васкулит, гранулематозное воспаление (скопление гигантских клеток Лангханса, плазматических клеток, лимфоцитов и гистиоцитов) и паренхиматозный некроз.
Для клинической картины ГВ характерна триада симптомов:
? некротизирующий гранулематозный процесс в верхних дыхательных путях (риниты и синуситы с образованием язв, деструкцией, гнойные отиты);
? системный некротизирующий васкулит с поражением легких (кашель, одышка, кровохарканье, геморрагический плеврит);
? очаговый или диффузный некротизирующий гломерулонефрит.
Возможно поражение других органов и систем, общие симптомы воспаления (лихорадка септического типа, похудание, артралгии, миалгии).
Среди лабораторных показателей специфичным является только наличие АНЦА к протеиназе-3 в сыворотке крови. На рентгенограммах легких выявляются множественные обширные инфильтраты, в центре которых нередко образуются полости распада от нескольких миллиметров до 10 см в диаметре (фиброзно-гнойный процесс с некрозом), а также геморрагические инфаркты легкого, милиарная диссеминация. Исследование ФВД обычно выявляет смешанные нарушения вентиляционной функции. Необходимо гистологическое подтверждение диагноза (биопсия слизистой носа, придаточных пазух, почек, легкого).
Диагностические критерии ГВ (Американская ассоциация ревматологов, 1990г):
— воспаление носа и полости рта
— рентгенологические изменения в легких
— гранулематозное воспаление при биопсии органов диагноза Наличие двух из четырех критериев свидетельствует о достоверном ГВ.
При ГВ проводят комбинированное лечение цитостатиками (циклофосфамид) и глюкокортикоидами. Патогенетическая терапия включает антикоагулянты, антиагреганты, плазмаферез, гемосорбцию, витамины, стимуляторы кроветворения, гемотрансфузии.
5.2. Синдром Чарджа-Стросса (Churg-Ctrauss) (CЧС) — эозинофильное гранулематозное воспаление респираторного тракта и некротизирующий васкулит, поражающий мелкие и средние сосуды, часто сочетающийся с астмой и эозинофилией.
Чаще болеют мужчины, в возрасте 35-50 лет. В патогенезе СЧС большое значение придают АНЦА, обладающим специфичностью к миелопероксидазе. При СЧС в интерстиции легких, стенке сосудов и бронхиол формируются некротизирующие гранулемы, состоящие из центрального эозинофильного ядра и радиально окружающих его макрофагов и гигантских клеток («эозинофильные микроабсцессы»).
СЧС — хроническое рецидивирующее заболевание. Для продромального периода характерны аллергический ринит, поллиноз, синусит, синдром бронхиальной астмы. Во втором периоде наблюдается высокая эозинофилия (иногда достигающая 80%) в периферической крови. Генерализация болезни в третьем периоде сопровождается полиорганными поражениями (мигрирующие двусторонние инфильтраты в легочной ткани, эозинофильный плевральный выпот, кровохарканье, лихорадка, эозинофильный гастроэнтерит, эозинофильные гранулемы в миокарде, полинейропатия, энцефалопатия, крапивница, артралгия, миалгия).
Диагностика СЧС основывается на триаде симтомов:
1) выраженный бронхоспастический синдром; 2) гиперэозинофилия (более 10%); 3) симптомокомплекс васкулита.
Иммунологические исследования крови позволяют выявить повышенные уровни циркулирующих иммунных комплексов (ЦИК), общего IgE, АНЦА со специфичностью к миелопероксидазе. На рентгенограммах обнаруживаются летучие инфильтраты, занимающие большой объем (1-2 доли, тотальное затемнение) без полостей распада. При исследовании ФВД чаще всего выявляется синдром обратимой бронхиальной обструкции. Для гистологической диагностики используют материал, полученный при биопсии пораженных органов (легкие, кожа, слизистая носа, желудочно-кишечный тракт).
Диагностические критерии СЧС (Американская коллегия ревматологов,
1990г):
• аллергия в анамезе
• легочные инфильтраты
Наличие у больного четырех из перечисленных признаков позволяет поставить достоверный диагноз СЧС.
В качестве базисной терапии СЧС используются глюкокортикоиды (в том числе и ингаляционные), бронхолитические препараты, антикоагулянты.
5.3. Синдром Гудпасчера (легочно-почечный синдром) (СГ) — редкое аутоиммунное заболевание, при котором в патологический процесс вовлекаются базальные мембраны сосудов легких и почек.
Болеют преимущественно мужчины в возрасте 18-35 лет. В основе патогенеза лежит цитотоксическая тканевая реакция. Под влиянием неустановленных этиологических факторов развивается аутоиммунная реакция к базальным мембранам сосудов почечных клубочков и альвеолярно-капиллярной мембране. В результате иммунокомплексного поражения мембран нарушается их проницаемость. Отсюда появление основных клинических симптомов СГ: кровохарканье (легочное кровотечение) и мочевой синдром (протеинурия, гематурия, цилиндрурия). Больной во время кашля выделяет пенистую ярко-красную мокроту, возможны непостоянные боли в груди, одышка, лихорадка и общая слабость. Прогрессирование поражения почек сопровождается картиной почечной недостаточности.
Диагноз устанавливают на основании сочетания респираторной и почечной симптоматики. Лабораторными признаками служат: гипохромная анемия, анизоцитоз, пойкилоцитоз, снижение уровня железа в сыворотке крови, признаки почечной недостаточности в биохимическом анализе крови, выявление циркулирующих антител против базальных мембран и повышенное содержание циркулирующих иммунных комплексов при серологическом обследовании. При исследовании ФВД определяется рестриктивный тип нарушений. При рентгенологическом исследовании выявляются мелкоочаговая диссеминация на фоне сетчатой деформации легочного рисунка, иногда инфаркты легкого. Для лечения СГ применяют комбинированную терапию иммунодепрессантами (азатиоприн, циклофосфамид) и глюкокортикостероидами в сочетании с плазмаферезом. Прогноз неблагоприятный.
6. Интерстициальные фиброзы легких.
6.1. Диффузные заболевания соединительной ткани (ДЗСТ) сопровождаются различными вариантами поражения легких. При проведении дифференциальной диагностики важными являются системность заболевания (полисиндромность) и его внелегочные проявления. При необходимости верификации диагноза выполняется биопсия легкого.
При системной склеродермии поражение легких чаще возникает на фоне уже развернутой картины основного заболевания (у 50-70% больных). Варианты поражения легких при склеродермии:
• Интерстициальный фиброз легких (на рентгенограмме визуализируются сетчатая деформация легочного рисунка преимущественно в базальных отделах («сотовая перестройка»); при исследовании ФВД наблюдается снижение объемов по рестриктивному типу).
• Легочный васкулит.
• Вторичная легочная гипертензия.
Поражение легких при ревматоидном артрите (РА) встречается у 4-30% пациентов. Возможные следующие варианты легочных изменений:
• Плеврит (обычно возникает в течение первых пяти лет дебюта суставного синдрома и носит двусторонний экссудативный характер).
• Фиброзирующий альвеолит (проявляется постепенно нарастающей одышкой с затруднением вдоха, сухим кашлем)
• Легочные ревматоидные узелки (множественные, диаметром от 1 до 3 см, ассоциируются с высоким титром ревматоидного фактора).
• Бронхиолит (клинически проявляется стойкой одышкой с затруднением выдоха, цианозом, при исследовании ФВД выявляется обструктивный синдром).
• Вторичная артериальная легочная гипертензия.
• Вторичные инфекционные поражения легких (туберкулез, бактериальные пневмонии, пневмоцистные пневмонии, бронхоэктазии). Фактором, предрасполагающим к инфекционным осложнениям, становится все шире применяемое лечение биологическими агентами — ингибиторами TNF-? (инфликсимаб, адалимумаб).
• Лекарственное поражение легких. Наиболее часто встречаются метотрексатиндуцированные интерстициальные пневмониты («метотрексатный пневмонит»). Это потенциальное опасное для жизни осложнение терапии, требует отмены препарата, клинически проявляется лихорадкой, кашлем, одышкой, распространенной крепитацией, функциональными рестриктивными нарушениями, инфильтратами на рентгенограмме и эозинофилией в периферической крови.
Варианты легочных проявлений при системной красной волчанке:
• Волчаночный плеврит (чаще двусторонний экссудативный, в клеточном составе преобладают лимфоциты, определяются LE-клетки, антинуклеарный фактор, высокий уровень глюкозы).
• Острый волчаночный пневмонит (тяжелая форма, развивается на фоне генерализации болезни, проявляется одышкой, кашлем, кровохарканьем, лихорадкой).
• Вторичная легочная гипертензия.
• Поражение дыхательных мышц («синдром усадки легкого»). У пациента возникает одышка, усиливающаяся в положении сидя, вследствие поражения диафрагмального нерва, обусловливающего паралич диафрагмы.
• Инфекционные осложнения (очень характерны вследствие снижения иммунитета)
При дерматомиозите поражение легких возможно по типу фиброзирующего альвеолита или синдрома мышечных расстройств (поражение дыхательной мускулатуры, высокое стояние купола диафрагмы приводят к рестриктивным изменениям ФВД).
При хронической ревматической болезни сердца у 1-3% больных наблюдаются ревматические пневмонии. Кроме того, возможно развитие васкулита, плеврита, гемосидероза, пневмонита, интерстициального фиброза. Перечисленные изменения возникают на фоне активации ревматизма, характерна быстрая динамика при противоревматическом лечении.
При узелковом периартериите поражение легких встречается у 10-30% больных. Характерны боли в грудной клетке, кашель, кровохаркание, одышка. На рентгенограммах легких видны множественные округлые тени с центральным размягчением. Диагностическое значение имеет системность поражения.
6.2 Кардиогенный пневмосклероз при левожелудочковой недостаточности — характеризуется двусторонней очаговой диссеминацией, развивается при пороках сердца, чаще при стенозе митрального клапана. У больных наблюдаются:
• положение ортопное,
• выраженная одышка в покое и при разговоре,
• акроцианоз, дистанционные хрипы,
• нарушение показателей общей гемодинамики и сознания.
• Аускультативно определяются:
• глухие сердечные тоны, нередко ритм галопа,
• над легкими — значительное количество влажных средне- и крупнопузырчатых хрипов симметрично в нижних отделах обоих легких.
При исследовании мокроты можно обнаружить «клетки сердечных пороков».
Рентгенологическое исследование выявляет множественные очаговые тени в прикорневых и базальных отделах легких на фоне усиленного легочного рисунка, увеличение кардиоторакального индекса (более 50%). В плевральной полости нередко двусторонний плевральный выпот.
Тестовые задания по теме.
Выберите один или несколько правильных ответов.
1. СИНДРОМ ЛЕГОЧНОЙ ДИССЕМИНАЦИИ — ЭТО
1) клинико-рентгенологический синдром, для которого характерны клинические проявления дыхательной недостаточности и ретикуло-нодулярные изменения на рентгенограмме
2) рентгенологический синдром, для которого характерно появление множественных очаговых затемнений и/или усиление и сетчатая деформация легочного рисунка чаще двусторонней локализации
3) рентгенологический синдром, для которого характерно появление множественных очаговых затемнений чаще двусторонней локализации
4) рентгенологический синдром, для которого характерно усиление и сетчатая деформация легочного рисунка чаще двусторонней локализации
2. ДИССЕМИНАЦИЯ С РАЗМЕРАМИ ОЧАГОВ 5-8 ММ НАЗЫВАЕТСЯ
4) крупноочаговой
3. В МОРФОЛОГИЧЕСКУЮ КЛАССИФИКАЦИЮ ДИССЕМИНИРОВАННЫХ ПРОЦЕССОВ ВХОДЯТ ВСЕ ПЕРЕЧИСЛЕННЫЕ ГРУППЫ ЗАБОЛЕВАНИЙ, КРОМЕ
3) опухолевые
4. КАКОВ НАИБОЛЕЕ ХАРАКТЕРНЫЙ ФИЗИКАЛЬНЫЙ СИМПТОМ ИДИОПАТИЧЕ-
СКОГО ФИБРОЗИРУЮЩЕГО АЛЬВЕОЛИТА
1) цианоз
2) снижение эластичности грудной клетки
3) притупление перкуторного звука
4) двусторонняя крепитация в нижних отделах легких, напоминающая треск целлофана
5. ДЛЯ ДИССЕМИНИРОВАННЫХ ЗАБОЛЕВАНИЙ ЛЕГКИХ ХАРАКТЕРНЫ ВСЕ ПРИЗНАКИ КРОМЕ ОДНОГО
1) прогрессирующая одышка
2) двухсторонняя диссеминация на рентгенограмме
3) обструктивные изменения на спирограмме
4) рестриктивные изменения на спирограмме
6. КАК НАЗЫВАЕТСЯ ОДИН ИЗ ВАРИАНТОВ ОСТРОГО НАЧАЛА САРКОИДОЗА
1) синдром Горнера
2) синдром Чарджа-Стросса
3) синдром Лефгрена
4) синдром Дресслера
7. ХАРАКТЕРНЫМИ ЛАБОРТАРНЫМИ ПРИЗНАКАМИ САРКОИДОЗА ЯВЛЯЮТСЯ
1) гиперурикемия
3) повышение активности АПФ и гиперкальциемия
8. К КЛИНИЧЕСКИМ ФОРМАМ ОСТРОГО ДИССЕМИНИРОВАННОГО ТУБЕРКУЛЕЗА
ОТНОСЯТСЯ ВСЕ ПЕРЕЧИСЛЕННЫЕ, КРОМЕ
4) менингеальная
5) острейший туберкулезный сепсис
9. КАКОЙ РЕНТГЕНОЛОГИЧЕСКИЙ СИМПТОМ ХАРАКТЕРЕН ДЛЯ ПНЕВМОКОНИОЗОВ
1) «сотовое легкое»
2) симптом «рассыпанных монет»
3) симптом «снежной бури»
4) симптом «матового стекла»
10. НАИБОЛЕЕ ЧАСТЫМИ ИСТОЧНИКАМИ МЕТАСТАТИЧЕСКОГО ПОРЖЕНИЯ ЛЕГКИХ ЯВЛЯЮТСЯ ВСЕ ПЕРЕЧИСЛЕННЫЕ ОПУХОЛИ, КРОМЕ:
1) молочной железы
3) матки 4) щитовидной железы
Ситуационная задача № 4
Пациент К., 36 лет, работающий шлифовщиком камня, обратился к участковому терапевту с жалобами на малопродуктивный кашель, одышку при значительной физической нагрузке, повышенную утомляемость, снижение работоспособности и аппетита, повышение температуры тела до 37,2-37,6?С. Больным себя считает на протяжении 1,5-2 месяцев. За медицинской помощью ранее не обращался, принимал парацетамол, лазолван без значительного эффекта.
Флюорографическое обследование — 6 месяцев назад, изменений в легких не обнаружено.
При объективном обследовании общее состояние больного удовлетворительное, кожные и слизистые покровы чистые, бледно-розовые. ИМТ = 24,5. Периферические лимфатические узлы пальпируются в 4-х группах, единичные, безболезненные, размерами до 1,0 см. Грудная клетка нормостеническая, симметрично участвует в акте дыхания, число дыханий 19 в мин. При сравнительной перкуссии притупление звука слева в I-II межреберьях, при аускультации дыхание в этой зоне бронхиальное, выслушиваются немночисленные среднепузырчатые влажные хрипы после покашливания. Над остальными отделами легких перкуторный звук легочный, дыхание ослабленное везикулярное. Пульс — 92 удара в мин., ритмичный. АД — 130/65 мм рт.ст. Ритм сердечных сокращений нормальный, тоны нормальной звучности, дополнительные шумы отсутствуют. Живот обычной конфигурации, мягкий и безболезненный при пальпации. Размеры печени и селезенки не увеличены. Периферических отеков нет.
Вопросы:
1. Поставьте предварительный диагноз.
2. С какими заболеваниями нужно провести дифференциальный диагноз?
3. Составьте план дополнительных методов исследования.
4. Оцените результаты дополнительного обследования.
5. Сформулируйте клинический диагноз в соответствии с классификацией.
6. Определите тактику дальнейшего ведения пациента.
Приложения к ситуационной задаче № 4
Анализ крови общий
эритроциты — 3,5 т/л, Нв — 120 г/л, лейкоциты — 11,4 Г/л, э — 1%, п — 16%, с — 50%, м — 17%, л — 16%, СОЭ — 36 мм/час. Анализ мочи общий реакция — слабо кислая, относительная плотность — 1017, белок и сахар не обнаружены, лейкоциты — 3-4 в зр., эритроциты — 0-1 в п/зр. Исследование мокроты на кислотоустойчивые микобактерии в одном образце из 3-х обнаружены КУМ (10 в 100 полях зрения). Обзорная рентгенограмма органов грудной клетки в прямой проекции
В легких с обеих сторон множественные рассеянные очаговые тени размерами 3-5 мм, средней интенсивности, без четких контуров, с тенденцией к слиянию. Слева в S1-2 определяется кольцевидная тень размерами 3 см с нечетким внутренним и наружным контуром. V. ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ ПРИ СИНДРОМЕ
Плевральный выпот — это клинико-рентгенологический синдром, в основе которого лежит скопление патологической жидкости в плевральной полости при воспалительных процессах в прилежащих органах или листках плевры или же при нарушении соотношения между коллоидно-осмотическим давлением плазмы крови и гидростатическим давлением в капиллярах.
В нормальных условиях плевральная жидкость образуется в апикальной части париетальной плевры. Дренирование жидкости происходит посредством лимфатических пор, также расположенных в париетальной плевре. В физиологических условиях висцеральная плевра в фильтрации плевральной жидкости не участвует.
Образование экссудативного выпота обусловлено повышением проницаемости капилляров париетальной плевры, приводящей к увеличению содержания белка в плевральной жидкости, либо изменениями плевральной поверхности, приводящими к снижению внутриплеврального давления.
Для накопления транссудата необходимо, чтобы либо повысилось капиллярное давление в малом круге кровообращения, либо чтобы снизилось онкотическое давление плазмы крови до уровня, когда количество образующейся жидкости превысит количество выводимой.
Классификация плевральных выпотов По этиологии.
Источник: need4stud.ru
Параканкрозная пневмония при бронхо-альвеолярной карциноме
Саркоидоз легких АБСЦЕСС ЛЕГКОГО — это чаще всего вторичный гнойно-деструктивный ограниченный процесс в легких, осложняющий различные заболевания и патологические состояния. Характеризуется образованием одной или нескольких полостей с гнойным содержимым в легочной паренхиме, окруженных грануляционной тканью, зоной перифокальной воспалительной инфильтрации; протекает с выраженной интоксикацией и лихорадкой. В зависимости от варианта развития различаются постпневмонические, обтурационные, аспирационные, гематогенно-эмболические, лимфогенные и травматические абсцессы в легких. Абсцесс легкого может быть острым и хроническим.
Этиология и патогенез. Образование абсцесса легкого главным образом зависит от способности патогенной инфекции выделять соответствующие ферменты и токсины, приводящие к некрозу легочной ткани.
Некроз легочной ткани способны вызвать золотистый стафилококк, клебсиеллы, стрептококки группы А, бактероиды, фузобактерии, анаэробные и микроаэрофильные кокки и стрептококки, другие анаэробы, нокардии, микобактерии, грибы (гистоплазмы, аспергиллы, кокцидиоиды), паразиты (амебы, легочные двуустки).
В соответствии с последовательностью патологоанатомических изменений выделяются три фазы развития абсцесса легкого: 1) пневмоническая; 2) пневмобронхическая; 3) полостная. В первой фазе наблюдаются лейкоцитарная инфильтрация, экссудация, нагноение и некроз капилляров альвеол,бронхиол, полнокровие и лимфостаз, тромбозы и кровоизлияния. Во второй фазе в процесс вовлекаются бронхи, происходит расплавление некротизированного участка, проникновение воздуха в абсцесс, ограничение воспалительного фокуса грануляционным валом и соединительнотканной капсулой. В третьей фазе полость абсцесса опорожняется, образуется фиброзная капсула, появляются участки ателектаза и дистелектаза, в процесс вовлекается плевра.
В ряде случаев абсцесс легкого осложняется плевритом, эмпиемой, пиопневмотораксом.
Клиническая картина и диагноз. Небольшие абсцессы легкого, чаще эмболические, расположенные центрально, не дают характерной клинической симптоматики.
При развитии более значительного абсцесса (например, аспирационного) часто удается проследить дни периода: 1) расплавления легочной ткани с формированием абсцесса (до его вскрытия); 2) после прорыва абсцесса в бронх. Первый период продолжается в среднем 10-12 дн и по симптомам нередко напоминает крупозную пневмонию: острое начало, тяжелое состояние, лихорадка (умеренная, а затем гектическая) с ознобами и проливным потом, сухой надсадный кашель, сильные боли в груди при дыхании, одышка.
Физикальные данные в первом периоде зависят от фазы, размеров, характера осложнений и давности абсцесса легкого. В условиях поражения большего объема выявляются ограничения дыхательных экскурсий грудной клетки, укорочение перкуторного звука, жесткое, бронховезикулярное, а иногда бронхиальное дыхание на небольшом участке грудной клетки. В некоторых случаях определяются влажные и сухие хрипы.
После прорыва абсцесса в бронх наступает значительное улучшение: температура снижается, прекращается познабливание, улучшается аппетит. Прорыв гнойника в бронх часто сопровождается приступом кашля с внезапным выделением большого количества мокроты (100-500 мл).
Мокрота при абсцессе легкого обычно зловонная, что обусловлено присоединением гнилостной флоры.
Для абсцесса легкого характерна зависимость отделения мокроты от положения тела больного.
Дальнейшая симптоматика и течение абсцесса легкого определяются состоянием бронхиального дренажа. Если гнойник опорожнился хорошо и проводилось адекватное лечение, через 6-8 лет на месте полости абсцесса образуется рубец и наступает выздоровление. При плохом бронхиальном дренаже воспалительный процесс протекает либо волнообразно со сменой ремиссий и обострений, либо постепенно прогрессирует с нарастанием явлений интоксикации.
Различаются следующие осложнения абсцесса легкого: 1) прорыв гнойника в плевральную полость с развитием пиопневмоторакса; 2) легочное кровотечение; 3) напряженный клапанный пневмоторакс; 4) септикопиемия; 5) вторичные бронхоэктазы; 6) амилоидоз.
В первом периоде абсцесса легкого отмечаются выраженный лейкоцитоз со сдвигом лейкоцитарной формулы влево, абсолютная лимфопения, гипохромная анемия, увеличение СОЭ.
При больших потерях белка с гноем (общее количество гноя может достигать более 500 мл в течение суток, в результате чего теряется до 50 г белка) отмечаются гипопротеинемия и диспротеинемия (уменьшается содержание альбуминов в сыворотке крови и повышается уровень альфа-глобулиновых фракций белка). Увеличивается концентрация мукопротеина, сиаловых кислот, гаптоглобина.
В мокроте больного с абсцессом легкого отмечаются большое количество разрушающихся лейкоцитов, распадающиеся обрывки легочной ткани, эластические волокна, кристаллы гематоидина, холестерина, жирных кислот.
При бактериоскопии мокроты можно обнаружить в значительном количестве труднокультивируемые микроорганизмы, которые попадают в нее непосредственно из очага деструкции.
Рентгенологическая картина в первом периоде характеризуется крупноочаговым затемнением с неровными краями и нечеткими контурами. В последующем, после прорыва абсцесса в бронх, рентгенологически в полости абсцесса выявляется большее или меньшее количество воздуха, который либо располагается в виде серпа при наличии плотного содержимого в полости абсцесса, либо обусловливает характерную картину горизонтального уровня жидкости в полости.
Результаты бронхоскопии имеют решающее диагностическое значение только при обтурационных абсцессах легкого.
Острый абсцесс дифференцируют с заболеваниями, которые могут вызывать образование полостей в легких: туберкулезом, раком легкого, кистами легкого, бронхаэктазией, грибковой инфекцией (аспергиллемой легких), острой деструктивной пневмонией (вызванной грамотрицательными бактериями и золотистым стафилококком), васкулитами, септической эмболией и ТЭЛА, осложненной инфарктом легкого.
Лечение. Основой лечения большинства больных с острыми легочными нагноениями являются интенсивная комплексная консервативная терапия с использованием ряда приемов и манипуляций “малой хирургии” и эндоскопические методы. Комплексная консервативная терапия включает:
1) поддержание и восстановление общего состояния и коррекцию нарушенного гомеостаза;
2) подавление микроорганизмов — возбудителей инфекционного процесса (в том числе вирусов);
3) обеспечение оптимального дренирования очагов деструкции в легком (в плевре);
4) коррекцию иммунологической реактивности. При наличии зловонной мокроты или зловонного запаха изо рта больного необходимо изолировать от других пациентов.
Питание должно быть разнообразным, высококалорийным, витаминизированным и содержать большое количество белка.
С первого дня лечения проводятся массивная дезинтоксикационная инфузионная (внутривенное введение гемодеза, полиглюкина, 40 % раствора глюкозы, плазмы и т. д.) и десенсибилизирующая (кальция хлорид — 10 % раствор, 10 мл, или 1 % раствор, 100-200 мл, внутривенно, супрастин, димедрол и т. д.) терапия. Энергетический баланс целесообразно поддерживать введением концентрированных растворов глюкозы с добавлением соответствующего количества инсулина (1 ЕД на 3-4 г глюкозы).
Белковые потери восполняются вливанием белковых гидролизатов — аминокровина (осветленного), гидролизина (осветленного), инфузамина, а также растворов аминокислот — полиамина, амикина и др.
При выраженной анемии производятся трансфузии свежей донорской крови или эритроцитарной массы по 250-500 мл 1-2 раза в неделю.
У наиболее тяжелых больных применяются гемосорбция или плазмаферез, экстракорпоральное ультрафиолетовое облучение крови.
Для борьбы с гипоксемией показаны оксигенотерапия с использованием носовых катетеров, гипербарическая оксигенация.
Твердо установившимся принципом лечения острых легочных нагноений является антибактериальная терапия, которая проводится после бактериологического исследования содержимого бронхов с идентификацией возбудителей и их чувствительности к антибиотикам. Рекомендуются антибиотики широкого спектра действия: полусинтетические, аминогликозиды, тетрациклины, хинолоны.
Если возбудителем острого легочного нагноения являются нсклостридиальные анаэробы, рекомендуются: метронидазол (трихопол, флагил) внутрь в суточной дозе 1,5-2 г, курс лечения 8-10 дн; большие дозы пенициллина (20 000 000-50 000 000 ЕД/сут) внутривенно капельно в сочетании с метронидазол ом; линксшицин внутрь — 1-1,5 г/сут в 2-3 приема, а также внутримышечно или внутривенно — 1,4 г/сут в 2-3 приема.
При выявлении грамотрицательной микрофлоры назначаются препараты широкого спектра действия. Так, если этиологическим фактором является клебсиелла пневмонии, рекомендуется сочетание гентамицина или канамицина с левомицетином (2 г/сут) или же с препаратами тетрациклинового ряда. Для лечения инфекций, пытанных синегнойной палочкой, эффективен гсптамицин п сочетании с карбенициллином (4 г/сут внутримышечно при четырехкратном введении). В ряде случаев для подавления грамотрицательной флоры применяется доксициклин (0,1-0,2 г/сут внутрь однократно).
При деструкциях, вызванных стафилококком, назначаются полусинтетические пенициллины, устойчивые к действию пенициллиназы (метициллин, 4-6 г/сут, оксациллин, 3-8 г/сут), при четырехкратном введении внутримышечно или внутривенно; гентамицин (240-480 мг/сут) в сочетании с линкомицином (1,8 г/сут) при четырехкратном введении внутримышечно или внутривенно.
Если причиной острого легочного нагноения являются респираторные вирусы, назначаются интерферон местно в виде орошений слизистой оболочки носоглотки и бронхов, а также ингаляций в течение 5-15 дн; нормальные иммуноглобулины человека, рибонуклеаза и дезоксирибонуклеаза.
Развитие и исход легочного нагноения в значительной мере зависит от состояния дренирующих абсцесс бронхов, их вентиляционной и дренажной функции.
Естественное отделение продуктов распада легочной ткани через дренирующий бронх можно усилить внутривенным введением 10-20 мл 2,4 % раствора эуфиллина, приемом внутрь 2 % раствора калия йодида по столовой ложке несколько раз в день (или современных муколитиков — ацетилцистеина, бромгексина и др.), паровыми ингаляциями 2 % раствором гидрокарбоната натрия, постуральным дренажем 8-10 раз в сутки (в том числе и ночью). Эффективным лечебным мероприятием является бронхофиброскопия с активной эвакуацией мокроты из дренирующего бронха.
При подозрении на временную окклюзию бронха целесообразна санация с помощью жесткого бронхоскопа. В зону поражения под визуальным контролем вводятся различные растворы (фурагин, фурацилин, метилурацил и др.) в комбинации с протеолитическими ферментами (трипсином, химотрипсином и др.). В зависимости от вида микрофлоры и чувствительности к антибиотикам производится санация соответствующими антибактериальными препаратами с интервалом в 1-2 дн, иногда ежедневно, а по мере улучшения состояния и уменьшения интоксикации — через большие промежутки времени. Бронхоскопическая санация дополняется микротрахеостомией с введением гибкого катетера в бронхи пораженного легкого.
При значительных размерах абсцесса и кортикальной локализации гнойника эффективны трансторакальные пункции с целью аспирации гнойных масс с последующим введением антибиотика непосредственно в полость абсцесса.
В период разгара инфекционного процесса широко используются средства заместительной (пассивной) иммунотерапии. К ним относятся инфузии свежецитратной крови и плазмы, содержащих антитела, а также ряд факторов неспецифической защиты.
Широко используются противокоревой гамма-глобулин, антистафилокковый гамма-глобулин, а также иммуноглобулин с повышенным содержанием антител к синегнойной палочке, протею и другим грамотрицательным бактериям. Тяжелым больным показаны внутривенные вливания нормального человеческого гамма-глобулина (по 25-50 мл ежедневно или через день в течение 5-7 дн).
Определенное положительное действие оказывают иммуномодулирующие медикаментозные средства: нуклеинат натрия, левамизол, диуцифон, пентоксил и метилурацил, Т-активин и тималин.
При неэффективности консервативных мероприятий производится оперативное вмешательство (5-8 % больных). Показаниями к нему служат осложнения острых абсцессов легких: кровотечение или обильное прогрессирующее кровохарканье, пиопневмоторакс, эмпиема плевры, распространенная гангрена легкого, подозрение на опухоль. Хронические абсцессы легкого подлежат хирургическому лечению в тех случаях, когда при рентгенологически определяемой полости клинические проявления (постоянный кашель с гнойной мокротой, кровохарканье, лихорадка, склонность к простудам) сохраняются 3-6 мес после ликвидации острого периода. Обычно производится резекция пораженной доли и большей части легкого.
В фазе затухания и ремиссии воспалительного процесса, а также в послеоперационном периоде важное значение приобретают методы функциональной реабилитации (ЛФК, массаж, физиопроцедуры) и санаторно-курортное лечение.
БРОНХИАЛЬНАЯ АСТМА (БА) — это хроническое персистирующее воспалительное заболевание дыхательных путей (преимущественно бронхов) с их обратимой обструкцией, проявляющееся приступами удушья или астматическим статусом. Больных БА характеризует высокая реактивность (гиперреактивность) бронхов в ответ на действие различных раздражителей, которое у здоровых людей не вызывает бронхоспастической реакции.
В результате увеличения числа больных хроническими заболеваниями легких, аллергизации населения, загрязнения воздушной среды, широкого использования антибиотиков, вакцин, сывороток и т. д. отмечается рост заболеваемости бронхиальной астмой, которая порой становится причиной смерти. На распространенность и форму БА влияют климат и природные особенности региона. Заболеваемость БА составляет около 1 % всего взрослого населения, а в наиболее развитых странах — 7-8 %.
Этиология и патогенез. БА — этиологически и патогенетически неоднородное заболевание. Этиологические факторы БА схематично делятся на экзогенные и эндогенные. К наиболее распространенным экзогенным фактором относятся: 1) аллергизация населения (урбанизация); 2) загрязнение воздушной среды; 3) внедрение химии в сельское хозяйство, промышленность и быт; 4) широкое использование антибиотиков, вакцин, сывороток и др.; 5) климатические и природные особенности региона (например, холодный и сырой климат, обилие цветущих растений, запыленность и др.).
Эндогенными этиологическими факторами БА являются различные инфекционно-воспалительные заболевания органов дыхания (острая пневмония, острый и хронический бронхиты), врожденные или приобретенные дефекты и нарушения иммунной, эндокринной, нервно-психической, нейрогуморальной и других систем организма.
В основе БА могут быть различные специфические (иммунологические) и (или) неспецифические (неиммунологические), врожденные или приобретенные патогенетические механизмы. Основным проявлением БА являются в большей или меньшей степени выраженные приступообразные нарушения бронхиальной проходимости, т. е. обратимая (спонтанно или в результате лечения) бронхиальная обструкция. Восстановление проходимости бронхов при БА обусловлено тем, что основными патофизиологическими механизмами приступа удушья являются такие обратимые компоненты бронхиальной обструкции, как воспалительный отек слизистой оболочки, избыток слизи в бронхиальном дереве (гиперкриния) и спазм гладкой мускулатуры бронхов. Значительно меньшую роль в формировании бронхиальной обструкции при БА играют необратимые компоненты -гиперпластические и фиброзные изменения бронхов, экспираторный коллапс мелких бронхов, гипотоническая дискинезия трахеи и крупных бронхов с пролапсом мембранозной части на выдохе, которые появляются в случае сочетания БА с хроническим обструктивным бронхитом и эмфиземой легких.
У некоторых больных с тяжелым течением БА развивается стойкий, рефрактерный к обычной терапии бронхообтурационный синдром — астматический статус. Наиболее частыми причинами астматического статуса бывают острые инфекции и обострения хронических инфекций верхних дыхательных путей, бронхолегочного аппарата, вирусные заболевания, неоправданное уменьшение дозы или отмена глюкокортикостероидов, передозировка симпатомиметических средств, избыточное применение снотворных, седативных и антигистаминных препаратов, применение нсстсроидных противовоспалительных средств (аспирина, бруфена, метипдола), пиразолоновых препаратов, анальгина, ферментных муколитических средств (трипсина, химотрипсина), антибиотиков, сульфаниламидов.
Клиническая картина и диагноз. Клиническая картина БА разнообразна: от редких слабовыраженных проявлений до длительных и мучительных приступов удушья. Центральное место в клинической картине БА занимают астматические приступы. Они наступают обычно ночью, часто неожиданно, иногда после неясных предвестников в виде ощущения стеснения в груди, затрудненного дыхания.
В начале заболевания приступы удушья большей частью короткие — от нескольких минут до получаса; в дальнейшем они становятся более продолжительными, упорными, затягиваясь на целые сутки и переходящие иногда в астматический статус.
Часто во время приступа (обычно к концу) с кашлем выделяется небольшое количество слизистой, тягучей мокроты. В сероватых комочках ее иногда удается рассмотреть спирально закрученные завитки слизи (спирали Куршманна) и слепки мелких бронхов.
При всех клинико-патогенетических вариантах выделяются легкая, средняя и тяжелая степени БА. Легкое эпизодическое течение БА: • приступы удушья кратковременные и, возникают не чаще 1-2 раз в неделю;
• ночные симптомы не чаще 2 раз в месяц;
• в межприступном периоде самочувствие не нарушено;
• показатели функции внешнего дыхания — ПСВ или ОФВ, -не менее 80 % от должных;
• суточные колебания ПСВ или ОФВ не превышают 20 %;
• после ингаляции бронхолитика (при обострении) показатели ПСВ и ОФВ, возвращаются к нормальным значениям. Легкое персистирующее течение БА:
• приступы удушья чаще 2 раз в неделю, но не ежедневно;
• обострения (приступы) могут нарушать физическую активность и сон;
• ночные симптомы чаще 2 раз в месяц;
• показатели ПСВ или ОФВ не менее 80 % от должных;
• суточные колебания ПСВ 20-30 %. Среднетяжелое течение БА:
• необходимость ежедневного приема р 2 -агонистов короткого действия;
• ночные симптомы более 1 раза в неделю;
• обострения нарушают физическую активность и сон;
• ПСВ или ОФВ составляют 60-80 % от должных величин;
• суточные колебания ПСВ более 30 %. Тяжелое течение БА:
• симптомы постоянны с частыми обострениями;
• физическая активность ограничена;
• частые ночные симптомы;
• показатели ПСВ или ОФВ| менее 60 % от должных;
• суточные колебания ПСВ более 30 %. Ни один признак в отдельности не позволяет точно оценить степень тяжести БА, только комбинированная оценка симптомов и показателей ФВД позволяет отнести заболевание к определенной степени тяжести. Наличие даже одного показателя, относящегося к более тяжелому варианту течения болезни, достаточно для того, чтобы расценить течение болезни как более тяжелое.
Степень тяжести БА у одного больного может изменяться как в сторону возрастания, так и в сторону убывания при адекватно подобранной и применяемой терапии. Поэтому не говорят о стадии заболевания (это правомочно для неуклонно прогрессирующих болезней), а указывают фазу: обострения или ремиссии (стабилизации).
У пациентов с любой степенью тяжести (даже легкой) могут развиваться тяжелые и даже угрожающие жизни обострения.
Общепринятой этиологической классификации бронхиальной астмы до настоящего времени не существует из-за разнообразия причин, ее вызывающих, и нередкого комбинированного воздействия разных факторов.
Выделяются следующие основные формы болезни: аллергическая, неаллергическая и смешанная. В основе аллергической БА лежит иммунологический механизм с избыточной продукцией IgE. Это приводит к массированному выбросу медиаторов тучной клеткой при всяком контакте больного с “виновным” аллергеном. Аллергическая БА чаще возникает у людей с отягощенным семейным или персональным аллергологическим анамнезом, начинается обычно в детском возрасте, у таких больных — положительные кожные и провокационные пробы с неинфекционными аллергенами, повышен уровень общего и специфического IgE, имеются другие аллергические проявления (аллергический ринит, конъюнктивит, атонический дерматит).
При неаллергической бронхиальной астме не удается выявить сенсибилизации к определенному аллергену. Начало болезни приходится на более зрелый возраст, и пусковым фактором, а также “виновником” обострения чаще всего является перенесенная респираторная вирусная инфекция. Спустя несколько дней после начала вирусного заболевания появляются одышка, кашель, приступы удушья, которые могут сохраняться от нескольких дней до нескольких месяцев.
Пациенты, болезнь которых имеет признаки аллергической и неаллергической астмы, относятся к группе смешанной формы БА.
Достоверная диагностика БА возможна только путем исключения вторичного бронхоспастического синдрома (БС). Вторичный БС наиболее часто встречается при заболеваниях гетероаллергического генеза (анафилактический шок. сывороточная болезнь), аутоиммунных болезнях (системная красная волчанка, пневмокониозы), инфекционно-воспалительных заболеваниях бронхолегочного аппарата (бронхит, пневмония, туберкулез), обтурационных патологических процессах (злокачественные и доброкачественные опухоли, бронхостенозы вследствие туберкулеза, ожога дыхательных путей), заболеваниях и патологических состояниях, которые вызывают рефлекторную гиперкинезию бронхов (истерия, механическое раздражение блуждающего нерва, передозировка вагостимуляторов, например р-адреноблокаторов, интратрахеальный наркоз), заболеваниях системы кровообращения, обусловливающих гемодинамические нарушения в бронхолегочном аппарате (первичная лет очно-артериальная гипертензия, тромбоэмболия легочной артерии, застойная левожелудочковая недостаточность), и др.
Лечение. Общая программа лечения больного БА должна включать в себя: 1) образовательную программу; 2) оценку и мониторинг степени тяжести болезни; 3) исключение факторов, провоцирующих обострение болезни, или контроль над ними; 4) разработку индивидуальной схемы медикаментозного лечения; 5) разработку плана лечения обострения болезни, неотложную терапию при приступе удушья и (или) астматическом статусе; 6) диспансерное наблюдение.
Общеобразовательная программа предполагает санитарное образование больного БА: он овладевает методами профилактики БА, которые значительно повышают качество его жизни, оценивает и записывает в дневник основные симптомы своего заболевания, проводит индивидуальный контроль за пиковой скоростью выдоха с помощью портативного пикфлоуметра. Обнаруженные им изменения в течении болезни позволяют своевременно обратиться к врачу.
Успешное лечение больных БА во многом зависит от своевременного устранения контакта с аллергенами или снижения их влияния. Элиминация аллергена достаточно эффективна в контроле степени тяжести болезни.
Индивидуальная схема медикаментозного лечения определяется в первую очередь степенью тяжести БА. Назначение медикаментов проводится в виде четырех ступеней с возрастающим бронходилатирующим и противовоспалительным эффектом. Ступень лечения соответствует степени тяжести БА: первая — легкой степени БА, вторая и (или) третья — средней тяжести БА, четвертая — тяжелой степени БА.
Основу базисной противовоспалительной терапии составляют нестероидные противовоспалительные средства (кромогликат и недокромил натрия) и ингаляционные кортикостероиды. Кромогликат и недокромил натрия применяются при легкой и некоторых формах среднетяжелой астмы.
Ступень 1. Легкое эпизодическое течение заболевания. На этой ступени нет необходимости в назначении базисной противовоспалительной терапии и лечение складывается из элиминационных мероприятий (избегать воздействия триггеров) и купирования приступов с помощью (5 2 -агонистов короткого действия.
Возможно профилактическое применение р 2 -агонистов или кромогликата натрия перед физической нагрузкой или воздействием других провоцирующих факторов. Обучение больного на этом этапе должно складываться из:
• основных сведений об астме;
• правил пользования ингачятором (спейсером); объяснения роли препаратов;
• разработки плана самонаблюдения;
• разработки плана действий при обострении; • обсуждения мер по контролю за факторами внешней среды (аллергенами и другими триггерами). Ступень 2. Легкое персистирующее течение БА. Такое состояние требует проведения постоянной противовоспалительной терапии, иначе болезнь будет прогрессировать. Начинается базисное лечение с кромогликата или недокромила (особенно в молодом возрасте) натрия. При недостаточном эффекте следует перейти на ингаляционные глюкокортикостероиды в низких дозах или комбинировать их с кромолинами. Альтернативой этим препаратам на данной ступени могут быть теофиллин пролонгированного действия (сывороточная концентрация 5-15 мкг/мл) или антилейкотриеновые препараты (зафирлукаст, зилеутон).
Для купирования приступов удушья рекомендуются р 2 -агонисты короткого действия. Частый их прием (ежедневно) указывает на необходимость усиления базисной терапии.
В программу обучения включаются все вопросы 1-й ступени, а также: • обучение самоконтролю;
• периодический пересмотр и обновление плана лечения;
• направление в астма-школу. Ступень 3. Среднетяжелое течение БА. Противовоспалительная базисная терапия у этих больных включает ингаляционные глюкокортикостероиды в средних дозах или комбинацию низких доз этих препаратов с р 2 -агонистами длительного действия (ингаляционными или пероральными). Возможна замена р 2 -агонистов длительного действия пролонгированным теофиллином. В качестве альтернативы могут быть использованы антихолинергические препараты (ипратропий бромид) или их комбинация с Р 2 -агонистом, особенно при плохой переносимости р 2 -агонисгов или сопутствующем хроническом обструктипном бронхите, а также у пожилых.
Недостаточный эффект проводимой базисной противовоспалительной терапии может потребовать на этой ступени применения и высоких доз ингаляционных глюкокортикоидов.
Для купирования приступов используются ингаляционные Р 2 -агонисты, но не чаще 3-4 раз в сутки (угроза передозировки).
В программу обучения больных на этой ступени включаются вопросы 1-2-й ступеней с периодическим пересмотром и обновлением плана самонаблюдения и лечения.
Ступень 4. Тяжелое течение БА. Противовоспалительная терапия складывается из:
• регулярного применения ингаляционных глюкокортикоидов в высоких дозах;
• длительного приема кортикостероидов внутрь (обычно не более 60 мг преднизолона в день);
• приема длительно действующих бронходилататоров (р 2 -агонисты длительного действия или пролонгированный теофиллин). При выраженных побочных реакциях на эти бронходилататоры возможна замена их или комбинация с холинолитиками (ипратропий бромид).
В качестве симптоматического средства для купирования приступов используются р 2 -агонисты короткого действия, но не более 3-4 раз в сутки (возможность передозировки). При необходимости более частого приема р 2 -агонистов требуется контроль базисной противовоспалительной терапии.
В обучении больных этой группы основное место занимает информация, предусмотренная на 1, 2 и 3-й ступенях.
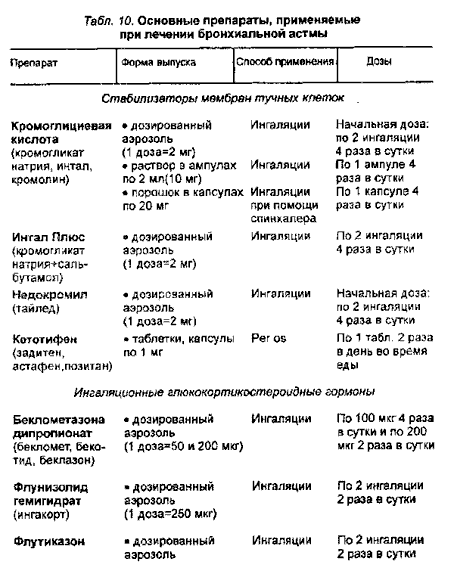




Так, дополнительная лечебная программа у больных с атоническим вариантом БА включает в себя раннее выявление аллергена (атопена) с целью его элиминации или проведения курсов специфической иммунотерапии; применение экстракорпоратъных методов терапии.
Элиминационная терапия проводится совместно с врачом-аллергологом, специфическая гипосенсибилизация (введение подкожно в нарастающих дозах аллергенов неинфекционного происхождения) — в аллергологическом кабинете. Специфическая иммунотерапия у больных с БА среднетяжелого и тяжелого течения, как правило, малоэффективна. Экстракорпоральные методы терапии (плазмаферез, гемосорбция, плазмофильтрация и др.) позволяют быстро прекратить очередное обострение БА, улучшить переносимость медикаментозного лечения и добиться хороших результатов с помощью меньших доз лекарственных препаратов.
Дополнительная лечебная программа при инфекционно зависимом варианте аллергической астмы включает в себя проведение иммунотерапии, направленной на повышение резистентности организма к инфекциям дыхательных путей, а также использование некоторых современных противовирусных и иммуномодулирующих средств. К последним относятся Т-активин, в меньшей степени тималин, декарис, при некоторых формах иногда помогают интерферон, препараты группы иммуноглобулинов. Целесообразно проведение иммунотерапии гетерогенными бактериальными вакцинами или мукополисахаридными комплексами, продуктами жизнедеятельности бактерий (пирогенал, продигиозан).
В острой фазе заболевания необходимо ликвидировать воспалительный процесс в органах дыхания. С этой целью назначаются антибиотики, сульфаниламиды, фитонциды, а также салицилаты и другие нестероидные противовоспалительные препараты.
При развитии дисгормональных расстройств лечение проводится совместно с врачом-эндокринологом. Больным с преобладанием глюкокортикоидной недостаточности коры надпочечников назначается этимизол, производится санация очагов хронической инфекции, повышается неспецифическая резистентность организма.
При вненадпочечниковой недостаточности, обусловленной слабой стимуляцией стероидогенеза адренокортикотропным гормоном, применяются кортикотропин или синактен. Для возбуждения адренокортикотропной функции гипофиза и повышения уровня глюкокортикостероидов в крови можно использовать этимизол.
При нервно-психических нарушениях в схему дополнительного лечения включаются психотерапия, психотропные и седативные средства, электросон, вагосимпатические и паравертебральные новокаиновые блокады по методу Сперанского.
Дополнительная лечебная программа при нсаллсргической аспириновой астме состоит из элиминационной диеты и десентизации небольшими дозами аспирина. При проведении элиминационной диеты исключаются продукты, содержащие большое количество дериватов салициловой кислоты (консерванты, томаты, молодой картофель, цитрусовые и др.). Хорошего лечебного эффекта удается достичь с помощью десентизации аспирином. Начальная доза аспирина не превышает 5-6 мг, в последующем постепенно увеличивается.
При астме от физического усилия в дополнительную лечебную программу включаются физические тренировки и назначаются антагонисты кальция (нифедипин, коринфар и др.). Следует отметить, что глкжокортикостероидные гормоны при этом варианте БА абсолютно неэффективны.
Немаловажное значение в комплексной терапии больных БА имеет симптоматическое лечение. Так, для улучшения дренажной функции бронхиального дерева и уменьшения вязкости мокроты используются отхаркивающие средства. Рекомендуются секретолитические препараты, которые действуют непосредственно на слизистую оболочку бронхов (эфирные масла, йодиды, натрия гидрокарбонат и др.); секретомоторные препараты (рефлекторно — через желудок и рвотный центр — усиливают бронхиальную секрецию: настой термопсиса, алтейного корня, листьев мать-и-мачехи, подорожника) и муколитики (трипсин, химопсин, рибонуклеаза, мукалтин, бромгексин, бисольвон и др.). Калия йодид является наиболее сильным отхаркивающим средством, назначается по 1 ст. ложке 3 % раствора 5-6 раз в день после еды, не более 5 дн подряд. Настой термопсиса — 0,8-1 г на 200 мл воды — назначается до еды по 1 ст. ложке 5-6 раз в день. Хороший эффект наблюдается от ультразвуковых ингаляций трипсина, химопсина и других ферментов.
Для улучшения насыщения артериальной крови кислородом используется оксигенотерапия. Больной дышит 24-28 % кислородно-воздушной смесью через нос с помощью Т-образной трубки.
Эффективными немедикаментозными методами симптоматического лечения больных с БА являются дыхательная гимнастика, массаж грудной клетки, постуральный дренаж, иглорефлексотерапия. Дыхательная гимнастика включает такие упражнения, как потягивание, маховые движения руками (“колка дров”), причем при разведении или подъеме рук следует делать максимально глубокий вдох, а при опускании рук — форсированный глубокий выдох. В некоторых случаях применяются поверхностное дыхание по Бутейко, парадоксальная дыхательная гимнастика по Стрельниковой (вдох делают при наклоне корпуса вперед, выдох — при разгибании). Широко используются небуляторы — приборы, создающие сопротивление дыханию.
Удаление мокроты существенно усиливается с помощью постурального (позиционного) дренажа.
При некупирующемся приступе удушья в условиях реанимационного отделения применяются плазмаферез, лечебная бронхоскопия, искусственная вентиляция легких (управляемое дыхание).
Неотложная помощь при приступах удушья и астматическом статусе. Легкий приступ удушья может быть купирован приемом внутрь таблеток эуфиллина, теофедрина или антастмана, но-шпы, папаверина или галидора, 30-60 капель солутана. Могут быть эффективны отвлекающие мероприятия (беседа с больным, горячая ножная ванна, горчичники или банки на спину). Иногда для купирования приступа достаточно одной ингаляции производных адреналина — изопреналина (новодрина, эуспирана), орципреналина (астмопента, алупента), гексапреналина (ипрадола), вентолина (сальбутамола), беротека (фенотерола).
Среднетяжелый приступ удушья купируется в большинстве случаев 0,1 % раствором адреналина, вводимым в дозе 0,5-1 мл подкожно или в виде аэрозоля. Действие адреналина наступает через 2-3 мин и продолжается около 1 ч, поэтому некоторым больным необходимо вводить его повторно (до 10 раз в сутки). Для сохранения бронхоспазмолитического действия одновременно с адреналином целесообразно вводить 5 % раствор эфедрина в дозе 0,5-1 мл подкожно или внутримышечно; действие его наступает позже и продолжается несколько часов. Введенный одновременно с адреналином, эфедрин усиливает и продлевает действие адреналина. При наличии противопоказаний к введению адреналина (повышенная чувствительность), при гипертонической болезни и ИБС можно применять некоторые его производные — орципреналин (алупент), гексапреналин (ипрадол), вентолин (сальбутамол), беротек (фенотерол). Они почти не повышают АД, оказывают минимальное побочное влияние на миокард и сосуды, поскольку практически не возбуждают их адренергические рецепторы. Алупент применяется в виде инъекций (0,5 мг), аэрозоля (2 % и 5 % растворы, до 1 мг). Современные бронхоспазмолитики (беротек, вентолин) используются в виде аэрозоля. Ипрадол вводится в вену в дозе 5-10 мкг (1-2 ампулы).
При отсутствии эффекта от адреналина и его производных применяется эуфиллин (аминофиллин, диафиллин) в виде 2,4 % раствора, по 10 мл внутривенно медленно. При побочных воздействиях эуфиллина (тошноте, рвоте, болях в сердце) одновременно используются растворы: 2 % — папаверина, 2 мл, 2 % -ношпы, 2 мл, 1 % — дибазола, 4-6 мл. При ночных приступах удушья и брадикардии можно значительно улучшить состояние больного подкожным введением 1 мл 0,2 % раствора платифиллина или 0,5-1 мл 0,1 % раствора атропина, у некоторых больных, особенно при болевом синдроме, хороший эффект дает вдыхание закиси азота в смеси с кислородом при помощи аппарата для газового наркоза. Если у больных наблюдаются различные сопутствующие аллергические проявления, показано внутримышечное или внутривенное введение растворов димедрола, супрастина или пипольфена.
При тяжелом приступе удушья, не поддающемся вышеуказанной терапии и угрожающем перейти в гиперкапническую кому, необходимо вызвать специализированную бригаду скорой медицинской помощи. На догоспитальном этапе больному следует ввести внутривенно адреналин, эуфиллин в обычной дозировке, алупент — 0,5 мг в 1 мл раствора натрия хлорида медленно в течение 5 мин или 5-20 мг в 250 мг 5 % раствора глюкозы со скоростью 10-15 капель в минуту, ипрадол — 1-2 ампулы внутривенно в течение 5 мин. Наряду с этим внутривенно вводятся глюкокортикоидные гормоны — преднизолон, 30-60 мг, или гидрокортизон, 100-250 мг, на 250-500 мл 5 % раствора глюкозы.
Астматический статус (АС) является тяжелейшим осложнением БА. Он представляет собой острую дыхательную недостаточность вследствие обструкции дыхательных путей, резистентной к терапии симпатомиметиками и эуфиллином.
Неотложная помощь при АС состоит из трех обязательных компонентов: кислородотерапии, инфузионной и медикаментозной (эуфиллин и его аналоги, глюкокортикостероидные гормоны) терапии.
Кислородотерапия проводится в форме непрерывной инсуфляции кислородно-воздушной смеси с относительно небольшим содержанием кислорода (30-40 %); инфузионная терапия — гепаринизированным раствором 5 % глюкозы, раствором Рингера, полиглюкином, реополиглюкином. Общий объем инфузионной терапии — 3-3,5 л в 1-е сутки, в последующие — из расчета 1,6 л/м 2 поверхности тела.
Медикаментозное лечение АС проводится при максимально суженном круге препаратов, в том числе при полном отказе от адреностимуляторов. Внутривенно вводятся 15 мл 2,4 % раствора эуфиллина на изотоническом растворе глюкозы или хлорида натрия в течение 4-6 мин вместе с 5000 ЕД гепарина. Суточная доза эуфиллина — 1,5-2 г. Преднизолон вводится внутривенно: от 30 до 90 мг.
При декомпенсации наряду с вышеуказанными мерами проводится лечебная бронхоскопия с посегментарным лаважем бронхов, больной переводится на искусственную вентиляцию легких.
Во время ремиссии БА большое внимание должно быть обращено на немедикаментозное лечение: гипоаллергенную диету, лечебную физкультуру, плавание, массаж, физиотерапию, санаторно-курортное лечение (Южный берег Крыма, Кисловодск, высокогорные районы Приэльбрусья и др.).
БРОНХОЭКТАЗИЯ — патологический необратимый бронхолегочный процесс, характеризующийся образованием бронхоэктазов преимущественно в мелких и средних бронхах с развитием в них периодически обостряющегося хронического гнойного воспаления и эндобронхиального нагноения их содержимого.
Патогенез. Бронхоэктазы — эторегионарноерасширение бронхов, превышающее просвет неизмененного бронха в два и более раза, и их деформация.
По анатомической форме бронхоэктазы делятся на цилиндрические, мешотчатые, смешанные, кистевидные, веретенообразные и варикозные. Все формы, за исключением смешанной, полностью соответствуют своему названию. Смешанные бронхоэктазы в своей начальной части имеют цилиндрическую форму, а в концевой — мешотчатую, напоминающую колбу.
Принципиальное клиническое значение имеет деление бронхоэктазии на первичную, или бронхоэктатическую болезнь, и вторичную.
Бронхоэктатическая болезнь (БЭБ) — это самостоятельная полиэтиологическая форма хронических неспецифических заболеваний легких, которая в большинстве случаев возникает в детском и юношеском возрасте, характеризуется образованием инфицированных бронхоэктазов без стойких причинно-следственных связей с хроническими болезнями органов дыхания.
Характерной патогенетической особенностью БЭБ является относительная изолированность инфицированных бронхоэктазов от анатомически связанных с ними участков легочной паренхимы.
Вторичная бронхоэктазия (ВБЭ) — это одна из форм осложнений различных хронических заболеваний органов дыхания, которая п большинстве случаев развивается в зрелом возрасте и характеризуется образованием инфицированных бронхоэктазов. Характерной патогенетической особенностью ВБЭ является тесная связь гнойного процесса в расширенных бронхах с респираторными отделами. Наиболее частые причины ВБЭ — хронический гнойный обструктивный бронхит, абсцессы легких, туберкулезное и сифилитическое поражение легких, центральный рак, инородные тела, плевриты и т.д. ВБЭ, являясь осложнением заболеваний и патологических состояний органов дыхания, иногда бывает их основной клинической “маской”.
Распространенность БЭБ колеблется, по данным разных авторов, от 0,45 до 1,2 %, а БЭБ и ВБЭ вместе составляют 12-33 % всех случаев хронических заболеваний легких. Значительно чаще болеют лица мужского пола (соотношение 3:1). Большинство случаев бронхоэктазий выявляются у больных в возрасте до 5 и 40-60 лет.
В образовании бронхоэктазов в первую очередь играют роль врожденные и приобретенные нарушения в стенке бронхов. Кроме того, большое значение имеют патологические процессы в перибронхиальной ткани, паренхиме легких и плевре, приводящие к стойкому растяжению стенок бронхов, а также “бронхо-дилатирующие силы” — повышение эндобронхиального давления при кашле, растяжение стенок бронхов скапливающейся мокротой (секретом) и др.
В основе БЭБ лежит врожденная и (или) первично приобретенная неполноценность структуры и функции бронхиальной стенки, при этом врожденные (генетические) факторы являются главными, а приобретенные — разрешающими.
Клиническая картина и диагноз. Клиническая картина бронхоэктазий представлена главным образом симптомокомплексами воздушной полости в легких (продуктивный кашель, кровохарканье), хронической эндогенной интоксикации (повышение температуры тела, потливость, слабость, анорексия, анемия, истощение) и иммунной недостаточности (частые рецидивирующие бронхопневмонии, хронические инфекции верхних дыхательных путей, внелегочные инфекционные осложнения) в зависимости от характера бронхоэктазов (БЭБ или ВБЭ), их локализации, распространенности, фазы течения и т. п.
Клиника основного заболевания дополняется симптомокомплексами бронхиальной обструкции, гипертензии малого круга кровообращения, хронической дыхательной и хронической сердечной недостаточности.
Изменения в общем анализе крови — лейкоцитоз, нейтрофилез, увеличение СОЭ — обычно связаны с фазой обострения БЭБ. При нарастающей интоксикации в периферической крови появляются признаки анемии, а в моче — протеинурии. Стойкое наличие белка в моче может свидетельствовать о поражении почек.
Выраженность воспалительной реакции в легких подтверждается биохимическими показателями острой фазы воспаления (“острофазовые” показатели) — диспротеинемией (снижение содержания альбуминов, увеличение альфа-2-пюбулинов и гамма-глобулинов), увеличением количества сиаловых кислот, фибрина, серомукоида, гаптоглобина. Следует отнестись настороженно к выраженной гипоальбуминемии, которая может быть ранним признаком амилоидоза печени.
В мокроте обнаруживается большое количество нейтрофилов эластических волокон, могут быть эритроциты.
Важным этапом осбледования больных БЭБ является изучение микрофлоры мокроты.
Рентгенологическая картина БЭБ зависит от степени поражения бронхиального дерева и легочной паренхимы, а также распространенности процесса. В начале БЭБ рентгенограмма легких отображает лишь деформацию легочного рисунка. Позднее появляются разнообразные изменения, вплоть до множественных гидровоздушных полостей в легких.
Более информативна томография легких, выполненная в соответствующих проекциях и на разной глубине, при которой четко выявляется сотовый рисунок поражения.
Решающим методом, подтверждающим наличие и уточняющим локализацию бронхоэктазий, является бронхография с полным контрастированием обоих легких.
Бронхоскопия при БЭБ выявляет различные изменения слизистой оболочки бронхов — атрофические, гипертрофические, отечно-гиперемийные, а также гной в их просвете.
Лечение. При лечении конкретного больного с бронхоэктазией первоначально необходимо определить основной метод лечения — хирургический или консервативный. Хирургическое лечение показано при ограниченных в пределах отдельных сегментов или даже долей легкого бронхоэктазах без выраженного хронического обструктивного бронхита.
Консервативное лечение проводится при начальных формах болезни и иноперабельных двусторонних процессах. Оно обязательно при подготовке больных к бронхологическим исследованиям и оперативному лечению. Консервативное лечение заключается в определенном лечебном режиме, полноценном, богатом белками питании, эффективном дренаже бронхов, воздействии на гноеродную микрофлору, повышении общей реактивности организма, санации верхних дыхательных путей и придаточных пазух носа, ЛФК и массаже, физиотерапевтическом и санаторно-курортном лечении.
В фазе обострения эндобронхиального нагноительного процесса проводится антибактериальная терапия, при этом следует учитывать микрофлору выделяемой мокроты. Из антибиотиков обычно используются пенициллин и полусинтетические препараты группы пенициллина, тетрациклины и цефалоспорины в терапевтических дозах. Для эндобронхиального введения с успехом применяются производные хиноксалина (10 мл 1 % раствора диоксидина), производные нитрофурана (фурацилин, фурагин) и антисептические средства природного происхождения (хлорофиллипт).
В последние годы арсенал антимикробных средств пополнился фторхинолонами: офлоксацином (таривидом), ципрофлоксацином (ципробаем, ципринолом), пефлоксацином (абакталом), ломефлоксацином (максаквином). Они обладают высокой бактерицидной активностью в отношении большинства патогенных микроорганизмов, в том числе и тех штаммов, которые выработали устойчивость к основным противоинфекционным средствам. Нередко эту группу противомикробных средств называют синтетическими антибиотиками. Офлоксацин (таривид) обладает бактерицидным действием на грамотрицательные и грамположительные возбудители. Назначается внутрь по 200 мг 2 раза в сутки. Курс лечения 3-10 дн. Ципрофлоксацин назначается внутрь по 250-500 мг или внутривенно по 200 мг 2 раза в сутки. Пефлоксацин назначается внутрь и парентерально по 400 мг 2 раза в сутки. Ломефлоксацин действует бактерицидно на большинство патогенных грамотрицательных возбудителей, а также на ряд грам-положительных бактерий (стрептококки), быстро всасывается при приеме внутрь и накапливается в слизистой оболочке бронхов, легочной ткани и бронхиальном секрете. Назначается по 400 мг (1 табл.) 1 раз в сутки, курс лечения 7-10 дн.
При необходимости больным назначаются средства, повышающие общую реактивность организма (метилурацил по 0,5 г 3 раза в день на протяжении 1-2 мес, неробол, переливание альбумина, интралипида и др.), применяются иммуномодуляторы (левамизол по 50-75 мг 2 раза в день 2 дн подряд еженедельно в течение 1-2 мес).
С участием отоларинголога больным необходимо тщательно санировать верхние дыхательные пути. Показано физиотерапевтическое лечение (электрическое поле УВЧ, микроволновая терапия). В теплые и сухие месяцы года при отсутствии выраженного обострения эндобронхиального воспалительного процесса желательно проводить санаторно-курортное лечение (Южный берег Крыма, юг Украины и Беларуси).
ОСТРЫЙ БРОНХИТ (ОБ, ТРАХЕОБРОНХИТ, БРОНХИТ С ПРЕИМУЩЕСТВЕННЫМ ПОРАЖЕНИЕМ БРОНХОВ СРЕДНЕГО КАЛИБРА, БРОНХИОЛИТ) — это воспалительный процесс в трахее, бронхах или бронхиолах, характеризующийся острым течением и диффузным обратимым поражением преимущественно слизистой оболочки. Обычно воспалительный процесс купируется в течение нескольких недель, а пораженная слизистая оболочка дыхательных путей полностью восстанавливается .
Острый бронхит является чаще всего одним из клинических этапов ОРЗ (острых респираторных заболеваний), значительно реже — самостоятельным заболеванием.
По происхождению ОБ может быть первичным и вторичным. Последний нередко возникает на фоне инфекционных заболеваний (кори, коклюша, брюшного тифа, острой пневмонии и др.) или острых нарушений кровообращения и обмена веществ (уремии, желтухи и др.).
В большинстве случаев ОБ — это инфекционное заболевание.
Инфицирование бронхов происходит аэрогенно, бронхогенно или гематогенно.
В развитии ОБ выделяются две фазы: 1) реактивно-гиперемическая, или нервно-рефлекторная; 2) инфекционная.
Клиническая картина и диагноз. ОБ может развиться в течение нескольких часов, но симптомы могут нарастать и постепенно, в течение нескольких дней (3-4 дн). Если ОБ является следствием ОРЗ, то ему предшествуют насморк (ринит), першение и боли в горле при глотании (фарингит, ангина), охриплость голоса (ларингит), жжение, саднение или “царапанье” за грудиной (трахеит). Больные жалуются в это время на недомогание — общую слабость, разбитость, ухудшение аппетита, мышечные боли в спине и конечностях, познабливание.
Клиническая картина ОБ состоит главным образом из симптомов раздражения чувствительных нервных окончаний в слизистой оболочке трахеи и крупных бронхов (упорный кашель и преходящие явления бронхоспазма), бронхиальной обструкции при распространении воспалительного процесса на мелкие бронхи и бронхиолы (одышка и цианоз), эндогенной интоксикации (слабость, потливость, повышение температуры и др.).
Различаются несколько вариантов течения ОБ: 1) остротекущий (обычно не более 2 нед); 2) затяжной (до месяца и более); 3) рецидивирующий (до 3 и более раз в течение года). Средняя продолжительность неосложненного ОБ составляет 7-14 дн.
Картина периферической крови в легких случаях ОБ — в пределах нормы, при более выраженных явлениях воспаления и интоксикации определяются нейтрофильный лейкоцитоз и повышенная СОЭ.
Рентгенологическое исследование: рентгенограмма грудной клетки чаще всего без изменений, в тяжелых случаях могут выявляться расширение и нечеткость корней легких, усиление легочного рисунка, бол’ьше в нижних отделах.
Спирография (пневмотахометрия): при явлениях бронхиальной обструкции снижаются скоростные показатели легочной вентиляции.
ОБ дифференцируют в первую очередь с бронхопневмонией, остро начинающимся туберкулезом легких, инфекционными заболеваниями, при которых ОБ является их составной частью (корь, коклюш, паратиф А, краснуха и др.).
Лечение. Поскольку ОБ в большинстве случаев является инфекционным заболеванием, чаще всего осложняющим ОРВИ верхних дыхательных путей, то больной по возможности должен находиться в изолированной светлой, хорошо проветриваемой, но с нехолодным воздухом комнате. На весь период болезни категорически запрещается курение табака. При повышенной температуре тела следует соблюдать постельный режим. Легкие и среднетяжелые необструктивные формы ОБ лечатся на дому. В госпитализации нуждаются больные с обструктивным острым бронхитом и бронхиолитом с тяжелой интоксикацией, сопутствующей легочной и сердечно-сосудистой патологией.
Пища должна быть легкоусвояемой, достаточно калорийной и витаминизированной, в первую очередь витаминами С и А. Если у больного нет признаков сердечной или почечной недостаточности, то с самого начала болезни ему рекомендуется обильное питье горячего чая с лимоном и медом, подогретых щелочных минеральных вод (боржоми, Славяновская, Смирновская, Березовская, Поляна Квасова и др.), горячего молока пополам с теплым боржоми или щепоткой питьевой соды.
Если тяжелый острый бронхит вызван вирусной инфекцией (в том числе вирусно-бактериальной ассоциацией), в схему комплексного этиотропного лечения включается активная противовирусная терапия: противогриппозный или противокоревой гамма-глобулин по одной дозе 1-2 раза в день инъекционно, одновременно одна доза вводится в виде ингаляций и одна в виде орошения дыхательных путей (всего 3-5 доз за сутки в период лихорадки); лейкоцитарный интерферон назначается в виде орошений слизистой оболочки носа и глотки (одна ампула в день), введения в гортань и интратрахеальных вливаний (одна ампула), а также ингаляций (одна ампула). При наличии в бронхах трудноотделимой тягучей, вязкой слизи местной противовирусной терапии должны предшествовать 3-5 интратрахеальных вливаний 5 % раствора аскорбиновой кислоты (2-3 мл на физиологическом растворе).
Для правильного выбора антибиотика при остром бактериальном или вирусно-бактериальном гнойном бронхите необходимо выяснить этиологический фактор. Поскольку возбудителями острого бактериального бронхита чаще бывают пневмококк и другая кокковая флора, целесообразно вначале использовать оксациллин (2-4 г/сут парентерально), ампициллин, пенициллин (3-6 млн ЕД/сут), бактрим или бисептол (триметоприм/ сульфаметоксазол) по 2 табл. в день, сульфален — 1 г в день с последующим снижением дозы.
Лечение антибиотиками и сульфаниламидами сочетается с приемом внутрь фурагина и интратрахеальными заливками фурагина, фурацилина и диоксидина.
При выраженном воспалительном процессе следует назначать нестероидные противовоспалительные препараты (ацетилсалициловую кислоту по 0,5 г 3-4 раза в день после еды, индометацин (метиндол) по 0,025 г 3 раза в день после еды).
При сухом (непродуктивном) мучительном кашле в первые дни заболевания можно применять противокашлевые наркотические (кодеин, кодтерпин, дионин) и ненаркотические (либексин, глауцина гидрохлорид, глаувент, балтикс, пакселадин и др.) средства. Если воспалительный процесс локализуется главным образом в трахее, то кашель можно уменьшить щелочными (минеральной щелочной водой, 2 % раствором натрия бикарбоната) или паровыми ингаляциями, что содействует разжижению слизи и ее более легкому отделению.
Всем больным с острым бронхитом показаны безаппаратная физиотерапия (особенно при болезненных ощущениях за грудиной), горчичники или перцовый пластырь, парафиновые или грязевые аппликации на область грудины и межлопаточные пространства, круговые банки, согревающие спиртовые компрессы и растирание скипидарной мазью грудной клетки, горчичные ножные ванны.
При катаральном остром бронхите эффективным способом восстановления нарушенного кровообращения в слизистой оболочке дыхательных путей являются ежедневное ультрафиолетовое облучение грудной клетки одной биодозой площадью 400-600 см, диатермия или индуктотермия на межлопаточную область, электрофорез кальция на грудную клетку, массаж грудной клетки.
В периоде выздоровления всем больным рекомендуются звуковая и дыхательная гимнастика, лечебная физкультура.
КРОВОХАРКАНbЕ И ЛЕГОЧНОЕ КРОВОТЕЧЕНИЕ —грозные неспецифические симптомы различных заболеваний бронхов, легких и сердца.
Патогенез. Кровохарканье и легочное кровотечение -наиболее частые осложнения заболеваний легких, существенно отягощающие состояние больных, а у 5-15 % они становятся причиной летального исхода. Чаще встречаются у больных зрелого возраста (в большинстве случаев средний возраст 50-55 лет).
Наиболее распространенными причинами кровохарканья и легочного кровотечения являются бронхоэктазия, бронхит, абсцесс легкого, туберкулез, пневмония, новообразования (рак легкого, аденома бронха), заболевания сердца и сосудов (митральный стеноз, тромбоэмболия легочной артерии, пороки развития сосудов легких), аутоиммунные нарушения (гранулематоз Вегенера, синдром Гудпасчера), геморрагические диатезы.
Самой частой причиной кровохарканья среди заболеваний легких нетуберкулезного происхождения следует считать бронхоэктазию.
Клиническая картина и диагноз. Кровохарканье — выделение мокроты с кровью в виде прожилок и точечных вкраплений. Мокрота может быть равномерно окрашена в розово-красный цвет (вид малинового желе), она может быть кровянисто-пенистой, ржавого или желто-коричневого цвета.
Кровохарканье в большинстве случаев вызывается диапедезным выходом эритроцитов из кровеносного русла при возрастании давления в сосуде на фоне повышения проницаемости его стенки или паренхиматозным кровотечением (мелкими кровоизлияниями) при разрыве капилляров.
Легочное кровотечение — выделение (откашливание) чистой, алой, пенистой крови в количестве 5-50 мл и больше. Различаются малые (до 100 мл), средние (до 500 .мл) и большие, профузные (более 500 мл) легочные кровотечения. Легочное кровотечение обычно обусловлено наличием деструктивных процессов в легочной паренхиме, сопровождающихся изъязвлением или разрывом кровеносных сосудов в системе легочной артерии или большого круга кровообращения.
Обильное легочное кровотечение приводит к острой анемии и гиповолемическому шоку. В то же время кровь, попадая в бронхи здоровых отделов легких, закупоривает их и вызывает развитие обтурационных ателектазов. Вследствие уменьшения объема функционирующей легочной ткани и нарушения соотношения между вентиляцией и кровотоком эти ателектазы приводят к тяжелой прогрессирующей дыхательной недостаточности. Для таких больных характерны бледность лица, испуганный вид, одышка, частый, слабый пульс, холодный пот. При легочном кровотечении в первый момент кровь в мокроте ярко-красная, алая, на следующий день — более темная, позже — коричневая. Откашливание крови может прекратиться сразу, если бронх закупориваетсясгустком. При обильных легочных кровотечениях развивается картина острой постгеморрагической анемии и коллапса.
При физикальном исследовании определяются булькающие хрипы в области грудины и среднепузырчатые — в лёгких. В случаях аспирации крови, развития аспирационных пневмоний и ателектазов отмечаются укорочение перкуторного звука и ослабленное дыхание, некоторое ослабление голосового дрожания, шум трения плевры.
Уточняется диагноз бронхоскопическим и рентген отомографическим методами исследования, что особенно важно в случаях предполагаемого оперативного вмешательства.
Прогноз. Примерно у 1/3 больных кровохарканье проходит бесследно. Легочное кровотечение редко бывает таким обильным, чтобы непосредственно угрожать жизни больного. Чаще всего в тяжелых случаях внезапная смерть вызывается асфиксией в результате закупорки сгустками крови воздухоносных путей при одновременном спастическом сокращении бронхов.
Лечение. Все больные с кровохарканьем и легочным кровотечением нуждаются в срочной госпитализации и оказании неотложной медицинской помощи.
При оказании неотложной помощи следует воздействовать непосредственно на кровоточащий сосуд, понизить кровенаполнение в малом круге кровообращения и легких, уменьшить проницаемость капилляров легкого и повысить свертываемость крови, восстановить проходимость воздухоносных путей и предупредить гемоаспирационную пневмонию, восполнить кровопотерю .
Больному придают полусидячее положение, накладывают жгуты на нижние конечности, согревают ноги и нижнюю часть живота, периодически поворачивают его на бок, активно аспирируют отсосом кровь и слизь из полости рта, носа и глотки. Больной должен свободно дышать, может негромко разговаривать.
Легочное кровотечение можно задержать внутривенным капельным введением питуитрина — 2 мл или 10 ЕД в 200 мл изотонического раствора натрия хлорида. Основными действующими веществами питуитрина являются окситоцин и вазопрессин, который суживает капилляры, повышает АД, регулирует осмотическое давление крови.
Для разгрузки малого круга кровообращения вводятся раствор атропина (1 мл), камфора (3-4 мл 4 раза в сутки), эуфиллин (2,4 % раствор, 10 мл), ганглиоблокаторы под контролем АД (пентамин, гексоний, димеколин).
С гемостатической целью и для уменьшения проницаемости стенки сосудов применяются викасол (5 мл 0,3 % раствора внутривенно или внутримышечно, по 0,015 г 4 раза в сутки внутрь), аскорбиновая кислота (1 г 3 раза в сутки внутрь), эпсилон-аминокапроновая кислота (5 % раствор до 100 мл на изотоническом растворе натрия хлорида), пентоксил (0,2 г 3 раза в день), дицинон — внутривенно медленно или внутримышечно (2 мл 12,5 % раствора с 20 мл физиологического раствора); адроксон (2 мл 0,025 % раствора внутримышечно), кальция и натрия хлорид, кальция глюконат (10 мл 10 % раствора внутривенно), витамин Р (цитрин, рутин).
Кровопотеря восполняется гемотрансфузиями одногруппной крови (250-500 мл), введением плазмы (100-200 мл).
Для профилактики аспирационной пневмонии больному обеспечивается полусидячее положение и назначаются антибиотики и сульфаниламиды.
При безуспешности консервативного лечения применяются коллапсотерапевтические (компрессионный пневмоперитонеум и пневмоторакс) и хирургические (различные виды резекций легких, торакопластика, перевязка легочных сосудов и бронхов, кавернотомия и т. д.) методы лечения.
ХРОНИЧЕСКИЙ БРОНХИТ (ХБ) — это длительное, прогрессирующее, с волнообразным течением воспаление бронхов и бронхиол, сопровождающееся кашлем с выделением мокроты (обычно вязкой), одышкой, снижением толерантности к физической нагрузке.
По определению группы экспертов ВОЗ, к больным ХБ следует относить тех лиц, у которых кашель с мокротой длится не менее трех месяцев в году в течение двух лет подряд при исключении других заболеваний верхних дыхательных путей, бронхов и легких, которые могли бы вызвать эти симптомы.
При упорном течении ХБ к нему присоединяются бронхоспазм и эмфизема. По мере прогрессирования ХБ нарастают явления легочной гипертензии и формируется хроническое легочное сердце.
Этиология и патогенез. ХБ может быть первичным и вторичным (как осложнение других заболеваний, в первую очередь инфекционных и профессиональных), специфическим (туберкулезным) и неспецифическим.
В большинстве случаев (80 %) первичный ХБ развивается у курильщиков с длительным стажем и протекает более тяжело, чаще отмечаются обструктивные нарушения вентиляции и их большая выраженность.
У некурящих и больных первичным ХБ моложе 50 лет с эмфиземой легких основным этиологическим фактором чаще всего является дефицит альфа-1 -антитрипсина.
В ряду других значимых экзогенных этиологических факторов первичного ХБ выделяются загрязнение воздушной среды, профессиональные вредности, неблагоприятные погодные и климатические условия, инфекции.
В некоторых случаях ХБ является следствием острого бронхита. Формирование ХБ после ОБ отмечено у 10-12 % больных, чаще при смешанных вирусных, вирусно-микоплазменных, вирусно-бактериальных микстинфекциях.
В основе патогенеза лежит нарушение мукоцилиарной системы различными примесями вдыхаемого воздуха (поллютантами).
Вредоносные физические, химические и термические агенты, нарушая структуру и функцию слизистой оболочки трахеобронхиачьного дерева, приводят к развитию асептического воспаления — экссудации и инфильтрации.
Нарушенная дренажная функция бронхиального дерева способствует присоединению к асептическому воспалению респираторной инфекции, активность и рецидивы которой в значительной степени зависят от местного иммунитета бронхов. В последующем на месте бывшего воспаления развивается грануляционная ткань — от “нежного” склероза до рубцевания;происходят глубокие изменения в бронхиальном эпителии — гибнет реснитчатый слой, цилиндрический эпителий метаплазируется в многослойный плоский, появляются атипичные клетки с гиперхромными ядрами неправильной формы.
Одним из неблагоприятных проявлений хронического бронхита, определяющим в значительной степени его прогноз, является развитие выраженных обструктивных нарушений в бронхиальном дереве.
Клиническая картина и диагноз. Клиника ХБ характеризуется главным образом симптомокомплексами бронхиальной обструкции, повышенной воздушности легочной ткани (эмфиземы легких), гипертензии малого круга кровообращения, хронической дыхательной и хронической сердечной недостаточности. При этом особенности клинической картины ХБ у каждого больного определяются вариантами сочетания поражения бронхов и эмфиземы легких (т. е. уровнем поражения бронхолегочного апарата), фазой воспалительного процесса (ремиссией или обострением) и степенью тяжести (в том числе осложнениями).
Наиболее часто больные ХБ жалуются на кашель, одышку и отделение мокроты. Значительно реже отмечаются повышение температуры тела и кровохарканье.
Обострение ХБ обычно носит сезонный характер, возникая в холодное и сырое время года и продолжаясь в среднем 3-4 нед. В период обострения воспалительного процесса появляются или усугубляются вышеуказанные характерные симптомы болезни, а также признаки интоксикации: головные боли, бессонница, гастриты, запоры, зябкость, потливость, особенно ночью (симптом “влажной подушки”), субфебрильное повышение температуры. Следует отметить, что для обострения ХБ не типичны значительное повышение температуры и высокая активность воспалительного процесса по лабораторным показателям. Поэтому в случае выраженной гипертермии (фебрильная температура) и высокой активности воспаления (СОЭ более 40 мм в час, лейкоциты более 12 • 10 3 и т. д.) следует искать какое-либо инфекционное осложнение, например бронхопневмонию, абсцесс легкого и др.
Обострение обструктивного бронхита проявляется цианозом, увеличением одышки (при физической нагрузке и переходе из тепла в холод), отделением небольшого количества мокроты после приступообразного мучительного кашля, удлинением фазы выдоха и возникновением свистящих сухих хрипов на форсированном выдохе.
Наличие обструкции приводит к прогрессированию ХБ, эмфиземе легких, развитию легочного сердца, возникновению ателектазов сложного генеза и как следствие последних — к пневмонии.
В крови даже в период обострения заболевания изменения могут отсутствовать. Иногда определяются умеренный лейкоцитоз, сдвиг лейкоцитарной формулы влево, небольшое повышение СОЭ.
Рентгенологические симптомы у большинства больных длительное время не выявляются. У некоторых больных рентгенограммы показывают диффузное, неравномерное усиление и деформацию, а также изменение контуров легочного рисунка вследствие сетчатого перибронхиального пневмосклероза, при эмфиземе — повышение прозрачности легочных полей.
Бронхоскопически определяются эндобронхиальные признаки воспалительного процесса и оцениваются их выраженность, формы эндобронхитов — гипертрофический, гнойный, атрофический, фибринозно-язвенный, геморрагический, изменения конфигурации и уменьшение просветов бронхов, трахеобронхиальная гипотоническая дискинезия.
Обструктивный характер хронического бронхита подтверждается данными функционального исследования (пневмотахометрией, спирографией).
Лечение больных ХБ должно начинаться на возможно более ранней стадии. Важно устранить все факторы, обусловливающие раздражение слизистой оболочки бронхов (курение, неподходящие условия труда, климатическая зона и т. д.). Лечебные мероприятия в первую очередь должны быть направлены на ликвидацию воспалительного процесса и респираторной инфекции, гипосенсибилизацию, коррекцию вторичных иммунодефицитных состояний и сниженной неспецифической резистентности организма, улучшение бронхиальной проходимости, коррекцию гипоксии.
Необходимо санировать хронические очаги назофарингеальной инфекции, обеспечить свободное дыхание через нос.
Воспалительный процесс купируется нестероидными противовоспалительными средствами (аспирином, ибупрофеном, реопирином и др.).
При обострении ХБ с отделением гнойной мокроты следует назначать антибактериальные препараты, эффективные прежде всего в отношении палочки инфлюэнцы, пневмококка и грамотрицательных микробов. В случае легкого обострения с отделением слизистой или слизисто-гнойной мокроты можно применять сульфаниламидные препараты длительного действия (сульфадиметоксин, сульфапиридазин по 0,5-1 г один раз в сутки, сульфален — 0,2 г один раз в сутки). Больным с небольшой длительностью заболевания, не лечившимся ранее разнообразными антибиотиками, показано внутримышечное введение бензилпенициллина по 300-500 тыс ЕД 4-6 раз в сутки. Больным с выраженными признаками воспалительного процесса антибиотики назначаются с учетом чувствительности микрофлоры. Правильность выбора препарата подтверждается результатом лечения. Чаще всего назначаются полусинтетические пенициллины (ампициллин, ампиокс, диклоксациллин и др.), аминогликозиды (гентамицин), цефалоспорины (кефзол, клафоран и др.), тетрациклины пролонгированного действия (вибрамицин), макролиды (эритромицин), левомицетин и др. Курс лечения — 2 нед, иногда больше (до 20 дн). Весьма эффективны эндотрахеальные вливания подогретого раствора фурацилина или фурагина (на курс лечения 10-12 заливок). После каждой процедуры эндобронхиальной санации выполняются позиционный дренаж и вибрационный массаж грудной клетки.
Для восстановления бронхиальной проходимости назначаются селективные стимуляторы р 2 -адренергических рецепторов (беротек, бриканил, сальбутамол), блокаторы ацетилхолина (атровент), препараты метилксантина (эуфиллин, теофиллины длительного действия — теопэк, дурофилин и др.), блокаторы каналов тока кальция (коринфар). Эффективны препараты комбинированного действия — теофедрин, солутан, беродуал и др.
Лучшему отхождению мокроты способствуют отхаркивающие средства (настои термопсиса, мать-и-мачехи, багульника, чабреца, подорожника, отвар алтейного корня, 3 % раствор йодида калия и др.), ингаляции щелочных растворов, обильное горячее питье, прием щелочных минеральных вод. При вязкой мокроте назначаются ингаляции ферментов — трипсина, химотрипсина, химопсина, рибонуклеазы, дезоксирибонуклеазы. Ферменты можно вводить и внутримышечно (трипсин или химотрипсин — по 10-20 мг в растворе новокаина 1-2 раза в день). Для разжижения мокроты с успехом используются также муколитические средства: 10 % раствор ацетилцистеина по 2 мл внутримышечно или в виде ингаляций аэрозоля 3 раза в день, бромгексип (бисольвон) внутрь, парентерально или в виде ингаляций аэрозоля по 4-7 мг 2-3 раза в день.
Дренажную функцию бронхов у больных с гнойным ХБ можно улучшать с помощью лечебных бронхоскопий (2-4 процедуры с интервалом в 3-7 дн) с интратрахеальным введением лекарств (антибиотиков; муколитических препаратов — ацетилцистеина, химотрипсина, трипсина, рибонуклеазы; бронхолитических средств — эфедрина, нафтизина; антисептических растворов -фурацилина, фурагина и др.).
Для купирования бронхоспазма назначается электрическое поле УВЧ с последующим электрофорезом платифиллина (0,1 % раствор), эуфиллина (5 % раствор). Для улучшения отхождения мокроты применяются йод-электрофорез (5 % раствор) с индуктотермией, трипсин- или панкреатин-электрофорез и др.
Не утратило своего значения применение различных отвлекающих средств (горчичников, банок, теплых ножных ванн и т. д.). При стихании явлений обострения заболевания, обычно с 4-6-го дня от начала заболевания, назначаются физиотерапевтические процедуры (соллюкс, УФО, токи УВЧ, электрофорез новокаина, хлорида кальция на грудную клетку) .
Для улучшения бронхиальной проходимости и восстановления дренажной функции бронхов назначаются массаж грудной клетки и лечебная физкультура, включая постуральный дренаж. Основным методом ЛФК у больных ХБ является лечебная “экспираторная” гимнастика. В комплексе “экспираторной” гимнастики используются динамические дыхательные упражнения, акцентированные на выдохе.
Санаторно-курортное лечение при ХБ проводится в теплое сухое время года на климатических курортах Южного берега
Крыма, среднегорья (Кисловодск, Теберда) или в местных санаториях (Бобруйск, Нарочь).
ЭМФИЗЕМА ЛЕГКИХ. В практической медицине термином “эмфизема легких” обозначается всякое увеличение воздушности легких, которое может быть функциональным (острое вздутие легких), компенсаторным (викарным), старческим (атрофическим), хроническим субстанциальным (обструкционным) и др.
Наиболее часто встречающиеся формы эмфиземы легких делятся на две большие группы — необструкционные и обструкционные эмфиземы легких. При необструкционных эмфиземах отсутствуют явления обструкции терминальных бронхиол и мелких бронхов, а при обструкционных эмфиземах нарушения вентиляции, обусловленные коллапсом терминальных бронхиол и (или) обтурацисй мелких бронхов, составляют часть потенциала болезни.
К необструкционным эмфиземам легких относятся компенсаторная и старческая, а к обструкционным — функциональная и хроническая субстанциальная эмфизема как самостоятельная форма хронической обструкционной болезни легких.
Эмфизематозное легкое напоминает собой изношенную перерастянутую резину, которая, потеряв свои эластические свойства, не может сократиться до своего прежнего объема. Эмфизематозное легкое не спадается, а следовательно, занимает больший объем, чем здоровое.
Патогенез. В большинстве случаев эмфизема легких вторична и является следствием диффузных заболеваний легких, прежде всего хронического обструктивного бронхита (обструкционная, центрилобулярная, или центриацинозная, эмфизема легких). Эмфизематозный процесс поражает альвеолы, расположенные вблизи от респираторных бронхиол, поскольку воспалительно-дистрофический процесс переходит с респираторных бронхиол на прилежащие к ним альвеолы.
Эмфизема легких может развиваться и без предшествующего заболевания легких (первичная диффузная, идиопатическая или панацинозная). Возникновение первичной эмфиземы прежде всего связывается с наследственным дефицитом альфа-1-ингибитора протеаз (альфа-1-антитрипсина), определенное значение имеют также нарушения легочной микроциркуляции, изменения свойств сурфактанта, курение и т. п. Первичная эмфизема при наследственном дефиците альфа-1-антитрипсина возникает у молодых людей, поэтому называется юношеской эмфиземой легких. В последние годы отмечается существенное увеличение больных ХНЗЛ с дефицитом альфа-1-антитрипсина. Первичная панацинозная ( панлобулярная) эмфизема легких равномерно поражает все альвеолы, входящие в состав дольки легкого. Уменьшается функционирующая поверхность легкого.
БОЛЕЗНИ ОРГАНОВ ДЫХАНИЯ
Клиническая картина и диагноз. Клиника эмфиземы легких в основном ограничивается симптомокомплексом повышенной воздушности легочной ткани, а также симптомами дыхательной и сердечной недостаточности. Клинические проявления хронической субстанциальной (истинной) эмфиземы легких заметно “отстают” от патоморфологических, поэтому по клиническим признакам диагностируется уже полностью сформировавшаяся эмфизема. Главные жалобы больных эмфиземой легких — одышка и повышенная утомляемость.
Больные эмфиземой, страдающие хроническим бронхитом, жалуются также на сухой кашель, усиливающийся с одышкой.
Для больных эмфиземой легких внешне характерны приподнятые плечи, короткая шея, бочкообразная грудная клетка, сдавленная с боков, со втягивающимися при вдохе межреберными промежутками, акроцианоз. Выбухает грудина. Расширены и даже выбухают межреберные промежутки, сглаживаются или выбухают надключичные области, уменьшается дыхательная экскурсия грудной клетки. В акте дыхания участвуют вспомогательные мышцы: на вдохе — грудино-ключично-сосцевидные и лестничные, на выдохе — передние зубчатые и брюшного пресса . На выдохе больные прикрывают рот, раздувая щеки (пыхтение). Перкуторно определяются “коробочный” звук, ограниченная подвижность легочного края, низкое стояние и уменьшение подвижности диафрагмы, ослабленное дыхание с усиленным выдохом. Выслушиваются рассеянные сухие, иногда влажные мелкопузырчатые хрипы. Границы сердца определяются с трудом. У больных эмфиземой легких снижается масса тела, что объясняется преобладанием катаболических процессов, которые главным образом затрагивают альвеолы и в меньшей степени — другие ткани.
При выраженной дыхательной недостаточности в периферической крови могут отмечаться эритроцитоз, увеличение содержания гемоглобина.
У больных с первичной панацинозной эмфиземой легких понижен уровень альфа-1-антитрипсина в сыворотке крови .
Наиболее характерными рентгенологическими симптомами первичной панацинозной эмфиземы являются: однородное повышение прозрачности легочных полей и обеднение легочного рисунка, особенно в нижних отделах, низкое стояние диафрагмы и “висячее сердце”. При вторичной центриацинозной эмфиземе легких прозрачность их нижних отделов значительно уменьшена вследствие перибронхита и других изменений. Диафрагма обычно не смещается книзу, так как общий объем легких изменен незначительно.
Лечение. Полное излечение эмфиземы легких невозможно в связи с ее неуклонным прогрессирующим течением и необратимостью структурных изменений легочной ткани. Поэтому лечение эмфиземы легких направлено в основном на борьбу с заболеванием, вызвавшим ее развитие (например, хроническим бронхитом, дыхательной недостаточностью, легочной гипертензией и хроническим декомпенсированным легочным сердцем). При наличии хронического обструктивного бронхита назначаются отхаркивающие и успокаивающие кашель средства (термопсис, муколитики, кодеин), аэрозольтерапия, трахеобронхиальные вливания антимикробных растворов, ферментов; при бронхоспазме — бронхоспазмолитики (эуфиллин); при декомпенсированным легочном сердце — сердечные гликозиды (коргликон), препараты, разгружающие систему легочной артерии (лазикс).
При лечении эмфиземы легких необходимо учитывать негативные последствия использования адреналина, Шадрина, норадреналина, эфедрина, холинолитических средств. Так, адреналин ухудшает вентиляционную функцию, способствует открытию артериовенозных шунтов. Изадрин, норадреналин, эфедрин у многих больных эмфиземой легких также ухудшают легочную вентиляцию. Холинолитические препараты эффективны только при парентеральном введении.
Не следует применять стимуляторы дыхания, поскольку дыхательный центр у больных эмфиземой легких остается функционально сохранным. Эуфиллин наиболее эффективен при внутривенном введении (2,4 % раствор по 5 мл в изотоническом растворе натрия хлорида 2-3 раза в день повторными 10-дневными курсами) или при назначении его в суппозиториях по 0 , 4 г 2 раза в день.
Лечение дыхательной недостаточности включает в себя прежде всего обязательный отказ от курения, употребления алкоголя, ограничение физической активности, обучение рациональному дыханию с участием диафрагмы. Рекомендуется работа в теплом помещении с хорошей вентиляцией и чистым воздухом. Противопоказано работать при загрязненном воздухе, в сырости и холоде. Больные эмфиземой легких не должны находиться и накуренном помещении. Иногда целесообразно сменить место жительства, причем предпочтение следует отдавать районам с сухим и теплым климатом (например, Крым и юг Украины). Большую пользу может принести лечебная физкультура, которая укрепляет дыхательную мускулатуру, обеспечивает полноценный выдох. Особое внимание обращается на дыхательные упражнения. Больному рекомендуется делать короткий вдох и длительный выдох. Причем в дыхании должны участвовать мышцы диафрагмы и брюшной стенки. Если эти мышцы тренированы, усиливается выдох. Одним из наиболее действенных является следующее упражнение: вдох через нос, во время медленного выдоха — через рот — больной произносит как можно дольше одну из следующих букв: С, 3, Ш, Ж, И или У. Это упражнение повторяется 4-5 раз с паузами в одну-полторы минуты.
Назначаются также массаж грудной клетки, аэротерапия прогулки на свежем воздухе с постепенным удлинением маршрута. Показаны курсы оксигенотерапии, которые позволяют уменьшить гипоксемию и способствуют снижению давления в легочной артерии. Однако при этом необходимо помнить, что если эмфизема легких осложняется гиперкапнией, то чувствительность дыхательного центра к углекислому газу резко снижается. Поэтому бесконтрольное применение оксигенотерапии, устраняя гипоксемический стимул дыхания, ведет к усилению гиповентиляции и усугублению гиперкапнии. При тяжелой эмфиземе легких оксигенотерапия должна проводиться методом прерывистой ингаляции кислородно-воздушной смеси с 30 % концентрацией кислорода.
В случаях тяжелой дыхательной недостаточности можно применять вспомогательную искусственную вентиляцию легких с помощью респираторов любого типа, регулируемых по объему, частоте или давлению (Ро-1, Ро-2, Ро-5, РД-1, ДП-8, РЧП-1). Методика вспомогательной искусственной вентиляции заключается в проведении двухразовых сеансов продолжительностью 40-60 мин. Длительность курса составляет S*-4 нед.
При локализованных формах эмфиземы легких (в пределах доли), крупных буллах, осложнениях в виде спонтанного пневмоторакса применяется хирургическое лечение. Удаление эмфизематозных булл расправляет и улучшает работу той части легкого, которая до этого была сдавлена и практически бездействовала.
ПЛЕВРИТ — это инфекционный или асептический воспалительный процесс различной этиологии в листках плевры, сопровождающийся образованием на их поверхности фибринозных наложений и (или) скоплением в плевральной полости жидкого (серозного, гнойного, геморрагического, хилезного и др.) экссудата. Плевриты могут быть первичными и вторичными. Плевриты считаются первичными в тех случаях, когда местный воспалительный процесс и связанная с ним общая реакция организма являются основными признаками болезни. Абсолютное большинство плевритов является вторичным процессом и возникает при наличии гнойно-воспалительных процессов в прилежащих (туберкулез легких, пневмония, медиастинит, абсцесс печени, поддиафрагмальный абсцесс, паранефрит, панкреатит и др.) или отдаленных (остеомиелит, отит, синусит и др.) органах и тканях. В зависимости от наличия или отсутствия выпота плевриты делятся на сухие (фибринозные) и выпотные (экссудативные).
Спаечные и рубцовые изменения в плевральной полости часто обозначаются как адгезивный, оссифицирующий плеврит. Однако правильнее их рассматривать как исход воспаления. Свободный выпот в плевральной полости наблюдается при отсутствии сращений между листками висцеральной и париетальной плевры и может располагаться типично и атипично.
Осумкованные плевриты возникают при наличии сращений между плевральными листками. Их локализация весьма разнообразна.
Клиническая картина и диагноз. Клинически выраженный сухой плеврит начинается обычно с внезапных болей в той или другой половине грудной клетки, лихорадки и кашля. Наблюдаются общие явления — слабость, недомогание, плохой аппетит, ночные поты, ознобы.
При осмотре больного обращают на себя внимание его поза, мимика и характер дыхания. Так, при одностороннем плеврите больной щадит пораженную сторону: ограничивает дыхательные движения, предпочитает положение лежа на больном боку, не шевелясь; придавливает рукой больную сторону в положении сидя или стоя.
При аускультации над областью сухого плеврита можно выслушать ослабленное дыхание и шум трения плевры, различный по тембру и продолжительности, локализованный либо разлитой. Шум трения плевры, вначале очень нежный, впоследствии приобретает более грубый характер, напоминает скрип новой кожи или грубое царапанье. Клиническая картина экссудативного (выпотного) плеврита обычно зависит от заболеваний, осложнением которых он явился.
При клинически выраженном экссудативном плеврите типичными жалобами больных являются одышка, чувство тяжести в груди и кашель. По мере накопления выпота одышка и ощущение тяжести в грудной клетке нарастают, хотя строгой зависимости этих жалоб от количества жидкости в плевральной полости не отмечается. При осмотре можно наблюдать характерное вынужденное положение больного — лежа на больном боку. При очень больших выпотах или явлениях дыхательной и сердечной недостаточности больные принимают полусидячее положение. Дыхательные экскурсии больной стороны грудной клетки ограничены (грудная клетка на стороне поражения отстает при дыхании ) . Повышенное давление скопившейся в плевральной полости жидкости увеличивает объем соответствующей половины грудной клетки, а также приводит к выбуханию и расширению межреберных промежутков. Если количество плеврального превышает 300-500 мл, то на пораженной стороне отмечаKIи и притупление перкуторного звука (при массивных выпотах щук чупой), ослабление или исчезновение голосового дрожания и дыхательных шумов. Зона притупления имеет изогнутую верхнюю границу (линия Дамуазо). При левостороннем плеврите исчезает иолулунное пространство Траубе.
Нередко решающим методом диагностики становится плевральная пункция. Оцениваются внешний вид плевральной жидкости, ее клеточный состав, производится биохимическое и бактериологическое исследование.
При рентгенологическом исследовании при сухом плеврите выявляется лишь ограниченная подвижность диафрагмы на больной стороне; позднее отмечается легкое диффузное затемнение легочного поля, обусловленное плевральными сращениями, швартами.
Рентгенологическое отображение плеврального выпота зависит от его количества, состояния плевральной полости (например, спайки, шварты и др.) и положения туловища больного (вертикальное или горизонтальное). На рентгенограммах легких определяется затемнение от небольшого до тотального в зависимости от величины выпота.
Очень большое диагностическое значение имеет торакоскопия с биопсией плевры, которая позволяет выявить туберкулезное или опухолевое происхождение плеврита.
Лечение. Лечение плеврита должно быть комплексным и направленным прежде всего на ликвидацию основного процесса, приведшего к его развитию. Симптоматическое лечение имеет целью обезболивание, ускорение рассасывания фибрина, предупреждение образования обширных шварт и сращений в плевральной полости.
Опасность преобразования серозного экссудата в гнойный или осумкованный обусловливает необходимость проведения регулярных плевральных пункций (через 1-2 да) с его максимальной эвакуацией. Данная тактика дает наилучшие анатомические и функциональные исходы, поскольку легкое полностью расправляется и не развивается облитерация.
При гнойных плевритах экссудат эвакуируется, полость дренируется и промывается антисептическими растворами, вводятся внутриплеврально антибиотики.
При интоксикации, выраженной одышке, нарушениях деятельности сердца применяются внутривенно капельно плазмозамещающие растворы, ингаляции кислорода, сердечные гликозиды. Для уменьшения болей (особенно у больных сухим плевритом) можно использовать банки, горчичники, сухое тепло, согревающие компрессы с тугим бинтованием нижних отделов грудной клетки, смазывание пораженной стороны йодной настойкой в виде сетки.
По мере рассасывания экссудата, после исчезновения боли, нормализации температуры тела и СОЭ больным рекомендуются занятия ЛФК с включением дыхательных упражнений для предотвращения плевральных спаек. При отсутствии противопоказаний проводится физиотерапевтическое (соллюкс, индуктотермия, электрофорез) и санаторно-курортное (санатории местные, Южного берега Крыма, Черноморского побережья Кавказа и др.) лечение.
ПНЕВМОКОНИОЗЫ (от греч. pneumon — легкие, konis -пыль) — группа хронических профессиональных заболеваний легких, обусловленных попаданием в легкие большого количества пылевых частиц в течение длительного времени.
Этиология и патогенез. Пневмокониозы встречаются у рабочих горнорудной, угольной, асбестовой, машиностроительной и некоторых других отраслей промышленности, которые вдыхают различные виды пыли на протяжении 5-15 лет и более. Общим признаком всех видов пневмокониоэов является развитие интерстициального фиброза. Наиболее выраженными фиброгенными свойствами обладает пыль, содержащая свободную двуокись кремния. Менее опасна пыль, содержащая большинство силикатов, еще ниже фиброганнм активность пыли некоторых металлов, в частности бериллия, Слабо выражены фиброгенные свойства у большинства видов. Определенное значение в развитии пнсвмокониозов имеют форма и величина пылевых частиц, их концентрация и другие факторы. Так, наиболее опасна мелкодисперсная пыль, состоящая из частиц диаметром 0,5-7 мм. Предельно допустимая концентрация фиброгенной пыли колеблется от 1 до 10 мг в 1 м 3 в зависимости от содержания в ней свободной двуокиси кремния. Важный лхологический фактор пневмокониозов — цитотоксичность пыли (разрушение пылью альвеолярных макрофагов).
В то же время на возникновение и развитие пневмокониозоп влияют предшествующее состояние органов дыхания, иммунологический статус, аллергическая реакция и др. Каждый вид пневмокониоза имеет свои особенности, определяемые в первую очередь при гистологическом исследовании.
Классификация пневмокониозов (МЗ СССР, 1976) состоит из двух разделов: 1) этиологическая группировка но пилам промышленной пыли; 2) рентгенологическая и клиники функциональная характеристика заболевания. Этиологическая группировка:
- Силикоз от вдыхания пыли свободной двуокиси кремния
- 2. Сшшкатозы от вдыхания пыли силикатов, содержащей двуокись кремния не в свободном, а в связанном с другими элементами состоянии (асбестоз, талькоз, каолиноз, цементный, слюдяной пневмокониоз и др.).
- Металлокониозы от вдыхания пыли металлов (бериллиоз, алюминоз, баритоз, станиоз, пневмокониоз) от редко-земельных твердых и тяжелых сплавов и др.).
- Карбокониозы от вдыхания углеродсодержащей пыли( сажевый пневмокониоз и др.).
- Пневмокониозы от вдыхания смешанной пыли, содержащей свободную двуокись кремния (антракоз, сидеросиликоз, сили косиликатоз) и не содержащей свободной двуокиси кремнии или с незначительным содержанием ее (пневмокониоз шлифовальщиков, электросварщиков и др.).
- 3. Пневмокониозы от вдыхания органической пыли (хлопковой, зерновой, пробковой, тростниковой и др.).
Рентгенологически определяемые затемнения подразделяются на три формы: узелковые, интерстициальные и узловые, что соответствует морфологическому представлению о формах пневмокониозов. По степени выраженности фиброзных изменений выделяются три рентгенологические стадии пневмокониозов: I -интерстициальные изменения (ячеистый и линейный легочный рисунок), или мелкоузелковый диффузный фиброз; II — крупноузелковый (узелки диаметром 1-4 мм) пневмофиброз типа “снежной бури” ; III — распространенный крупноузелковый фиброз с образованием сливных конгломератов, буллезная эмфизема, массивные плевральные сращения.
Клинико-функциональные признаки пневмокониозов включают бронхит, бронхиолит, эмфизему легких, легочную недостаточность (I, II и III степени), легочное сердце.
По течению болезни различаются пневмокониозы быстро прогрессирующие, медленно прогрессирующие, регрессирующие (встречаются в отдельных случаях) и с поздним развитием.
В классификацию включены возможные осложнения пневмокониозов: туберкулез, пневмония, бронхоэктатическая болезнь, рак легкого, ревматоидный артрит, спонтанный пневмоторакс, бронхиальная астма. Сочетание пневмокониоза с туберкулезом легких принято называть кониотуберкулезом — силикотуберкулез, антракосиликоз, сидеросиликоз и т. п.
Клиническая картина. Клиническая картина пневмокониозов имеет ряд сходных черт: одышка при физической нагрузке, боли в груди и сухой кашель. Часто выявляются симптомы гипер- и атрофического ринита, бронхита, базальной эмфиземы и сухого плеврита. При прогрессировании болезни нарастают одышка, эмфизема, кашель, уменьшаются ЖЕЛ, объем легочной вентиляции, развиваются легочная и сердечная недостаточность. Функциональные нарушения органов дыхания при пневмокониозе обусловлены выраженностью фиброза легочной ткани, последствиями взаимодействия пыли с тканями организма (раздражение дыхательных путей, токсичность, аллергизация и др.), осложнениями и сопутствующими заболеваниями.
Диагностика пневмокониозов основана на комплексном исследовании. Детальное клинико-рентгенофункциональное обследование больного должно быть дополнено изучением его профессионального маршрута. При этом следует иметь в виду как наличие контакта с производственной пылью, так и его длительность, концентрацию пыли, ее состав, содержание в ней свободной или связанной двуокиси кремния и других ингредисигов, дисперсность пылевых частиц и др. Данные о санитарно-гигиенических условиях труда больного должны быть в достаточной степени объективно оценены и документированы, без чего невозможно судить о профессиональной этиологии заболевания.
Наиболее надежным методом диагностики пневмокониоза является рентгенологическое исследование (обзорная полипозиционная рентгенография, томография, рентгенопневмополиграфия).
Лечение. Лечение пневмокониозов симптоматическое. Необходимо обеспечить рациональное питание для нормализации обмена веществ, в первую очередь белкового, насытить организм витаминами С, Р и PP. Большое значение имеет улучшение дренажной функции бронхов (отхаркивающие средства, аэрозольтерапия). При затрудненном дыхании показаны бронхорасширяющие средства (теофедрин, эуфиллин, аэрозоли атропина, эфедрина, эуспирана), кислородотерапия; при декомпенсации легочного сердца — мочегонные средства и сердечные гликозиды.
При обострении хронического воспалительного процесса в легких (бронхиты, пневмонии) применяется энергичная противовоспалительная и антибактериальная терапия. В некоторых случаях (например, при асбестозе) положительные результаты могут быть достигнуты с помощью кортикостероидов. С целью тренировки дыхательного аппарата и сердечно-сосудистой системы назначаются ЛФК и массаж грудной клетки.
В начальных стадиях пневмокониозов показано санаторно-курортное лечение (Южный берег Крыма, Кисловодск, кумысолечение на курортах Казахстана и др.).
Для профилактики пневмокониозов важное значение имеют санитарный надзор за работой производств с повышенной запыленностью, проведение предварительных (при поступлении на работу) и периодических медицинских осмотров (1-2 раза в год).
ОСТРЫЕ ПНЕВМОНИИ (ОП) — это группа самостоятельных острых малоконтагиозных болезней легких инфекционной природы, которые характеризуются преимущественно экссудации 1ым воспалением альвеол, межуточной ткани и (или) сосудистой системы и протекают обычно при отсутствии каких-либо других органных поражений.
Из числа ОП как самостоятельных заболеваний исключены также легочные воспалительные процессы неинфекционной природы, в том числе аллергические, эозинофильные и аутоиммунные (например, пневмониты при диффузных болезнях соединительной ткани, ревматические инфильтраты и др.).
Актуально деление ОП на первичные и вторичные. К первичным ОП относятся те, которые возникают в ранее здоровых легких обычно у молодых людей внезапно, остро, нередко бывают связаны с охлаждением. Вторичные ОП формируются на фоне других, чаще хронических, заболеваний (ХНЗЛ, недостаточность кровообращения, сепсис и др.) и патологических состояний, обусловленных аспирацией и сдавлением бронхов, травмой, операцией, токсическими, термическими, лучевыми и иными воздействиями.
Этиология и патогенез. Если раньше почти единственным возбудителем ОП считался пневмококк, то теперь существенное значение имеют условно-патогенные микроорганизмы — гноеродные кокки и грамотрицательные бактерии, т. е. по существу микробные виды, которые являются представителями нормальной микрофлоры дыхательных путей, причем в ряде случаев эти микроорганизмы приобретают признаки вирулентности.
В зависимости от этиологии первичные ОП делятся на бактериальные (пневмококковые, стрептококковые, стафилококковые, фридлендеровские, легионеллезные), вирусные (гриппозные, орнитозные, аденовирусные), микоплазменные, пневмоцистные, риккетсиозные, паразитарные и грибковые.
К. ОП предрасполагают различные причины, снижающие общую сопротивляемость организма: переохлаждение, переутомление, интоксикация, травмы, нарушение нормальных условий труда, быта, заболевания верхних дыхательных путей и ЛОР-органов, хронические заболевания органов дыхания, сердечнососудистой системы и др.
ПНЕВМОКОККОВЫЕ ОП — это большая часть бактериальных ОП. Пневмококки (Streptococcus pneumoniae, типы 1-83) могут вызывать два основных вида ОП — крупозную и бронхопневмонию, что зависит как от штамма и количества пневмококков, так и от состояния макроорганизма.
Крупозная пневмония протекает по гиперергическому типу, что проявляется быстрым, почти одномоментным поражением целой доли легкого и внезапным началом заболевания.
Патологоанатомически крупозная ОП отличается установленной последовательной сменой четырех стадий воспалительного процесса — прилива, красного и серого опеченения, разрешения.
В последние годы крупозная пневмония из “долевой” стала “сегментарной”, т. е. в большинстве случаев она начинается не с долевого, а с сегментарного поражения. Все патологоанатомические стадии крупозной пневмонии определяются в пределах одного-двух сегментов, вплоть до полного рассасывания.
Бронхопневмония (дольковая, катаральная, очаговая пневмония) в отличие от крупозной развивается по пути: эндобронхит — панбронхит — пневмонический фокус, т. е. вначале поражается стенка бронха, а затем легочная паренхима. При кашле, который вызывается обычно острым бронхитом, обсемененная пневмококками мокрота инфицирует различные отделы бронхиального дерева, а затем воспалительный процесс переходит на легочную паренхиму. Поэтому для бронхопневмонии характерно быстрое, но не одновременное возникновение множественных воспалительных очагов в различных отделах легких. При этом в одних пневмонических фокусах процесс только начинается (стадия прилива), в других он в разгаре (красное или серое опеченение), в третьих — уже завершается (стадия разрешения). Вследствие такого неодновременного поражения легкое на срезе имеет пестрый вид.
СТРЕПТО- И СТАФИЛОКОККОВЫЕ ОП составляют около 10 % всех пневмоний, диагностируемых у взрослых. В основном этой формой пневмонии болеют дети, особенно новорожденные и грудные.
Стрептококковая ОП в настоящее время встречается редко, что объясняется высокой чувствительностью стрептококка к антибиотикам группы пенициллина. Стрептококковая ОП может быть как первичной, так и осложнением другого заболевания (кори, гриппа и др.).
Стафилококковая ОП редко бывает первичной, чаще всего она вторичная бронхогенная и гематогенная при стафилококковом сепсисе. В отличие от стрептококковой ОП она плохо поддаются терапии антибиотиками.
Стрептококковые и стафилококковые ОП характеризуются нозникновением множественных воспалительных фокусов среднего и большого размера в обоих легких, обладают выраженной тенденцией к слиянию и последующему распаду.
Поскольку гнойная мокрота, содержащая стрепто- и стафилококки, переносит эту инфекцию в различные отделы легких неодновременно, то в момент наблюдения за больным можно сразу обнаружить в одних пневмонических фокусах признаки инфильтрации, в других — полости распада, в третьих — формирование кисты. Для стрепто- и стафилококковых ОП восьми типично присоединение к процессу в легких экссудативного пленрита, чаще всего гнойного. Затем остаются участки пневмосклероза. В отдельных случаях, ложные кисты разрываются и приводят к спонтанному пневмотораксу. В зоне бывшего плеврального экссудата остаются плевральные шварты и облитерация синусов.
ФРИДЛЕНДЕРОВСКАЯ (КЛЕБСИЕЛЛЕЗНАЯ) ОП вызывается фридлендеровской палочкой (Klebsiella pneumoniae). Среди других ОП она составляет 0,5-4 %. Фридлендеровская ОП обычно развивается у детей и относительно редко у взрослых. Мужчины (особенно злоупотребляющие алкоголем, длительно курящие, страдающие хроническими заболеваниями) болеют в 5-7 раз чаще женщин, люди среднего и пожилого возраста -чаще молодых.
Фридлендеровская ОП отличается тяжестью течения, чем немного напоминает крупозную ОП, чаще локализуется в верхней доле правого легкого и осложняется абсцедированием. Может быть полилобарное расположение процесса.
Воспалительные инфильтраты легочной паренхимы при этой форме ОП быстро сливаются в обширное долевое поражение, напоминающее фазу опеченения при долевой крупозной пневмонии. Уже в первые дни болезни в этом инфильтрате возникают множественные очаги распада и расплавления легочной ткани, на месте которых затем быстро образуются тонкостенные кистевидные образования без видимого перифокального воспаления.
Особая тяжесть фридлендеровской ОП связана с появлением метастатических фокусов воспаления в оболочках мозга, а также в костях. Ее типичным исходом является пневмосклероз, нередко с множественными полостями типа кист и бронхоэктазов. Пневмосклероз в большинстве случаев сопровождается облитерацией прилежащих отделов плевральной полости.
ЛЕГИОНЕЛЛЕЗНАЯ ОП вызывается грамотрицательной аэробной бактерией Legionella pneumophila. Название болезни и ее возбудителя связано с тем, что впервые вспышка этого заболевания была зарегистрирована у членов организации ветеранов войны “Американский легион”, которые в 1976 г. в г. Филадельфии (США) собрались на свой конгресс. Из 182 заболевших тогда 29 человек умерли.
Легионеллезная ОП составляет 0,5-1,5 % всех ОП. Считается, что если заболевание протекает в виде эпидемий — это болезнь “легионеров”, а если в виде спорадических случаев — это легионеллезная ОП. Инкубационный период с момента заражения длится 5-7 да.
Резервуарами возбудителя служат земля и, возможно, вода. Описаны вспышки заболевания во время земляных работ, при загрязнении систем кондиционирования; зарегистрировано также большое количество спорадических случаев заболевания.
Легионеллезную ОП следует предполагать при развитии тяжелой ОП в нехарактерный сезон (конец лета) у мужчин среднего или пожилого возраста при наличии предрасполагающих факторов (курение, применение иммунодепрессантов, алкоголизм, сахарный диабет и др.). Характерно возникновение легочного инфильтрата вначале в одной доле, а затем быстрое развитие инфильтратов в нескольких долях с обеих сторон. Нередко на фоне очагово-инфильтративного процесса выявляются признаки распада, иногда одновременно наблюдается эмпиема плевры.
При морфологическом исследовании легких выявляется картина, напоминающая появление опеченения при крупозной пневмонии; в экссудате определяется большое количество Legionella pneumophila.
Длительность заболевания колеблется от 3 нед до 2 мес и более. В очень тяжелых случаях к концу первой недели может наступить смерть от кровотечения, инфаркта легкого, острой почечной недостаточности и других осложнений.
ГРИППОЗНЫЕ ОП вызываются пневмотропными вирусами гриппа Al, A2 и В, а также вирусно-бактериальными ассоциациями. В настоящее время ставится под сомнение существование чистых (изолированных) вирусных ОП, поскольку вирус обладает только цитотоксическим действием.
ОП, возникающие в периоды эмидемий гриппа или сезонных вспышек ОРЗ, которые начинаются с вирусных поражений слизистых оболочек верхних дыхательных путей и глотки (подтвержденные лабораторными и вирусологическими исследованиями), объединяются в группу смешанных, или вирусно-бактериальных и бактериально-вирусных.
ОП считается вирусно-бактериальной, если вызывающим ее этиологическим фактором является острое вирусное заболевание на фоне хронической бактериальной очаговой инфекции. ОП считается бактериально-вирусной, если в основе ее этиологии лежит острая бактериальная инфекция на фоне острой или длительно персистирующей вирусной инфекции. Патогенез вирусно-бактериальной ОП, равно как и бактериально-вирусной, обусловлен ослаблением иммунного надзора. Если вирусное заболевание отвлекает зашитные силы иммунной системы от хронического бактериального очага воспаления, возникает бактериально-вирусная ОП. Если же вирусное заболевание отвлекает иммунную систему от персистирующей вирусной инфекции в цилиндрическом эпителии трахеобронхиального дерева, то возникает вирусная, или вирусно-бактериальная, ОП. 20 % больных смешанной формой ОП — это люди старше 60 лет, т. е. того возраста, когда проявляется физиологическая иммунная недостаточность.
Гриппозные пневмонии значительно чаще возникают во время эпидемий гриппа. Частота гриппозных пневмоний улиц молодого возраста без сопутствующих заболеваний во время эпидемий достигает 10 % всех заболеваний гриппом, а в межэпидемическое время составляет около 3 %. Следует отметить, что в межэпидемический по гриппу период это заболевание наблюдается очень редко (3-5 % всех острых респираторных заболеваний). Гриппозной ОП обычно подвержены беременные женщины и больные с заболеваниями сердца, особенно с ревматическим митральным стенозом.
Гриппозная ОП в отличие от бактериальной паренхиматозной является преимущественно интерстициальной, т. е. поражается главным образом межуточная ткань вокруг бронхов, сосудов, ацинусов, долек и сегментов. В части случаев вирус гриппа повреждает сосудистые и бронхиальные стенки, иногда возникают тромбозы мелких сосудов, в отдельных местах легких появляется геморрагический отек. Преимущественно интерстициальная локализация воспаления объясняется тем, что инфекция распространяется гематогенным путем, первично поражая эндотелий капилляров. Вирус гриппа поражает и способствует уплотнению эндотелия капилляров и собственной мембраны легочных альвеол. Возникает мембраноз, резко нарушающий газообмен, клинически проявляясь одышкой и цианозом.
Поскольку отсутствует массивное поражение легочной паренхимы, то легкое длительное время остается воздушным, т. е. в альвеолах нет экссудата.
При более длительном течении заболевания в процесс вовлекаются стенки альвеол, а затем в их просвете скапливается как экссудат, так и транссудат.
В случае присоединения вторичной флоры (стрептококки, стафилококки и др.) на фоне вышеуказанных интерстициальных изменений может развиться вторичная вирусно-бактериальная ОП, обычно локализующаяся в боковых и нижних отделах, а также в средней доле.
Течение гриппозной острой интерстициальной пневмонии длительное — 3-8 нед и более. В части случаев при затянувшемся течении могут наблюдаться уплотнение плевры, очаги пневмосклероза.
ОРНИТОЗНАЯ (ПСИТТАКОЗНАЯ) ОП вызывается особым фильтрующимся вирусом, который передается различными домашними и дикими птицами. Поскольку первые зарегистрированные случаи болезни были связаны с попугаями, то вначале ее называли попугайной болезнью, или пситтакозом. В последующем было установлено, что это заболевание возникает и при контакте с другими птицами, поэтому его окончательное название — орнитоз.
Замечено, что среди лиц, работающих на птицефермах и птицекомбинатах, могут наблюдаться эпидемические вспышки орнитоза. Весьма частые, но ограниченные вспышки болезни наблюдаются в семьях, где содержатся в домашних условиях попуши, канарейки, чижи и др. Заражение происходит контактным, шрогенным путем, а также через экскременты птиц, содержащие большое количество вирусных телец. Инкубационный период болезни длится 7-30 дн, в среднем — 10-14 дн.
МИКОПЛАЗМЕННАЯ ОП вызывается Mycoplasma pneumoniae, которая занимает промежуточное положение между бактериями и, вирусами. Микоплазма относится к группе микроорганизмов, рассматриваемых как бактерии, но не имеющих клеточной стенки. Они образуют различные формы и могут проходить через нормальные бактериальные фильтры.
Заболевание может передаваться капельным путем; возникают эпидемии, особенно в осеннее время. Инкубационный период длится 2-3 нед. Микоплазменные ОП составляют 5-15 % всех ОП, а у лиц в возрасте 5-20 лет их удельный вес возрастает до 30-60 %. Считается, что микоплазменная ОП развивается в первые 3 дня микоплазмоза. Если же пневмония появляется на 5-7-й день от начала микоплазмоза, то она — вторичная бактериальная или микоплазменно-бактериальная. Микоплазменная ОП обычно начинается и протекает как интерстициально-паренхиматозная. Эта ОП оставляет после себя грубые фиброзные изменения, а при паренхиматозном варианте — участки карнификации легочной ткани.
ПНЕВМОЦИСТНАЯ ОП вызывается протозойным микроорганизмом из класса простейших — Pneumocystis carini, pac-пространенным в окружающей среде. Носителями инфекции являются животные (крысы, кролики, кошки, собаки, овцы и др.). Источником инфекции могут быть больные дети, а также взрослые, у которых инфекция протекает латентно. Заражение происходит аэрогенно, о чем свидетельствует наличие на поверхности слизистой оболочки бронхов и в бронхиальном эпителии пневмоцист. Чаще пневмоцистной пневмонией болеют дети, особенно новорожденные и недоношенные. Взрослые болеют реже.
Активная пневмоцистная инфекция возникает в основном у людей с нарушенным иммунитетом, ослабленных тяжелыми заболеваниями (опухолевые поражения кроветворной ткани -лимфогранулематоз, миелоз, лимфаденоз, новообразования и др.) или проводимой терапией (лучевая терапия, иммунодепрессанты, кортикостероиды, антибиотики и др.). В последние годы интерес врачей к пневмоцистной ОП резко возрос в связи с тем, что пневмоциста — наиболее часто встречающийся микроорганизм, вызывающий легочные осложнения при СПИДе. Примерно в 75 % случаев она служит причиной первичной легочной инфекции при СПИДе. Инкубационный период длится в среднем 40 дн.
Для пневмоцистной ОП типичны плазмоклеточная инфильтрация межуточной ткани (отсюда ее старое название — интерстициальная плазмоклеточная пневмония), скопление экссудата с большим количеством пневмоцист в просветах альвеол, бронхиол и мелких бронхов, плазмоклеточная инфильтрация лимфатических узлов корней легких. Процесс почти всегда двусторонний. Вначале отмечается умеренная инфильтрация легочной ткани в области корней легкого,затем развиваются очаговые тени, сливающиеся в крупные участки уплотнения, которые перемежаются с лобулярными вздутиями, при разрыве последних может развиться серповидный пневмоторакс.
РИККЕТСИОЗНЫЕ ОП вызываются группой пневмотропных риккетсий. Это зоонозы с природной очаговостью.
Другое название этих пневмоний — Ку-лихорадка — происходит от начальной буквы наименования провинции Квинсленд (Австралия), в которой впервые в 1937 г. это заболевание было выделено и описано.
Основные носители инфекции — крупный рогатый скот. Заболевание передается чаще всего аэрогенным путем посредством пыли, зараженной риккетсиями. Определенную роль в передаче Ку-лихорадки играют клещи.
Болеют главным образом мужчины среднего возраста — чаще пастухи, скотоводы, работники боен и т. п.
Сама Ку-лихорадка в зависимости от климатических особенностей может протекать в тифоидной, гриппоподобной, бронхопневмонической, ложнобруцеллезной и смешанной формах. В легких при риккетсиозной ОП возникают одиночные дольковые, сегментарные и долевые инфильтраты в одном или обоих легких, чаще в наружных, средних или нижних отделах.
ГРИБКОВЫЕ ОП. Актиномикозная ОП, или актиномикоз легких, является наиболее распространенной по отношению к другим грибковым острым пневмониям.
Возбудитель — лучистый грибок актиномицет, который обычно сапрофитирует в полости рта и пищеварительном тракте. Превращение в патогенную форму происходит в присутствии смешанной микрофлоры (стафилококки, стрептококки, анаэробы) при снижении реактивности организма. Данный путь заражения -эндогенный — по-видимому, является основным.
Заражение человека может происходить также экзогенным путем — при внедрении в организм аэробного спороносного гриба, обитающего в свободной природе, обычно в несвежем сене, соломе, злаках.
Поражение легких вызывается попаданием гриба аэрогенным путем, а также распространением процесса со стороны пищевода, средостения и т. д. С учетом этого возникают различные клинические формы актиномикоза легких — бронхиальная или бронхопульмональная (при аэрогенном заражении), медиастинально-легочная, плеврально-легочная и абдоминально-легочная.
В легких наблюдается картина, характерная для пневмонической инфильтрации, но, как правило, без четкого ограничения по сегментам, нередко появляются признаки распада и расплавления. Вокруг внедрившегося в легочную ткань гриба развивается специфическая гранулема с некробиозом клеток в центре и развитием на периферии волокнистой соединительной ткани, в клетках которой имеются капли жира. Обнаружение в мокроте этих ксантомных клеток может облегчить диагностику актиномикоза. Актиномикоз легочной локализации считается одной из наиболее тяжелых форм заболевания, которая нередко приводит к смертельному исходу.
Гистоплазменная ОП, или острая форма гистоплазмоза легких (ретикулоэндотелиальный цитомикоз), — грибковое заболевание, при котором поражается ретикулоэндотелиальная система. Возбудитель — дрожжеподобный гриб Histoplasma capsulatum. Носителями инфекции являются животные, хронически болеющие гистоплазмозом. Гистоплазма широко распространена в местах обитания летучих мышей и птиц. Замечено, что гистоплазмозом часто болеют лица, связанные с птицеводством и спелеологией.
Заражение может произойти аэрогенным или алиментарным путем, а также через кожные покровы. Дети болеют острой формой заболевания, а взрослые — хронической, при которой продолжительность болезни может исчисляться годами и даже десятилетиями. В легких возникают плотные очаги или инфильтраты с полостями распада (каверны); в последующем на их месте развиваются фиброз и множественные кальцинированные очаги. Могут быть шаровидные плотные инфильтраты с обызвествлениями — гистоплазмы, похожие на туберкулемы.
Кандидамикозная ОП, или кандидамикоз легких, вызывается дрожжеподобными грибами рода Candida, которые обитают у человека в основном на коже и слизистых оболочках как сапрофиты. У практически здорового человека они не вызывают клинических симптомов заболевания, однако при ослаблении организма различными болезнями, авитаминозами и при длительном приеме антибиотиков Candida могут оказывать патогенное действие. Поражение легких грибами Candida в большинстве случаев бывает вторичным и возникает на фоне бактериальных и вирусных ОП, туберкулеза, нагноительных процессов и бронхоэктазов. Реже встречается первичный кандидоз легких. Заражение может быть экзогенным и эндогенным.
Основным источником экзогенного заражения являются больные со свежими формами кандидамикоза кожи и слизистых оболочек или носители, переболевшие ранее. Экзогенным кандидамикозом легких чаще болеют служащие в детских учреждениях, работники кондитерских фабрик, овощных консервных заводов, бань и т. п. Источником эндогенного заражения могут быть грибы, сапрофитирующие на коже и слизистых оболочках и превратившиеся из непатогенных в патогенные. Это обусловлено ослаблением сопротивляемости организма либо значительным изменением микрофлоры, что почти всегда является результатом действия антибиотиков.
Кандидамикоз легких может протекать в острой и хронической форме. Острая форма обычно возникает у детей грудного возраста, хроническая чаще наблюдается у взрослых.
Вторичные ОП при нарушениях кровообращения в малом круге — это застойная, гипостатическая и инфарктная ОП.
ЗАСТОЙНАЯ ОП развивается в “застойном” легком, в котором венозные сосуды переполнены кровью из-за препятствия ее оттоку вследствие пороков сердца, поражения миокарда, нарушения сердечного ритма и др.
Воспалительный процесс локализуется главным образом в межуточной ткани, обусловливая утолщение межальвеолярных и межацинозных стенок с развитием альвеолярно-капиллярного блока. У больных с застойной ОП резко снижаются газообмен и кислородное обогащение крови, циркулирующей в легких. При физической нагрузке у этих больных возникают приступы удушья, а в тяжелых случаях — острый отек легких из-за резкого повышения артериальногодавления и увеличения проницаемости капилляров. Легочная ткань становится отечной, в ее толще возникают более плотные участки размером от 2-3 мм до 2-3 см и более. Последние обусловлены скоплением транссудата и экссудата в альвеолах, ацинусах и дольках. При хроническом застое в центральных отделах легких появляются узелки гемосидероза — клубки гемосидерина, окруженные фиброзной тканью. Корни легких расширяются и становятся однородными. В плевральной полости часто скапливается жидкость — транссудат или экссудат. Иногда выпот может быть и в перикарде.
ГИПОСТАТИЧЕСКАЯ ОП возникает в наиболее низко расположенных отделах легких, в которых венозные сосуды переполнены кровью, скопившейся в силу собственной тяжести. Обычно это нижнезадние отделы легких, где медленный кровоток и плохая вентиляция способствуют суперинфекции.
Гипостатическая ОП чаще наблюдается у пожилых и ослабленных людей, длительное время находящихся в постели. Изменения в легких схожи с изменениями при застойной ОП.
ИНФАРКТНАЯ ОП развивается в зоне инфаркта легкого, который является следствием тромбоэмболии ветвей легочной артерии (ТЭЛА).
ТЭЛА возникает обычно при заносе током крови оторвавшихся тромбов из вен нижних конечностей, таза; частиц тканей при травматическом размозжении костей, распаде опухолей; капель жира, пузырьков воздуха, скоплений микробов, паразитов и др. Размеры инфаркта легкого зависят от характера ТЭЛА и колеблются от нескольких миллиметров до целой доли. На уровне инфаркта легкого могут быть ограниченный фиброзный или геморрагический плевриты. Типичным исходом инфарктной ОП является фиброз.
ВТОРИЧНЫЕ ОП ПРИ НАРУШЕНИЯХ БРОНХИАЛbНОЙ ПРОХОДИМОСТИ (ГИПОВЕНТИЛЯЦИОННЫЕ) возникают в частях легкого (сегменте, доле) с нарушенной вентиляцией вследствие аспирации инородного тела, внутрибронхиальной опухоли, бронхиолита, стеноза бронхов воспалительного происхождения и т. п. Так, например, у больных с центральным раком легкого в ранней стадии развития опухоли возникают повторные пневмонии с интервалом в несколько недель или месяцев. Такая параканкрозная пневмония, возникающая на фоне гиповентиляции, по всем клиническим признакам схожа с сегментарной или долевой первичной пневмонией.
ВТОРИЧНЫЕ ОП ПРИ ГНОЙНЫХ ЗАБОЛЕВАНИЯХ (СЕПТИЧЕСКИЕ МЕТАСТАТИЧЕСКИЕ ОП) вызываются гематогенным заносом из септических фокусов, находящихся в организме. Чаще всего эти пневмонии вызываются стафилококком и значительно реже — стрептококком, еще реже — другими представителями микробной флоры, например энтерококками, кишечной палочкой и др.
Обычно септические очаги известны — это может быть фурункул, карбункул, остеомиелит, гнойный аднексит и т. д. Реже вторичная септическая пневмония является первым свидетельством септического процесса, а первоисточник в течение определенного времени не проявляется как явно гнойный очаг.
Гематогенный путь заноса инфекционных эмболов обусловливает множественность пневмонических очагов и поражение обоих легких. Кроме того, на течении процесса сказывается и то обстоятельство, что эмболии и занос патогенных микробов в легкие могут происходить повторно. Легочные инфильтраты при септической ОП склонны к распаду, в легких длительное время сохраняются кистевидные тонкостенные полости.
АСПИРАЦИОННЫЕ ОП образуются вследствие аспирации различных веществ в бронхиальное дерево с последующим развитием и размножением патогенных микроорганизмов в легочной ткани. Особое значение при этом имеет аспирация крови, являющейся идеальной средой для роста микробов. В качестве этиологического агента приобретенной вне стационара аспирационной ОП преобладают анаэробные бактерии, в то время как приблизительно в 2/3 случаев госпитальной ОП (приобретенной в лечебном учреждении) обнаруживаются грамотрицательные патогенные микроорганизмы.
Аспирационные ОП обычно возникают у больных с угнетением центральной нервной системы (при обезболивании, кардио-респираторных расстройствах, передозировке наркотиков, эпилепсии), нарушением акта глотания (ахалазия, дивертикул
Зенкера, склеродермия или рак пищевода) и тяжелой нервно-мышечной слабостью или параличом (боковой амиотрофический склероз, квадриплегия).
Для аспирационной ОП характерна локализация в задних сегментах верхних долей и верхних сегментах нижних долей. Площадь пневмонического поражения зависит в первую очередь от калибра бронха, обтурированного аспирированными массами. В случае полного закрытия просвета бронха вначале развивается ателектаз, а затем уже в области ателектаза — пневмонический инфильтрат с абсцедированием и т. д. Если просвет бронха полностью не перекрывается, то через 1-2 дн в зоне гиповентиляции развивается пневмонический фокус с последующим распадом.
Клиническая картина и диагноз. Этиологическая и патогенетическая разнородность обусловливает особенности клинической картины каждой ОП, которая зависит от объема инфильтративного уплотнения легочной ткани и сопутствующих легочных симптомокомплексов (бронхоспастического обтурационного дистелектаза, легочного нагноения, воспалительного поражения плевры, дыхательной недостаточности и др.), а также от выраженности общих воспалительных и интоксикационных явлений, реакций сердечно-сосудистой, нервной и других систем. В то же время для всех ОП наиболее характерны симптомокомплексы инфильтративного уплотнения легочной ткани, бронхиальной обструкции (при распространении воспалительного процесса на мелкие бронхи и бронхиолы) и эндогенной интоксикации.
Основные жалобы больных ОП — кашель, выделение мокроты, боли в грудной клетке и одышка. Интенсивность кашля и его характер зависят от этиопатогенетических особенностей ОП. В первые дни болезни кашель, как правило, малопродуктивный (сухой), по мере развития пневмонии и появления мокроты он смягчается, а затем полностью исчезает. Мокрота может содержать прожилки крови или быть ею равномерно окрашенной. При крупозной пневмонии она имеет оттенок ржавого железа, в таких случаях говорят о “ржавой” мокроте. Неприятный гнилостный запах мокроты свидетельствует либо о распаде и нагноении воспалительного инфильтрата, либо о тяжелом осложнении -абсцессе или гангрене легкого.
Боли в грудной клетке при ОП бывают поверхностными и глубокими. Поверхностные боли обусловлены чаще межреберной миалгией и невропатией. Они ограничены зоной отдельных межреберных мышц или нервов; усиливаются при пальпации межреберий и при некоторых движениях, могут иметь связь с дыханием. Глубокие боли обычно плеврального происхождения, бывают очень интенсивными, при поражении диафрагмальной плевры иногда создают картину “острого” живота. Одышка как субъективное ощущение нехватки воздуха может наблюдаться при частом продолжительном мучительном кашле, сильных болях в грудной клетке, из-за которых больной не может осуществить полноценный вдох, уменьшении дыхательной поверхности легких в случае массивного воспаления легочной ткани.
К дополнительным жалобам, которые обычно обусловлены интоксикацией, относятся общая слабость и потливость различной степени, повышение температуры тела (нередко до 39-40° С), снижение аппетита вплоть до полной его потери (анорексия), тошнота, иногда рвота. У ослабленных больных и пожилых людей бывают расстройства сознания.
При осмотре определяются некоторые клинические признаки дыхательной недостаточности: цианоз, учащенное поверхностное дыхание, участие в дыхании вспомогательной мускулатуры. Если в патологический процесс вовлекается плевра, то об этом можно догадаться по характерной вынужденной позе больного — он лежит на больном боку или из-за болей сдерживает дыхание, прижимает руками грудную клетку на стороне поражения и т. д.
При физикальном исследовании легких в случае обширного воспаления, расположенного неглубоко от поверхности грудной клетки, можно выявить признаки инфильтративного уплотнения легочной ткани — отставание при дыхании грудной клетки в области очага поражения, укорочение перкуторного звука, усиление голосового дрожания и бронхофонии, жесткое, бронхиальное или ослабленное дыхание, влажные звонкие мелкопузырчатые хрипы и крепитацию.
Различаются четыре степени тяжести ОП. Легкая (абортивная) ОП протекает при отсутствии или минимальных признаках интоксикации, с незначительными признаками нарушения дыхания. Лабораторные показатели активности воспалительного процесса нерезко выражены (минимальные).
Среднетяжелая ОП характеризуется фебрильной температурой, умеренной интоксикацией (головная боль, слабость), нерезко выраженной дыхательной недостаточностью преимущественно при физической нагрузке, реакцией сердечно-сосудистой системы (тахикардия, гипотония), умеренно выраженными лабораторными показателями активности воспалительного процесса.
Тяжелой ОП свойственны выраженная интоксикация с гиигргмией, адинамия, респираторные и гемодинамические нарушения, осложнения, неблагоприятно влияющие на прогноз шГюмеиания, но непосредственно не угрожающие жизни больною (пира- и метапневмонический плеврит с выпотом, миокардит и др.).
Краппе тяжелая ОП проявляется резко выраженной ниток* i пк.щисй с церебральными и неврологическими нарушениями (острый психоз, сопорозные состояния с расстройствами дыхания, менингит и т. п.); острой тяжелой и рецидивирующей сосудистой и сердечно-сосудистой недостаточностью (коллапс, сердечная астма, отек легких); резко выраженной дыхательной недостаточностью с нарушением кислотно-основного состояния и гипоксемией; массивными и множественными деструктивными изменениями в легких.
Затяжной вариант течения ОП, к сожалению, в настоящее время отмечается у каждого 3-4-го больного. За последние 12-15 лет несколько изменилось клиническое течение ОП. Они стали протекать более торпидно, без выраженной лихорадки и других проявлений интоксикации, а также без заметных физикальных изменений в легких, чем приблизились к клиническому проявлению “мягкого” туберкулезного инфильтрата легких.
Причины затяжного течения ОП разнообразны: несвоевременное начало лечения, неправильно проводимая терапия, изменение иммунобиологических реакций в процессе заболевания. К затяжному течению предрасполагают сопутствующие болезни органов дыхания (в частности, верхних дыхательных путей или хронические бронхиты), латентно протекающая очаговая инфекция (хронический тонзиллит, синусит, холецистит и др.). Затяжной характер болезнь часто приобретает у ослабленных больных (особенно пожилого возраста) со сниженной иммунобиологической реактивностью организма и нередкими сопутствующими заболеваниями (сахарным диабетом, хронической сердечной недостаточностью и др.).
У большей части больных с ОП в периферической крови имеются неспецифические признаки инфекционного воспаления — нейтрофильный лейкоцитоз, сдвиг лейкоцитарной формулы влево (иногда до юных форм и миелоцитов), токсическая зернистость цитоплазмы нейтрофилов, лимфопения и эозинопения.
Наличие инфекционного процесса подтверждается также биохимическими показателями острой фазы воспаления (острофазовые показатели): повышением уровня глобулинов, увеличением содержания альфа-2- и гамма-глобулинов, СРП, сиаловых кислот, увеличением в крови уровня лактатдегидрогеназы (ЛДГ) и ее изоферментов.
Рентгенологическими признаками ОП являются инфильтрация легочной ткани, на фоне которой могут образовываться полости, микроабсцессы, появление в плевральной полости на стороне поражения плеврального выпота. Для ОП характерно реактивное увеличение тени корня легкого.
При исследовании функции внешнего дыхания выявляется рестрикгивный тип нарушения вентиляции альвеол, для которого характерно уменьшение ЖЕЛ и МВЛ. Проба с бронхорасширяющими препаратами отрицательная.
Оценивая результаты лабораторных и инструментальных исследований больных ОП, нужно учитывать, что более чем в 70 % случаев клиническое и рентгенологическое выздоровление при острой пневмонии не совпадает с морфологическим. Клиническое выздоровление больных наступает раньше, чем исчезают органические изменения в легких. Часть больных острой пневмонией по различным причинам выписываются из стационара в стадии неполного клинического выздоровления, которое может быть выявлено в результате последующего рентгенологического наблюдения. Критериями выздоровления при пневмониях являются: нормализация самочувствия и состояния больного, исчезновение клинических, рентгенологических и лабораторных признаков воспалительного процесса. Для оценки выздоровления используются и другие методы (изучение в динамике показателей внешнего дыхания, изменений крови, иммунологические исследования и др.).
Дифференциальный диагноз острой пневмонии необходимо проводить прежде всего с острым бронхитом, инфильтративно-пневмонической формой туберкулеза, экссудативным плевритом, раком легких, инфаркт-пневмонией.
Лечение. Лечение ОП должно быть комплексным и, как правило, в стационаре. В первую очередь это касается больных крупозной и очаговой пневмонией с инфекционно-токсическими явлениями, дыхательной и сердечной недостаточностью. Больные с неосложненной очаговой пневмонией нетяжелого течения могут лечиться на дому при условии соблюдения всех правил больничного режима (стационар на дому). В течение всего периода лихорадки и выраженных симптомов интоксикации показаны постельный режим, обильное питье (до 1,5-2 л в сутки), механически и химически щадящее питание с ограничением поваренной соли и достаточным количеством витаминов, особенно А и С. Диета должна состоять из разнообразных, легкоусвояемых продуктов, содержащих достаточное количество белков, жиров, углеводов и микроэлементов. В острый период лихорадки рекомендуется питье слегка подкисленной или минеральной воды, фруктовых соков, витаминных настоев. В первые дни Сюлезни питание состоит из бульонов, компотов и фруктов.
Комплексное лечение больных ОП включает применение антибактериальных препаратов, средств, повышающих иммунобиологическую реактивность организма, восстановление дренажной функции бронхов, физические методы лечения и лечебную физкультуру.
Основой лекарственной терапии является антибактериальная химиотерапия, которая должна: 1) начинаться как можно раньше, еще до выделения и идентификации возбудителя болезни,2) проводиться под клиническим и, если возможно, бактериологическим контролем (с исследованием мокроты или промывных вод бронхов перед назначением антибактериальных средств) с определением возбудителя болезни и его чувствительности к антибиотикам; 3) назначаться в достаточных дозах с интервалами введения, обеспечивающими создание лечебной концентрации препаратов в крови и легочной ткани; 4) проводиться в период разгара болезни при высокой температуре и интоксикации не менее 7-12 дн, а при клинико-рентгенологических признаках рассасывания воспалительной инфильтрации в легочной ткани, нормализации нейтрофильного сдвига формулы крови и температуры в течение 3 дн одномоментно отменяться без постепенного снижения дозы. При отсутствии клинического эффекта от применяемого антибиотика в течение 3 дн следует заменить его другим антибиотиком или другим этиотропным химиопрепаратом с учетом выделенных микробов и их чувствительности к антибиотикам.
В большинстве случаев целесообразна монотерапия антибиотиками, сульфаниламидными препаратами или другими этиотропно действующими средствами, например нитрофуранами (фурагином) или производными хиноксалина (хиноксидином, диоксидином). Нежелательно одновременно применять антибиотики бактерицидного и бактериостатического действия, а также несколько антибиотиков широкого спектра действия или с однотипным токсическим влиянием. Это может привести к тяжелым, а иногда и необратимым последствиям в виде токсического повреждения разных органов и систем организма или к развитию тяжелого дисбактериоза.
Пневмококковые инфильтраты легочной ткани хорошо поддаются лечению бензилпенициллином. Водный раствор натриевой соли бензилпенициллина применяется внутримышечно по 0,25-0,5 г 4 раза в день. Кроме бензилпенициллина на пневмококки действуют цефалоспорины (до 2-6 г/сут), линкомицин (до 1 г/сут), макролиды (до 2 г/сут), сульфаниламиды короткого действия (по схеме), бисептол (по 2 табл. в день), рифампицин (0,6-1,2 г/сут).
Стрептококковые и стафилококковые легочные инфильтраты также хорошо поддаются лечению бензилпенициллином. Кроме того, рекомендуется использовать полусинтетические пенициллины (ампициллин 1-10 г/сут, оксациллин 3-8 г/сут, метициллин 1-10 г/сут), цефалоспорины, макролиды, левомицетин, линкомицин, фузидин (1,5 г/сут).
Легочные инфильтраты, вызванные клебсиелловыми (энтеробактериальными) и синегнойными (псевдомонадными) грамотрицательными палочками, лучше всего лечить аминогликозидами (стрептомицином или канамицином по 1-2 г/сут, гентамицином по 240-320 мг/сут) с левомицетином или тетрациклином, производными хиноксалина — диоксидином (1 % раствор внутривенно по 10 мл или в аэрозоле по 5 мл 2 раза в день), хиноксидином (в таблетках по 0,25 г 3 раза в день), ципробаем (ципрофлоксацином) по 0,25 г 2 раза в день, таривидом (офлоксацином) по 0,2 г 2 раза в день.
Микоплазменные легочные инфильтраты хорошо поддаются лечению тетрациклином (0,1 г 2-3 раза в день) или эритромицином (0,25 г 4 раза в день). При участии вирусов гриппа и парагриппа, аденовирусов и др. в воспалительном инфильтративном процессе (вирусно-бакгериальные ассоциации) необходимо назначать противовирусное лечение — противогриппозный гаммаглобулин, нормальный иммуноглобулин человека, интерферон человеческий лейкоцитарный, ремантадин, 5 % раствор аминокапроновой кислоты, ДНКазу, РНКазу. Наряду с этим эффективно использование препаратов йода (йодинол — орошение слизистой оболочки носа и носоглотки; раствор Люголя — смазывание слизистой оболочки глотки; полоскание глотки — 6 капель настойки йода на стакан воды; вдыхание паров 5 % йодной нистойки). Уменьшают репродукцию вируса уротропин (40 % раствор внутривенно и в таблетках), препараты хлористого кальция (10 % раствор хлорида или глюконата кальция внутривенно), ингаляции фитонцидов (сок чеснока или лука в разведении 1:20, 1:10, 1:5), орошение слизистой оболочки носа и глотки 10-20 % раствором этилового спирта.
Противовирусные средства сочетаются с мочегонными препаратами (лазиксом, фуросемидом, гипотиазидом) и эуфиллином, что уменьшает токсический отек легочной ткани, пораженной вирусом.
Для лечения грибковых пневмоний, а также для профилактики и лечения кандидоза при длительном применении антибиотиков показаны нистатин, леворин, амфотерицин и амфоглюкамин.
При вялом, затяжном течении острой пневмонии показаны производные нитрофурана: фуразолин по 0,1 г 3-4 раза в день, фурагин растворимый по 300-500 мл 0,1 % раствора (0,3-0,5 г) внутривенно капельным методом в течение 3-4 ч ежедневно или через день. В комплексную терапию включаются противовоспалительные средства: ацетилсалициловая кислота по 0,5 г 3 раза в день, 2-3 нед, кальция хлорид по 1 ст. ложке 5-10 % раствора 3-4 раза в день или 10 мл 10 % раствора внутривенно ежедневно. При выраженной бактериальной аллергии назначаются десенсибилизирующие средства — димедрол, супрастин, тавегил. При тяжелом течении пневмонии с выраженной интоксикацией, при оГмиирности поражении, особенно лицам, страдающим хроническим обструктивным бронхитом, показан короткий курс стероидных гормонов (преднизолон по 20-25 мг в день с постепенным снижением дозы по 5 мг). При мучительном сухом кашле можно назначить кодеин, этилморфина гидрохлорид (дионин). Дин улучшения дренажной функции бронхов применяются отхаркивающие и муколитические средства (ипекакуана, термопсис, алтей, 3 % раствор йодида калия), протеолитические ферменты.
Больным с выраженной одышкой и цианозом показаны длительные ингаляции увлажненного кислорода (кислородные палатки, маски).
Присоединение бронхоспастического синдрома требует применения бронхоспазмолитических препаратов (теофедрина по 1/2 табл. 2-3 раза в день, эфедрина по 0,025 г 2-3 раза в день). Больным с затяжным течением острой пневмонии, особенно на фоне хронического обструктивного бронхита, в специализированном стационаре проводится санационная бронхоскопия с аспирацией воспалительного секрета из пораженных бронхов, промыванием их противовоспалительными растворами, протеолитическими ферментами с введением антибиотиков и бронхоспазмолитиков непосредственно в зону поражения. При выраженных симптомах интоксикации применяются внутривенно капельно гемодез, полиглюкин, 5-10 % раствор глюкозы. При затяжных пневмониях для повышения иммунобиологической реактивности и стимуляции рассасывания воспалительных очагов назначаются аутогемотерапия, инъекции алоэ, стекловидного тела, дробные переливания крови, пентоксил (по 0,2 г 3-4 раза в день), метилурацил (по 0,5 г 3-4 раза в день), оротат калия (по 0,5 г 3-5 раз в день), неробол (по 0,005 г 2-3 раза в день), женьшень, элеутерококк колючий, лимонник китайский, витамины.
Используются безаппаратная физиотерапия (круговые банки, горчичники, аппликации парафина, озокерита, лечебной грязи, полуспиртовые согревающие компрессы). После нормализации температуры тела можно назначить коротковолновую диатермию, индуктотермию, электрическое поле УВЧ, электрофорез йода, алоэ, кальция хлорида, дионина и натрия салицилата (при шуме трения плевры). В лечении легочного инфильтрата важны различные физические методы (лечебная физкультура и физиотерапия). Занятия лечебной физкультурой в остром периоде выполняются в положении лежа на больном боку с ограничением глубины вдоха и направлены на активизацию дыхания в здоровом легком и периферического кровообращения. По мере улучшения общего состояния (уменьшение болевых ощущений в груди и кашля) применяются дыхательные упражнения с удлиненным выдохом, с одновременным надавливанием рукой на грудную клетку с легким вибрационным массажем. На выдохе больной кашляет, что способствует более полному расправлению легкого. Затем нагрузка постепенно увеличивается, в комплекс включаются динамические дыхательные упражнения.
ПНЕВМОСКЛЕРОЗ. Пневмосклероз — образование в легких новых элементов соединительной ткани и (или) ее уплотнение в течение или в исходе различных заболеваний легких. При этом могут наблюдаться склерозы воспалительного происхождения (асептического и инфекционного), постнекротические, дисциркуляторные (при хроническом застое крови и лимфы) и развивающиеся в исходе дистрофического процесса. Развитию пневмосклероза сопутствует формирование эмфиземы легких. Пневмосклероз может возникать в любом возрасте, чаще у мужчин. Патогенез. Морфологически Пневмосклероз характеризуется прорастанием соединительной тканью легочных альвеол, бронхиол, утолщением альвеолярных перегородок, срастанием и рубцеванием альвеол, капилляров и мелких сосудов, запустенанием и редукцией капиллярного русла, развитием в стенках альнеол множества фибробластов, разрушением эластических иолокон, возникновением участков ателектаза, чередующихся с запустеванием альвеол или заполнением их экссудатом. Образование соединительной ткани происходит клеточным путем, реже без участия клеток (гиалиноз). По топографии пневмосклероза раишчаются карнификация, склероз интерстиция (межальвеолнрные перегородки, перибронхиальные и периваскулярные прослойки соединительной ткани), склероз мышечно-эластических структур стенок сосудов и бронхов, а также сочетания указанных причин. Карнификация чаще наблюдается при крупозной пневмонии и является исходом организации плотного экссудата, богатого фибрином, в просвете альвеол, альвеолярных ходов, бронхиол и мелких бронхов (в ходе рассасывания и организации фибрина просвет респираторных отделов заполня ется созревающей соединительной тканью). Интерстициальный склероз межальвеолярных перегородок развивается вследствие пролиферации септальных клеток при подострых и хронических воспалительных процессах в легких, при некрозах, которые вы зывают воспалительную реакцию в окружающих живых тканях, при хроническом застойном полнокровии, выражающемся в индурации легких. .
Склероз мышечно-эластических структур стенок сосудов и бронхов (фиброзный интерстиций) развивается в связи с выраженным воспалением бронхиальных стенок и перибронхия, что типично для бронхов среднего и мелкого калибра при бронхоэктазах и абсцессах легких.
В зависимости от выраженности разрастания соединительной ткани Пневмосклероз может обозначаться также как фиброз и цирроз легких. Фиброз легких — более выраженная степень склероза. Цирроз легких — крайняя степень развития склероза с уплотнением легочной ткани, плевры, смещением органов средостения и сторону поражения. С клинической точки зрения пневмосклероз представляет собой сложный полиморфный клинико — анатомо-функциональный симптомокомплекс, проявления которого в каждом конкретном случае зависят от выраженности склеротических изменений, тяжести и активности сопутствующих заболеваний (бронхит, бронхоэктазия, эмфизема и т. д.) и выраженности легочной и сердечной недостаточности.
Клиническая картина и диагноз. Диффузный пневмосклероз имеет клинические симптомы заболевания, следствием которого он является (хронический бронхит, пневмокониозы, диссеминированный туберкулез легких, синдром Хаммена — Рича и др.). Главное проявление диффузного пневмосклероза — одышка, которая вначале возникает при физической нагрузке, быстрой ходьбе, а в последующем и в покое. В результате снижения эластичности легких затруднен вдох, а постепенно углубляющаяся гипоксия приводит к еще одному характерному признаку диффузного пневмосклероза — цианозу. На ранних стадиях болезни отмечается сухой кашель с выделением слизистой, а в последующем гнойной мокроты. Возможны кровохарканье и неопределенные боли в груди.
Стетоакустические феномены (ослабленное, местами жесткое дыхание, рассеянные сухие и влажные мелкопузырчатые хрипы) появляются только при выраженном процессе. Перкуторный звук, если пневмосклерозу сопутствует эмфизема легкого, притупленный с тимпаническим оттенком.
Ограниченный пневмосклероз обычно протекает без клинических симптомов и длительное время проявляется только ослабленным или жестким дыханием, влажными хрипами на ограниченном участке грудной клетки, локальным укорочением перкуторного звука. Как правило, нет изменений в периферической крови, но у некоторых больных СОЭ увеличена до 20-30 мм/ч. В мокроте иногда обнаруживаются единичные эритроциты или их небольшие скопления. Ограниченный пневмосклероз, сопровождающийся бронхоэктазией, приобретает черты бронхоэктатической болезни. Основу диагностики пневмосклероза составляет рентгенологическое исследование, так как клинические проявления часто отсутствуют — процесс может протекать бессимптомно и доброкачественно, сопровождаясь иногда лишь незначительными нарушениями функции дыхания. Рентгенологически в зоне поражения определяются усиление и деформация легочного рисунка, снижение прозрачности легочных полей, грубые тяжи, исходящие из корня и постепенно исчезающие к периферии, утолщение плевры и подтягивание купола диафрагмы вверх, смещение органов средостения в сторону большего поражения. При ателектатическом сегментарном пневмосклерозе определяется сегментарный ателектаз, при опухолевидном — округлая тень, иногда окруженная фиброзными тяжами. При пневмосклерозе нарушается функция внешнего дыхания по рестриктивному типу, а в последующем развивается легочно-сердечная недостаточность. Учащается дыхание в покое, снижаются МВЛ и ЖЕЛ, увеличиваются МОД и остаточный объем.
Дифференциальный диагноз пневмосклероза чаще всего проводится с пневмокониозоми, туберкулезом легких, интерстициольной пневмонией, хроническим бронхитом, бронхоэктазоми и опухолями органов дыхания.
Лечение направлено прежде всего на заболевание, которое вызвало пневмосклероз. При далеко зашедших, необратимых изменениях в легких — лечение симптоматическое. Так, для улучшения бронхиальной проходимости применяются отхаркивающие и разжижающие мокроту средства, при одышке — бронхоспазмолитические средства (эуфиллин и др.), при осложненном течении (частые пневмонии, бронхиты, бронхоэктазы) — антибактериальная и противовоспалительная терапия, при недостаточности кровообращения — сердечные гликозиды, при выраженных аллергических проявлениях — глюкокортикоиды. Широко используются оксигенотерапия, ЛФК, массаж грудной клетки, физиотерапия. При ограниченных пневмосклерозах, фиброзах и циррозах (сегмент, доля), появлении деструкции и нагноения возможно хирургическое лечение (удаление пораженного участка легкого).
ПНЕВМОТОРАКС. Пневмоторакс — патологическое состояние, которое характеризуется скоплением воздуха между висцеральной и париетальной плеврой. Пневмоторакс может быть односторонним или двусторонним, в зависимости от объема газового пузыря — частичным или полным (тотальным), при этом легкое спадается (коллабируется) частично или полностью. Он может быть открытым, если атмосферный воздух при вдохе свободно поступает в плевральную полость, а при выдохе — выходит из нее. В случае затруднения эвакуации воздуха во время выдоха и поступления с каждым вдохом в плевральную полость новой порции атмосферного воздуха давление в ней постепенно нарастает. Такой пневмоторакс называется клапанным, или вентильным.
Если отверстие, через которое воздух поступает в плевральную полость, закрылось и поступивший воздух не имеет выхода, пневмоторакс называется закрытым.
В зависимости от причины все пневмотораксы делятся на травматические и искусственные. В практической деятельности терапевта чаще приходится иметь дело со спонтанным пневмотораксом, т. е. скоплением воздуха, не связанным с механическим повреждением легких или грудной клетки в результате травмы или врачебных манипуляций. Его причинами могут быть деструкция легочной ткани вследствие абсцесса, гангрены или рака легкого; прорыв туберкулезной или бронхоэктатической каверны, карциномы, дивертикула пищевода, поддиафрагмального абсцесса; разрыв буллы при эмфиземе легких, кисты легкого или плевры при ее приобретенной или врожденной конституциональной неполноценности и др.
Патологически измененные легочная ткань и висцеральная плевра легко разрываются при сильном кашле, глубоком вдохе, натуживании при значительном физическом усилии, быстром наклоне туловища, смехе, чиханье и т. п.
Появление воздуха в плевральной полости значительно повышает внутриплевральное давление. В результате наступает спадение (коллапс) ткани, влекущее за собой быстрое нарушение газообмена и легочной перфузии. Возникает клиническая картина острой дыхательной недостаточности. Вследствие альвеолярной гипоксии возникает острая легочная гипертензия, которая создает повышенную нагрузку на правый желудочек. Смещение средостения в здоровую сторону нередко приводит к перегибу и сдавлению в нем больших кровеносных сосудов. Эти явления, усугубляемые легочной гипертензией, ведут к развитию острой правожелудочковой сердечной недостаточности.
Клиническая картина и диагноз. Клинические проявления спонтанного пневмоторакса характеризуются в основном симптомами острой дыхательной и правожелудочковой сердечной недостаточности.
Больные жалуются на внезапно возникшую, нередко среди полного здоровья, колющую боль в груди на стороне поражения, которая может иррадиировать в шею, руку, эпигастральную область, одышку, сухой кашель, сердцебиение. Выраженность одышки зависит от объема воздуха в плевральной полости, степени спадения легкого и смешения органов средостения. Наиболее тяжело протекает спонтанный пневмоторакс с вентильным механизмом развития и полным спадением легкого. Поскольку одышка при спонтанном пневмотораксе смешанного характера (легочная и сердечная), она нередко сопровождается чувством страха смерти.
При осмотре больного обращают на себя внимание учащенное поверхностное дыхание, покрытая холодным потом кожа, диффузный цианоз. На стороне поражения может увеличиться объем грудной клетки. Межреберные промежутки становятся расширенными и сглаженными, а в отдельных случаях выбухают, ключица и лопатка стоят выше. При дыхании пораженная половина грудной клетки отстает от здоровой. При сильных болях в грудной клетке появляется брюшное (диафрагмальное) дыхание. Голосовое дрожание, как и бронхофония, ослаблено или полностью исчезает, что объясняется наличием массы воздуха, поглощающей чвуковые колебания, между легкими и грудной стенкой
При перкуссии на стороне поражения выявляется высокий тимпанический звук. Если перкутировать по металлическому плессиметру металлическим предметом (палочкой, ребром монеты), то тимпанический перкуторный звук приобретает металлический оттенок, напоминая звук при ударе по металлическому пустому сосуду. Металлический оттенок тимпанического звука обусловлен резонансом в гладкостенной плевральной полости, наполненной воздухом.
При открытом пневмотораксе, когда имеется узкое щелевидное сообщение плевральной полости с бронхом, перкуторный звук может напоминать “шум треснувшего горшка”.
Аускультативно выявляются ослабление или отсутствие везикулярного дыхания. При открытом пневмотораксе можно выслушать грубое бронхиальное дыхание, имеющее металлический оттенок. Над здоровым легким определяется патологически усиленное везикулярное дыхание. Рентгенологические признаки спонтанного пневмоторакса — относительно большое пристеночное просветление без легочного рисунка; четкая граница между спавшимся легким и воздухом в плевральной полости, которая соответствует изображению висцеральной плевры; смещение органов средостения в здоровую сторону, а купола диафрагмы на стороне поражения книзу. На электрокардиограмме возможно отклонение электрической оси вправо, увеличение амплитуды зубца Рн снижение амплитуды зубца Тъ отведениях II и III. Плевральная пункция с манометрией позволяет диагностировать клапанный пневмоторакс, для которого характерны положительные, постепенно нарастающие цифры внутриплеврального давления.
Лечение. При возникновении спонтанного пневмоторакса необходимо провести неотложные мероприятия в условиях торакального или специализированного пульмонологического стационара. Для уменьшения болей и предотвращения возможного плевропульмонального шока вводятся 1-2 мл 1 % раствора морфина под кожу. При клапанном, субтотальном и тотальном спонтанном пневмотораксе, осложненном выпотом, производится пункция плевральной полости с откачиванием воздуха и жидкости. Дренажная трубка вводится через троакар лучше всего во втором межреберье спереди или в третьем — в подмышечной области. При небольшом по объему закрытом спонтанном пневмотораксе (воздух занимает менее 25 % объема плевральной полости) без выраженного нарушения дыхания и сердечной деятельности коллабированное легкое может расправиться самостоятельно; в таких случаях показано лишь консервативное лечение (покой, симптоматические, обезболивающие средства).
РАК ЛЕГКОГО, МЕТАСТАТИЧЕСКИЕ ОПУХОЛИ ЛЕГКИХ. Рак легкого первичный — неоднородная группа злокачественных эпителиальных опухолей легкого, возникших из эпителия бронха, слизистых желез его стенки (бронхиальный рак) или из альвеолярных клеток (собственно легочный рак) и характеризующихся агрессивным ростом, ранним и обширным метастазированием. В зависимости от локализации опухоли в легком выделяются: 1) центральный (прикорневой) рак, исходной локализацией которого являются сегментарные, долевые и главные бронхи;
2) периферический рак, развивающийся из мелких бронхов и бронхиол периферической зоны. В группе центрального рака выделяются эндобронхиальные и перибронхиальные опухоли. Последние могут расти в виде узла или разветвляться по ходу бронха. Периферическому раку легкого присуща узловая форма роста.
Метастатические опухоли легких обычно являются вторичными, поскольку первичный очаг чаще всего расположен за пределами легких — в матке, почке, скелете, яичке, коже, щитовидной железе, молочной железе, яичнике, желудке и др.
Значительно чаще раком легких болеют мужчины (женщины болеют в 5-6 раз реже мужчин). Метастатические опухоли легких встречаются в 25-30 % всех случаев опухолевых заболеваний.
Главным моментом в этиологии рака легкого считается действие канцерогенов (урбанизация, длительные профессиональные контакты с пылью, содержащей никель, кобальт, железо, асбест, висмут, мышьяк, производственные смолы и сажу). Значительная роль отводится курению табака (15-20 и более сигарет или папирос, выкуриваемых ежедневно, увеличивают частоту рака легких в 7 раз и более). Способствуют развитию рака хронические заболевания легких (туберкулез, хронический бронхит, рубцовое изменение легочной ткани и др.) и пороки их развития, облучение радиоактивными веществамии рентгенологическими лучами более допустимых норм, продолжительный контакт (не менее года) с профессиональными вредностями.
В патогенезе рака легких ведущая роль отводится нарушению и извращению регенерации бронхиального эпителия. Чаще поражается раком правое легкое, передние сегменты его верхней доли. Исходной локализацией опухоли обычно являются устья сегментарных ветвей бронхиального дерева. По мере прогрессирования заболевания в процесс вовлекаются все более крупные бронхи. По виду преимущественного роста раковой опухоли различаются несколько форм рака легкого: 1) разветвленная, когда, возникнув в стенке бронха, раковая опухоль стелется вдоль бронхов; 2) пневмониеподобная, когда опухолевые клетки, разрастаясь, заполняют альвеолы, сохраняя межальвеолярные перегородки; 3) узловатая, когда опухоль растет с образованием узла преимущественно эндобронхиально или экзобронхиально.
Рак легкого метастазирует по лимфатическим путям в лимфатические узлы корня, трахеи, средостения (бифуркационные) и плевру; гематогенным путем — в кости, головной мозг, печень, надпочечники.
Большое практическое значение имеет деление рака легкого по гистологической структуре на две большие группы: мелкоклеточный рак и немелкоклеточный рак (все остальные формы). Мелкоклеточный рак легкого отличается высокой биологической активностью и склонностью к быстрому метастазированию. Клиническая картина и диагноз. Разнообразие макроскопической картины рака легкого обусловлено различными направлениями роста первичной опухоли и вторичных изменений ; соответственно проявляется сложной и многообразной клинико-рентгенологической картиной. Каждой анатомической форме рака свойственна своя клиническая картина, несколько отличная от других по характеру и срокам появления тех или иных симптомов, длительности их существования, что вызвано прежде всего морфологическим субстратом опухоли.
Начальные признаки рака легких весьма часто, на первый взгляд, не имеют прямого отношения к поражению органов дыхания. Больные в этих случаях обращаются к различным специалистам не онкологического или не пульмонологического профиля, долгое время у них обследуются и, естественно, неправильно лечатся.
Абсолютное большинство больных в начальном периоде жалуются на немотивированную общую слабость, субфебрилитет. Иногда первым симптомом может быть кожный зуд или возникновение дерматита на любом участке тела, а у больных пожилых людей — внезапное появление ихтиоза или наростов на коже. Другими кожными проявлениями рака легкого у лиц в возрасте 40 лет и старше могут быть папиллярно-пигментная дистрофия и ползучая эритема. Указанные кожные проявления рака легкого обусловлены неспецифическим или аллергическим действием опухоли.
У больных раком легкого бывают отеки, мышечная слабость, внешние признаки синдрома Иценко-Кушинга, что обусловлено выделением раковыми клетками АКТГ и АКТГ-подобных веществ. Если раковая опухоль секретирует антидиуретический гормон, то развиваются симптомы гипонатриемии — анорексия, рвота, нарушение деятельности центральной нервной системы.
В случае продукции раковыми клетками легкого вещества, близкого к гормону паращитовидной железы, наблюдаются признаки нарушения обмена кальция — гипокальциемия: вялость, мышечная слабость, рвота, иногда нарушение речи и зрения. При раке легкого бывают также гиперсеротонинемия и локализованные гипертрофические остеоартропатии (системные оссифицирующие периоститы). Последние часто бывают первыми проявлениями рака, особенно у курящих мужчин старше 50 лет. Эти больные жалуются на быстро развивающиеся, очень болезненные утолщения на концах пальцев рук и ног. В отличие от “пальцев Гиппократа” (пальцы в виде барабанных палочек), которые формируются постепенно и довольно длительно при хронических заболеваниях легких, печени, сердца и др., остеоартропатические изменения при раке легкого возникают быстро. Периостальные наслоения наблюдаются, как правило, в трубчатых костях: лучевой, больше- и малоберцовой. В далеко зашедших стадиях поражаются фаланги, плюсневые и пястные кости, кости таза, позвоночник. Эти костные изменения являются результатом интоксикации организма и влияния нервно-рефлекторных факторов.
Нередко при раке легкого возникают тромбозы и тромбофлебиты блуждающего и часто рецидивирующего характера. У некоторых больных задолго до обнаружения рака легкого отмечаются патологические изменения со стороны ЦНС. Это могут быть корковые нарушения, проявляющиеся головокружением и нарушениями координации движения; нередко — прогрессирующая деменция (слабоумие). Изменения возникают быстро, и в течение 1-2 нед больной полностью лишается способности стоять или ходить. Поражение периферической нервной системы проявляется обычно как чувствительными, так и двигательными расстройствами. Возникают “беспричинные” сильные боли в конечностях с потерей кожной чувствительности, мышечной слабостью. Могут развиться миопатия или проксимальный мышечный синдром, проявляющийся полимиозитами, миастениеподобными симптомами. Таким образом, рак легкого нередко задолго до появления клинических признаков поражения органов дыхания “дышит в лицо врача” паранеопластическими (параканкрозными) симптомами. Поэтому вышеуказанные жалобы и изменения, особенно у мужчин старше 40 лет, всегда должны быть абсолютными показаниями к рентгенограмме легких, а при необходимости — бронхоскопии и бронхографии.
По мере прогрессирования процесса у больных появляются те или иные лег,очные симптомы. Вначале появляется легкий сухой кашель, преимущественно в ночное время; он постепенно становится приступообразным и мучительным. Затем появляется мокрота, которая в ряде случаев бывает гнойной, с неприятным запахом.
Кашель, даже упорный, не заставляет больных своевременно обратиться к врачу, поскольку большинство из них курит и страдает привычным кашлем курильщика. Обычно настораживает больных и приводит к врачу кровохарканье, которое связано с распадом опухоли или прорастанием ею сосудистых стенок. Боли в груди наблюдаются у 50-80 % больных. Они связаны с прогрессированием опухолевого процесса и прорастанием плевры или вовлечением ее в воспалительный процесс; прорастанием опухоли в трахею. Боли в груди бывают разнообразного характера и различной интенсивности. В одних случаях они постоянные, не связанные с дыханием, тупые и локальные, в других — могут возникать периодически, быть более острыми, особенно усиливаться при вдохе и иметь распространенный характер, но все же локализоваться на стороне поражения легкого. Одышка наблюдается у абсолютного большинства больных раком легких. В начале болезни в ее развитии преобладают рефлекторные механизмы, а в последующем — механическая обтурация просвета дренирующего бронха и выключение легкого из дыхания.
Весьма распространенными клиническими признаками запущенного рака легкого являются общая слабость и повышение температуры тела, которые обусловлены эндогенной раковой интоксикацией, сопутствующим воспалением легочной ткани, развитием осложнений.
Температурная реакция у некоторых больных развивается остро с подъемом до высоких цифр, носит гектический характер, в других случаях она постоянно держится на высоких и средних цифрах либо на уровне субфебрильной. У многих больных уменьшается масса тела. При прогрессировании опухолевого процесса возможно появление синдрома сдавления верхней полой вены (развитие коллатеральных, подкожных вен, отечность шеи, плечевого пояса, нарушение акта глотания, боль в области грудины, стридор); синдрома Панкоста (выраженная боль и нарушение функции плечевого пояса); синдрома неврологических нарушений (паралич диафрагмального и возвратного нервов, нервных узлов, при метастазировании в мозг возможны любые неврологические нарушения и смерть); карциноидного синдрома (приступ бронхиальной астмы, гипотензия, тахикардия, гиперемия лица и шеи, тошнота, рвота, понос); эктопических гормональных синдромов, обусловленных появлением различных биологически активных гуморальных факторов, образуемых самой опухолью; возникновение перифокального воспаления и плеврального выпота, ателектаза.
Стетоакустические данные зависят от стадии опухолевого процесса и его осложнений.
В периферической крови наиболее часто определяется повышение СОЭ, реже — лейкоцитоз, увеличивается количество старых форм тромбоцитов.
При обнаружении на флюорограммах патологических изменений (очаги, шаровидные образования, усиление легочного рисунка, ограниченное сегментом или долей, уплотнения легочной ткани с уменьшением их объема, ограниченные сегментом или долей, расширение корня и снижение дифференцировки его элементов, расширение или смещение средостения) назначаются дополнительно крупнокадровые флюорограммы в прямой и боковых проекциях в разные фазы дыхания и с прямым увеличением измененного участка легкого. В поликлинике больному производятся обзорные рентгенограммы в передней и боковой проекциях. Рентгенологическая картина центрального рака обусловлена самой опухолью, возникающим нарушением проходимости бронха, осложнениями, развивающимися в связи с прогрессирующим ростом опухоли и метастазами.
Бронхографически можно обнаружить дефект наполнения бронха с неровными контурами, а при обтурирующем раке -“культю”, или “ампутацию”, бронха. Бронхографическое исследование позволяет выявить концентрическое сужение бронхов на большом протяжении со значительным утолщением их стенок.
Рентгенологическая тень периферического рака размером 1-1,5 см обычно бывает полигональной формы, а если диаметр опухоли превышает 3-4 см — шаровидной. На форму растущей опухоли в легком существенно влияют эластическая тяга и давление легочной ткани в окружности.
В большинстве случаев контуры опухоли нечеткие и представлены различной формы тяжами, уходящими в окружающую легочную ткань. Интенсивность тени зависит от размеров опухолевого узла и степени его плотности. Структура тени в большинстве случаев неоднородная. Нередко она представляет собой как бы слипшиеся отдельные, прилежащие друг к другу, плотные округлые тени.
При периферическом раке легочный рисунок в окружности опухоли обычно изменен. Довольно часто можно видеть “дорожку” к корню легкого, обусловленную либо лимфангитом, либо перифокальным и периваскулярным ростом опухоли.
Томографическое исследование дополняет классическую картину — видна множественная узловатость единой на обычных рентгенограммах тени, хорошо контурируются полости распада, их внутренние и наружные стенки и т. д. Метастатические опухоли в легких при рентгенологическом исследовании представлены узловатыми тенями различного размера — от 0,2-0,3 см до 10-14 см и более.
Ценным методом обследования больного с подозрением на центральный рак легкого является бронхоскопия. К сожалению, в выявлении периферического рака она помогает мало.
Рак легкого в первую очередь следует дифференцировать с острой пневмонией затяжного течения, рецидивирующей пневмонией, абсцессом легких и кистой, туберкулезом легких и синдромом средней доли. Дифференциальная диагностика ракового обструктивного пневмонита и первичной острой пневмонии основывается на онкологической настороженности в случае рецидивирующей или нетипичной пневмонии у курящих лиц без “легочного” анамнеза в ракоопасном возрасте (40 лет и старше). В настоящее время должно быть взято заправило бронхологическое исследование таких больных.
Лечение. В выработке плана лечения и программы реабилитации больных раком легкого принимают участие прежде всего онколог, радиолог и терапевт. Лечение больных раком легкого в зависимости от гистологической структуры опухоли, распространенности процесса, функционального состояния органов и систем может осуществляться хирургическим, комбинированным (сочетание хирургического и лучевого), лучевым, химиотерапевтическим и комплексным методами.
В случае мелкоклеточного рака легкого ведущими методами являются химиотерапевтический и лучевой. При немелкоклеточном раке легкого основной метод лечения — хирургический (пневмонэктомия, лобэктомия или расширение операции через переднебоковой, боковой или заднебоковой хирургические доступы). Хирургическое лечение абсолютно противопоказано при кахексии и выраженной раковой интоксикации больного; тяжелых сопутствующих заболеваниях; распространении опухолевого процесса за пределы трахеобронхиальных лимфатических узлов и обширном прорастании опухоли в стенку грудной клетки, перикард, диафрагму и т. д.; наличии метастазов и прорастании опухоли в средостение; обнаружении опухолевых клеток в содержимом плевральной полости.
Отдаленные результаты хирургического лечения рака легкого зависят от комплекса клинико-биологических факторов, к которым относятся размер первичного новообразования, состояние внутригрудных лимфатических узлов, анатомический тип роста и гистологическая структура опухоли. Процент пятилетней выживаемости среди радикально оперированных больных остается в среднем на уровне 30 % и не имеет заметной тенденции к повышению. При наличии метастазов в лимфатических узлах величина опухоли на прогноз не влияет. Продолжительность жизни существенно зависит от состояния внутригрудных лимфатических узлов. Абсолютное большинство больных с метастазами в трахеобронхиальные, паратрахеальные и лимфатические узлы переднего средостения умирают в первые два года после операции.
Пятилетняя выживаемость больных, перенесших радикальную операцию, наибольшая при I и II стадии процесса и составляет соответственно 45-61 % и 27-43,5 %. Это обосновывает хирургическое вмешательство как основной метод лечения на этих стадиях болезни. Результаты лечения больных раком легкого существенно улучшаются в результате проведения предоперационной лучевой терапии, которая уменьшает перифокальное воспаление, предупреждает и уменьшает метастазирование во время операции и в послеоперационном периоде. Лучевая терапия в послеоперационном периоде обязательна при нерадикальных оперативных вмешательствах, когда из-за генерализации раковой опухоли невозможно удалить субклинические метастазы в регионарных лимфатических узлах и тканях по границе резекции легкого и бронха. Послеоперационная лучевая терапия начинается сразу после заживления раны, т. е. через 2-4 нед после операции. Она снижает биологическую активность опухолевых клеток, разрушает наиболее чувствительные элементы остатка опухоли, уменьшает скорость метастазирования. Лучевому воздействию подвергаются зоны паратрахеальных, корневых и медиастинальных лимфатических узлов, а также рубец легкого после резекции. Лучевая терапия как самостоятельный радикальный метод возможна при подведении к опухоли канцероцидной дозы и удовлетворительном общем состоянии больного. Суммарная очаговая доза на первичный очаг колеблется в зависимости от гистологической структуры опухоли в пределах 45-70 Гр.
Лучевая терапия как самостоятельный паллиативный метод проводится больным с метастазами в надключичную область, с экссудативным плевритом, при ателектазе легкого, при рецидиве после хирургического лечения, у ослабленных больных с длительной лихорадкой и болевым синдромом. Следует помнить, что лучевая терапия может вызвать лучевое повреждение легкого (лучевой пневмонит), радиогенную пневмонию, абсцедирование, массивное кровотечение в результате распада опухоли и окружающей ткани, активизацию туберкулеза легких, лучевой пневмосклероз. Возможны лучевое поражение сердца (миокардиодистрофия, миокардиосклероз, перикардит), проявляющееся различными нарушениями ритма и проводимости, ишемическими расстройствами, а также обострение ранее существовавшего заболевания сердца. Химиотерапия осуществляется по разным схемам противоопухолевыми препаратами: метотрексатом, эмбихином, адриамицином, фарморубицином, прокарбазином, винкристином, циклофосфаном, цисплатином и др. Мелкоклеточный рак легкого значительно чувствительнее к химиотерапии, чем немелкоклеточный. Химиотерапия позволяет предотвратить или отсрочить развитие метастазов и тем самым увеличить сроки ремиссии. Она может .проводиться в пред- и послеоперационном периодах в качестве дополнения к хирургическому лечению. В предоперационном периоде она осуществляется обычно в виде одного цикла, после которого через 1-3 нед выполняется операция. В послеоперационном периоде химиотерапия проводится при отсутствии послеоперационных осложнений через 3-4 нед после завершения лучевого лечения.
Выделяются несколько клинических диспансерных групп онкологических больных: 1а — больные с заболеваниями, подозрительными на злокачественные новообразования; 16 — больные с предопухолевыми заболеваниями; II — больные со злокачественными опухолями, подлежащие специальному лечению; Па- больные со злокачественными опухолями, подлежащие радикальному лечению; III — практически здоровые (излеченные от рака); ГУ — больные с заболеваниями в запущенной стадии, подлежащие лишь симптоматической терапии. Больные с ГУ стадией рака легкого переводятся на первую группу инвалид-
ности, со II-III стадиями — на вторую, лица, перенесшие пульмонэктомию, — на третью группу. После окончания курса лечения больные еще в течение года обычно являются нетрудоспособными.
Основные меры профилактики рака легкого: борьба с загрязнением атмосферного воздуха и профессиональными вредностями, прекращение курения табака, выявление и лечение хронических заболеваний легких и в первую очередь хронического бронхита. Последний можно предупредить путем закаливания организма, регулярных занятий физкультурой и спортом, ежедневного выполнения комплекса упражнений гигиенической гимнастики, выработкой с детства привычки правильно дышать носом.
САРКОИДОЗ ЛЕГКИХ. Саркоидоз (болезнь Бенье-Бека-Шауманна) — это доброкачественное системное заболевание мезенхимы из группы гранулематозов, характеризующееся образованием эпителиоидноклеточных неказеозных гранулем, которые в последующем полностью рассасываются или замещаются гиалиновой соединительной тканью. Саркоидозный процесс, генерализуясь в ретикулогистиоцитарной системе, может поражать почти все ткани и органы, в первую очередь легкие и лимфатические узлы (80-90 %), печень и селезенку. Помимо этих органов при саркоидозе часто поражаются кожа (узловатая эритема, подкожные узелки), глаза (увеит, иридоциклит, кератоконъюнктивит), кости и суставы (артриты, множественные кисты в костях фаланг пальцев кистей и стоп), почки (нефрокальциноз, нефролитиаз, редко — интерстициальный нефрит), околоушные и слюнные железы и другие органы.
Этиология саркоидоза не установлена, хотя имеется несколько гипотез по поводу вызывающих его факторов.
В легких саркоидозные изменения начинаются с альвеол. Вначале развивается интерстициальный пневмонит или альвеолит, а затем образуются саркоидозные гранулемы в перибронхиолярной и субплевральной интерстициальной тканях и вдоль междолевых перегородок. Саркоидная гранулема состоит из эпителиоидных клеток и окружена мононуклеарами. В более поздней стадии болезни появляются гигантские многоядерные клетки Пирогова-Лангханса. Затем от периферии гранулемы к ее центру развивается фиброз, который постепенно превращает эту гранулему в бесклеточную гиалиновую массу.
При прогрессировании легочного процесса возникают выраженные вентиляционные нарушения, как правило рестриктивного типа. Если лимфатические узлы сдавливают стенки бронхов, то могут возникнуть вентиляционные нарушения обструктивного типа, а в отдельных случаях развиваются участки гиповентиляции и ателектазы. Различаются три стадии поражения органов дыхания. I стадия проявляется двусторонним, чаще асимметричным, увеличением паратрахеальных, трахеобронхиальных, бифуркационных и бронхопульмональных лимфоузлов; II стадия — двусторонней диссеминацией (милиарной, очаговой) и (или) инфильтрацией, связанной с корнем легкого преимущественно в его средних и нижних отделах; III стадия — значительным пневмосклерозом (фиброзом) и крупными, обычно сливными фокусными образованиями.
Клиническая картина и диагноз. Саркоидоз как системное заболевание может поражать все органы: легкие -почти всегда, другие органы реже. Поэтому клиническая картина определяется пораженным органом и степенью анатомо-функциональных нарушений. Выделяются две основные формы течения саркоидоза: острая и первично-хроническая. Острая форма саркоидоза обозначается как синдром Лефгрена. Клинически характеризуется триадой: узловатой эритемой, артралгиями и увеличением лимфатических узлов корней легких. Начало болезни зачастую бурное. На фоне высокой температуры и общей слабости появляются сильные боли в крупных суставах и узловатые уплотнения на коже размерами от 1-2 до 10 см в диаметре (пятна). В центре уплотнения — покраснения, болезненные, теплее окружающей кожи. Узловатая эритема сохраняется 2- 4 нед, иногда несколько месяцев. Она рассасывается без образования рубцов.
Полиартралгии в большинстве случаев предшествуют узловатой эритеме. Между появлением полиартралгии и увеличением лимфатических узлов в корнях легких может пройти несколько месяцев.
Первично-хроническая форма заболевания почти всегда начинается незаметно и выявляется чаще всего на основании увеличения лимфатических узлов в корнях легких, определяемых при рентгенологическом обследовании грудной клетки. В начальной стадии заболевания брльные жалуются на общую слабость, недомогание, плохой аппетит, потливость, боли в мышцах или суставах. Затем появляются сухой кашель и боли в грудной клетке, в тяжелых случаях возможно раннее появление одышки при физической нагрузке. В стадии выраженных легочных изменений больных беспокоят одышка, кашель с мокротой, боли в грудной клетке при дыхании и др.
При осмотре обращает на себя внимание диффузный цианоз. Перкуторно определяется высокое стояние нижней границы легких; при аускультации — влажные звонкие хрипы в проекции нижних долей легких, реже — сухие хрипы над отдельными участками.
При прогрессировании бронхолегочного саркоидозного процесса постепенно формируется хроническое легочное сердце.
При физикальном обследовании можно обнаружить внегрудные проявления саркоидоза. Чаще всего выявляется увеличение периферических лимфатических узлов, обычно шейных, надключичных, реже — подмышечных, паховых и локтевых. Они плотноэластичной консистенции, безболезненные, не спаяны с окружающей клетчаткой, не размягчаются и не образуют свищей.
У некоторых больных легочные симптомы сочетаются с умеренно выраженными артритами кистей, а также лучезапястных и коленных суставов.
Можно иногда наблюдать безболезненное увеличение слюнных околоушных желез, порой в сочетании с увеитом и лихорадкой. Весьма характерны кожные проявления саркоидоза. При мелкоузелковом саркоидозе на лице, верхней части туловища (в виде пелерины) и разгибательных поверхностях верхних конечностей появляются узелки, безболезненные, четко очерченные, красновато-синюшные или коричневые, размером от булавочной головки до горошины. Со временем они уплощаются, на их месте остаются пигментация или поверхностная атрофия кожи с пигментированным ободком и телеангиэктазии. Крупноузелковый саркоидоз проявляется немногочисленными (от 1 до 10) узелками более крупных размеров (иногда до лесного ореха), которые локализуются обычно на коже лица, шеи, реже — верхних конечностей. Очень крупноузелковый саркоидоз возникает на нижних конечностях. Эти высыпания могут годами оставаться без изменений, затем их центральная часть постепенно западает, становится атрофичной, пигментированной или депигментированной, выявляются телеангиэктазии. Болезнь длится от нескольких месяцев до нескольких лет. Возможно спонтанное выздоровление. Клинический прогноз острой формы саркоидоза обычно благоприятный. Чем стремительнее начало болезни, тем быстрее наступает ремиссия. При острых формах в 60-80 % случаев наблюдается спонтанная ремиссия в течение 12 мес.
Для клинической картины первично-хронической формы саркоидоза характерно несоответствие между незначительными субъективными проявлениями болезни (как общими, так и со стороны легких) и значительной степенью выраженности рентгеноморфологических изменений. Спонтанные ремиссии бывают только у 20-30 % больных.
Летальность при саркоидозе — 5-10 %. Рецидивы после спонтанного излечения возникают редко. Чаще всего они возникают в случаях, склонных к хроническому течению.
Саркоидоз легких может осложниться развитием бронхообтурационного синдрома, эмфиземы легких, дыхательной недостаточности, легочного сердца.
При остром течении саркоидоза изменяются лабораторные показатели, свидетельствующие о воспалительном процессе, например СОЭ увеличивается умеренно или сильно, наблюдаются лейкоцитоз с эозинофилией, лимфо- и моноцитоз. Первоначальное увеличение содержания альфа- и бета-глобулинов по мере возрастания длительности заболевания сменяется повышением титра гамма-глобулинов.
Рентгенологически в начальной стадии саркоидоза легких определяется расширение корней легких и средостения за счет опухолевидного увеличения всех групп лимфатических узлов грудной полости, преимущественно лимфатических узлов корней легких. Очертания корней легких и средостения имеют полициклический характер, тени передних и задних групп лимфатических узлов средостения, накладываясь друг на друга, создают симптом “кулис”, увеличение лимфатических узлов средостения из-за суммирования теней придает сердцу митральную конфигурацию.
На томограммах можно выявить увеличенные лимфатические узлы, которые располагаются вокруг крупных бронхов в области их деления на долевые, сегментарные и субсегментарные ветви.
В последующем характерны рентгенологическая картина очаговой диссеминации: избыточный, петлистый рисунок в прикорневых и нижних отделах легких, мелкие (милиарные) очаги, очаги средней величины диаметром 3-5 мм, крупные очаги диаметром более 6 мм; наличие распространенного фиброза, участков цирроза легких.
У 50-70 % больных саркоидозом может быть положительная реакция Квейма — проба выполняется путем внутрикожного введения 0,1 -0,2 мл специфического антигену (субстрат саркоидной ткани больного). Через 2-3 нед на месте инъекции появляется багрово-красный узелок, который еще через 2-3 нед подвергается биопсии. Отсутствие стандартного антигена и большая отсроченмость результатов пробы ограничивают ее диагностические возможности. Важное значение для диагностики имеют гистологические или цитологические исследования удаленных лимфатических узлов, кожи, слизистой оболочки бронхов, в которых обнаруживаются элементы саркоидной гранулемы.
Дифференциальную диагностику до обнаружения характерных для саркоидоза гранулем нужно проводить со многими заболеваниями, особенно системного характера.
Внутригрудную форму саркоидоза в первой стадии процесса следует дифференцировать с туберкулезом внутригрудных лимфатических узлов, медиастинальной формой лимфогранулематоза; во второй-третьей стадиях — с диссеминированным туберкулезом легких, карциноматозом, пневмокониозами, реже — с другими диссеминированными поражениями легких.
Лечение. Поскольку саркоидоз легких имеет этиологическое, патоморфологическое и клинико-рентгенологическое сходство с туберкулезом легких, подавляющее большинство больных наблюдаются фтизиатрами и лечатся в противотуберкулезных диспансерах.
В случае подтверждения диагноза при отсутствии клинических проявлений многие авторы предлагают воздержаться от активного лечения в течение 6-8 мес и лишь систематически наблюдать за больным. Если в течение этого времени болезни отмечаются замедленная регрессия или отсутствие благоприятной рентгенологической динамики в виде рассасывания диссеминации в легких и уменьшения размеров внутригрудных лимфатических узлов, осуществляется лечение глюкокортикоидами.
Основными показаниями к лечению служат явные клинические проявления и прогрессирующий характер заболевания, наличие генерализованных форм, комбинированные поражения различных органов, поражение внутригрудных лимфатических узлов при их значительном увеличении, выраженная диссеминация в легких.
Курс лечения обычно продолжается 6-8 мес и более. Его необходимо начинать в условиях стационара. Лечение включает в себя глюкокортикостероидные гормоны (чаще всего преднизолон), нестероидные противовоспалительные средства (аспирин, индометацин и др.), иммунодепрессивные препараты (азатиоприн, делагил, резохин и др.), антиоксиданты (токоферола ацетат, ретинол и др.), противотуберкулезные препараты (изониазид, этионамид, ПАСК натрия и др.), тиосульфат натрия.
В последние годы в комплексное лечение больных саркоидозом легких с целью немедикаментозной иммунокоррекции рекомендуется включать экстракорпоральную гемосорбцию и ультрафиолетовое облучение аутокрови.
Больные саркоидозом могут быть направлены на лечение в санатории общего профиля в любых климатических зонах.
Источник: www.adventus.info
 NEOSENSYS.COM Симптомы, диагностика и методы лечения заболеваний.
NEOSENSYS.COM Симптомы, диагностика и методы лечения заболеваний.